よむ、つかう、まなぶ。
2 先進医療Bに係る新規技術の科学的評価等について(別紙2)[3.7MB] (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00111.html |
| 出典情報 | 先進医療会議(第149回 12/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
2.NASOX 療法の日本国内での使用状況を説明してください。
【回答】
NASOX 療法は切除不能膵癌に対する緩和的化学療法、また切除可能膵癌の周術期補助化学療法と
もに日本国内での診療実績はありません。
類似レジメンである NALIRIFOX 療法が切除不能膵癌の一次治療として国内第 II 相試験を実施されたと
ころであり、今後日常臨床での使用が期待されている状況です。
3.NASOX 療法を術前に使用した際に周術期に想定されるリスクを説明してください。
【回答】
NASOX 療法を術前に使用した際に周術期で想定されるリスクとして、術前化学療法(NASOX)中の有害事
象と周術期(手術や術後)の合併症の増加が考えられます。
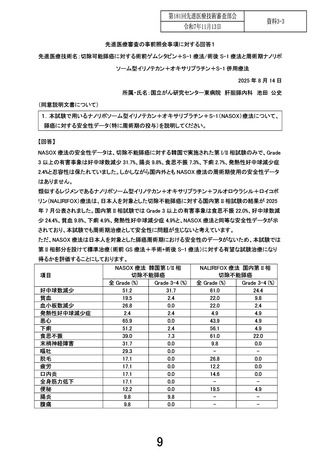
術前ゲムシタビン+S-1(GS)療法は、Prep-02/JSAP-05 試験で Grade 3 以上の有害事象は、好中球数減
少 57.6%、食欲不振 7.6%、発熱性好中球減少症 6.4%でした。一方、切除不能膵癌での NASOX 療法(韓国
での第 I/II 相試験)では、Grade 3 以上の有害事象は好中球数減少 31.7%、腸炎 9.8%、食思不振 7.3%、下
痢 2.7%、発熱性好中球減少症 2.4%で、術前 GS 療法より著しくリスクが増加するとは言えないと考えていま
す。
次に術前 NASOX 療法による周術期合併症は、骨髄抑制の残存による感染症や出血、また下痢や粘膜炎に
関連した栄養状態低下により創傷治癒遅延や浮腫・腹水のリスクが想定されます。
本試験では術前化学療法最終コースの最終投与日を day 0 として day 0-14 に有効性評価のための画像検
査を行い、day 21-56 に手術を行うこと、また手術適応規準を設けることとしており、十分な有事事象からの回
復し周術期のリスクの最小化を図ることとしています。
4. 切除可能膵癌の判定について、施設間でのばらつきを抑えるため中央判定の必要性について説
明してください
【回答】
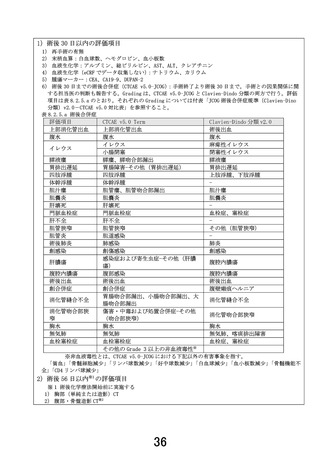
膵癌の切除可能性分類は、ダイナミック CT による腫瘍の進展度、特に腹部主要脈管への浸潤・接触程
度を評価し、標準的な手術により癌遺残のない手術が可能かどうかの視点で、切除可能、切除可能境
界、切除不能に分類されます。客観的かつ簡便に評価が可能であり、現在では広く世界中で臨床試験
や治療アルゴリズムに導入されています。米国で 2006 年ごろより定義されましたが、本邦でも 2016 年
に改訂された膵癌取扱い規約第 7 版に切除可能性分類が正式に記載され、以降、日常臨床において
広く普及しています。国内で現在進行中の切除可能膵癌を対象とした臨床試験(JCOG2101C, 2202)で
は、切除可能膵癌の判定の施設間のばらつきは十分に小さいと考えられ、本試験でも中央判定の必要
性はないと考えます。
以上
10
【回答】
NASOX 療法は切除不能膵癌に対する緩和的化学療法、また切除可能膵癌の周術期補助化学療法と
もに日本国内での診療実績はありません。
類似レジメンである NALIRIFOX 療法が切除不能膵癌の一次治療として国内第 II 相試験を実施されたと
ころであり、今後日常臨床での使用が期待されている状況です。
3.NASOX 療法を術前に使用した際に周術期に想定されるリスクを説明してください。
【回答】
NASOX 療法を術前に使用した際に周術期で想定されるリスクとして、術前化学療法(NASOX)中の有害事
象と周術期(手術や術後)の合併症の増加が考えられます。
術前ゲムシタビン+S-1(GS)療法は、Prep-02/JSAP-05 試験で Grade 3 以上の有害事象は、好中球数減
少 57.6%、食欲不振 7.6%、発熱性好中球減少症 6.4%でした。一方、切除不能膵癌での NASOX 療法(韓国
での第 I/II 相試験)では、Grade 3 以上の有害事象は好中球数減少 31.7%、腸炎 9.8%、食思不振 7.3%、下
痢 2.7%、発熱性好中球減少症 2.4%で、術前 GS 療法より著しくリスクが増加するとは言えないと考えていま
す。
次に術前 NASOX 療法による周術期合併症は、骨髄抑制の残存による感染症や出血、また下痢や粘膜炎に
関連した栄養状態低下により創傷治癒遅延や浮腫・腹水のリスクが想定されます。
本試験では術前化学療法最終コースの最終投与日を day 0 として day 0-14 に有効性評価のための画像検
査を行い、day 21-56 に手術を行うこと、また手術適応規準を設けることとしており、十分な有事事象からの回
復し周術期のリスクの最小化を図ることとしています。
4. 切除可能膵癌の判定について、施設間でのばらつきを抑えるため中央判定の必要性について説
明してください
【回答】
膵癌の切除可能性分類は、ダイナミック CT による腫瘍の進展度、特に腹部主要脈管への浸潤・接触程
度を評価し、標準的な手術により癌遺残のない手術が可能かどうかの視点で、切除可能、切除可能境
界、切除不能に分類されます。客観的かつ簡便に評価が可能であり、現在では広く世界中で臨床試験
や治療アルゴリズムに導入されています。米国で 2006 年ごろより定義されましたが、本邦でも 2016 年
に改訂された膵癌取扱い規約第 7 版に切除可能性分類が正式に記載され、以降、日常臨床において
広く普及しています。国内で現在進行中の切除可能膵癌を対象とした臨床試験(JCOG2101C, 2202)で
は、切除可能膵癌の判定の施設間のばらつきは十分に小さいと考えられ、本試験でも中央判定の必要
性はないと考えます。
以上
10