よむ、つかう、まなぶ。
2 先進医療Bに係る新規技術の科学的評価等について(別紙2)[3.7MB] (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00111.html |
| 出典情報 | 先進医療会議(第149回 12/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
・安全性が確かめられなかったときは、全部の試験が中止になると思いますが、どのように安全性を確
かめるのかについての記載がありません。ランダム試験のパートの場合、安全性をどのような形で確か
めたかについて、説明した上での同意が必要だと思いますが、その点について、記載がないのはどうし
てでしょうか。24 頁の利益不利益のところに、安全性についての記載をいつの段階で、どのように記載
するのでしょうか。
>貴重なご指摘ありがとうございます。安全性が確認できない場合には、試験全体の中止も含め試験の
計画を再考いたします。ご指摘の通り、パート毎にどのような評価を行うかについての記載がなかったた
め、「4.この臨床試験の治療法について」において、それぞれのパートの目的に以下のように追記しまし
た。
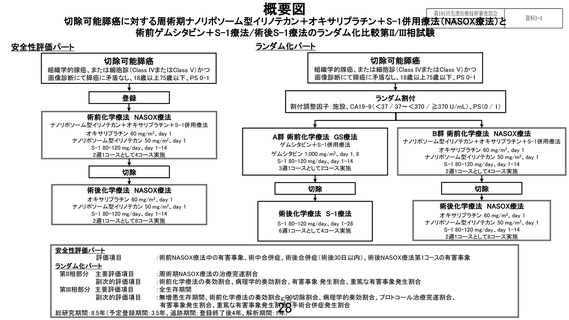
①試験治療の安全性を評価するパートの目的:術前 NASOX 療法中の副作用や、手術中・手術後の合
併症の評価を行います。
②標準治療と試験治療の 2 つの治療法を比較するパートの目的:それぞれの治療法ごとの生存期間や
増悪しない期間などの効果と、術前・術後化学療法の副作用や手術の合併症などの安全性の評価を行
います。
ご指摘の「8. 臨床試験の参加に伴って期待される利益と予想される不利益」への安全性に関する記載
について、安全性評価パートの結果を踏まえて追記を検討いたします。
・安全パートの参加者とランダム試験の参加者の同意文書のフォームが同じなのはなぜでしょうか。ラン
ダム試験であることについては、特別に項目として挙げる必要があると思います。
>ご指摘ありがとうございます。安全性パートで行う NASOX 療法は、ランダム化パートにおいても同じ治
療内容(治療方法・スケジュール・想定される副作用など)となるため、同意文書を統一した形にしており
ます。なお、文書内には両パートが存在すること、それぞれの患者さんがどちらのパートに該当するかが
明記されておりますので、このままの形でご対応させていただければ幸いです。
3. (副作用について)
10 頁以下の副作用についてですが、NASOX を術前術後に投与する場合、同じ薬の量が増えること
になりますが、量による副作用の違いはないのでしょうか。もしあるとしたら、それについて記載してく
ださい。
【回答】
ご指摘ありがとうございます。量とは総投与量との認識でよろしいでしょうか。NASOX 療法で用いるオキ
サリプラチンにおいて総投与量が増加することで末梢神経障害の増悪が懸念されます。そのため、説明
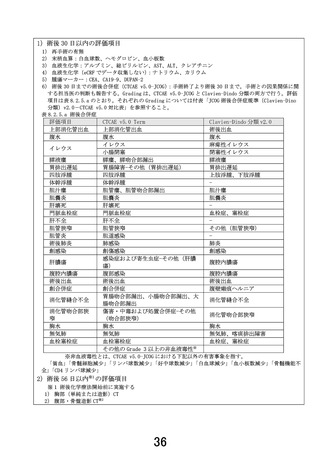
文書での起こりやすい副作用、⑧末梢神経障害(しびれ)、「治療を繰り返していくと、手指や足先にしび
れが出現しはじめ、徐々に悪化します。」と記載しております。
以上
16
かめるのかについての記載がありません。ランダム試験のパートの場合、安全性をどのような形で確か
めたかについて、説明した上での同意が必要だと思いますが、その点について、記載がないのはどうし
てでしょうか。24 頁の利益不利益のところに、安全性についての記載をいつの段階で、どのように記載
するのでしょうか。
>貴重なご指摘ありがとうございます。安全性が確認できない場合には、試験全体の中止も含め試験の
計画を再考いたします。ご指摘の通り、パート毎にどのような評価を行うかについての記載がなかったた
め、「4.この臨床試験の治療法について」において、それぞれのパートの目的に以下のように追記しまし
た。
①試験治療の安全性を評価するパートの目的:術前 NASOX 療法中の副作用や、手術中・手術後の合
併症の評価を行います。
②標準治療と試験治療の 2 つの治療法を比較するパートの目的:それぞれの治療法ごとの生存期間や
増悪しない期間などの効果と、術前・術後化学療法の副作用や手術の合併症などの安全性の評価を行
います。
ご指摘の「8. 臨床試験の参加に伴って期待される利益と予想される不利益」への安全性に関する記載
について、安全性評価パートの結果を踏まえて追記を検討いたします。
・安全パートの参加者とランダム試験の参加者の同意文書のフォームが同じなのはなぜでしょうか。ラン
ダム試験であることについては、特別に項目として挙げる必要があると思います。
>ご指摘ありがとうございます。安全性パートで行う NASOX 療法は、ランダム化パートにおいても同じ治
療内容(治療方法・スケジュール・想定される副作用など)となるため、同意文書を統一した形にしており
ます。なお、文書内には両パートが存在すること、それぞれの患者さんがどちらのパートに該当するかが
明記されておりますので、このままの形でご対応させていただければ幸いです。
3. (副作用について)
10 頁以下の副作用についてですが、NASOX を術前術後に投与する場合、同じ薬の量が増えること
になりますが、量による副作用の違いはないのでしょうか。もしあるとしたら、それについて記載してく
ださい。
【回答】
ご指摘ありがとうございます。量とは総投与量との認識でよろしいでしょうか。NASOX 療法で用いるオキ
サリプラチンにおいて総投与量が増加することで末梢神経障害の増悪が懸念されます。そのため、説明
文書での起こりやすい副作用、⑧末梢神経障害(しびれ)、「治療を繰り返していくと、手指や足先にしび
れが出現しはじめ、徐々に悪化します。」と記載しております。
以上
16