よむ、つかう、まなぶ。
2 先進医療Bに係る新規技術の科学的評価等について(別紙2)[3.7MB] (20 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00111.html |
| 出典情報 | 先進医療会議(第149回 12/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
用しか発現しないと誤解しないでしょうか。15ページ目も術後 NASOX 補助化学療法中に発現した副
作用によって現在の標準治療である S-1 療法が受けられなくなるリスクも説明すべきでしょう。
【回答】
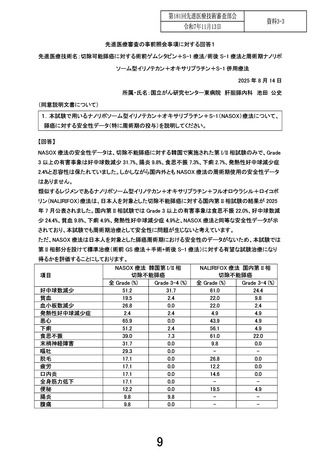
1)ご指摘の通り、NAPOLI3 では治療関連死亡が 2%と報告されております。一方、日本人の遠隔転移を
有する膵癌患者 41 人を対象とした NALIRIFOX 療法の第 II 相試験の結果が 2025 年 7 月の膵臓学会で
公表されましたが、治療関連死亡は報告されておりません。治療関連死亡の可能性は標準治療群、試
験治療群いずれにもあると考えられますので、「5. 副作用・合併症について」の「1)化学療法」の最後に
以下の追記を行うようにいたします。
「また、これらの副作用以外にもさまざまな副作用が発生することがあります。さらに、発生頻度は低い
ですが、重篤な場合には命に関わることや、手術や化学療法の継続が困難となることがあります。」
2)ご指摘いただいた、8 ページの表の術後 NASOX 療法の副作用ですが、術後 NASOX 療法のデータは
ありません。そのため韓国での進行癌における NASOX 療法のデータ、また本邦における S-IROX 療法、
オキサリプラチン、ナノリポソーム型イリノテカン、S-1 の添付文書などから代表的な副作用を引用してお
ります。術前 NASOX 療法と同様の副作用を記載しておりますが、想定されるものについては幅広く記載
しており、このままにさせていただければ幸いです。
3)ご指摘の通り、術後 NASOX 療法の副作用により、試験治療継続困難と判断され、中止となった場合
には、標準治療である術後 S-1 療法も受けられなくリスクもあると考えられます。1)に記載させていただ
きました通り、この臨床試験で受けられた化学療法により手術や化学療法の継続が困難となることがあ
ることを追記させていただきます。
3. 申請された書類に表のずれや誤記が散見されます。もう一度記載整備をお願いします。
例 先進医療実施届出書の p20 追跡調査時の増悪の、p10 表 6.1.1.a 投与量と投与スケジュール等
【回答】
このたびは、申請書類において表のずれや誤記がございましたこと、申し訳ございません。
ご指摘を踏まえ、全体の記載内容および表の整合性を再確認し、修正版を作成いたしました。
特に以下の箇所について修正を行っております。
・先進医療実施届出書 p20:追跡調査時の増悪に関する記載が「追跡調査時の」で文が途切れていた
箇所を修正し、文意が明確になるよう整備
・先進医療実施届出書 p10 表 6.1.1.a:投与量および投与スケジュールの誤記を修正するとともに、他の
投与スケジュールの表における表記揺れも併せて整備
以上
20
作用によって現在の標準治療である S-1 療法が受けられなくなるリスクも説明すべきでしょう。
【回答】
1)ご指摘の通り、NAPOLI3 では治療関連死亡が 2%と報告されております。一方、日本人の遠隔転移を
有する膵癌患者 41 人を対象とした NALIRIFOX 療法の第 II 相試験の結果が 2025 年 7 月の膵臓学会で
公表されましたが、治療関連死亡は報告されておりません。治療関連死亡の可能性は標準治療群、試
験治療群いずれにもあると考えられますので、「5. 副作用・合併症について」の「1)化学療法」の最後に
以下の追記を行うようにいたします。
「また、これらの副作用以外にもさまざまな副作用が発生することがあります。さらに、発生頻度は低い
ですが、重篤な場合には命に関わることや、手術や化学療法の継続が困難となることがあります。」
2)ご指摘いただいた、8 ページの表の術後 NASOX 療法の副作用ですが、術後 NASOX 療法のデータは
ありません。そのため韓国での進行癌における NASOX 療法のデータ、また本邦における S-IROX 療法、
オキサリプラチン、ナノリポソーム型イリノテカン、S-1 の添付文書などから代表的な副作用を引用してお
ります。術前 NASOX 療法と同様の副作用を記載しておりますが、想定されるものについては幅広く記載
しており、このままにさせていただければ幸いです。
3)ご指摘の通り、術後 NASOX 療法の副作用により、試験治療継続困難と判断され、中止となった場合
には、標準治療である術後 S-1 療法も受けられなくリスクもあると考えられます。1)に記載させていただ
きました通り、この臨床試験で受けられた化学療法により手術や化学療法の継続が困難となることがあ
ることを追記させていただきます。
3. 申請された書類に表のずれや誤記が散見されます。もう一度記載整備をお願いします。
例 先進医療実施届出書の p20 追跡調査時の増悪の、p10 表 6.1.1.a 投与量と投与スケジュール等
【回答】
このたびは、申請書類において表のずれや誤記がございましたこと、申し訳ございません。
ご指摘を踏まえ、全体の記載内容および表の整合性を再確認し、修正版を作成いたしました。
特に以下の箇所について修正を行っております。
・先進医療実施届出書 p20:追跡調査時の増悪に関する記載が「追跡調査時の」で文が途切れていた
箇所を修正し、文意が明確になるよう整備
・先進医療実施届出書 p10 表 6.1.1.a:投与量および投与スケジュールの誤記を修正するとともに、他の
投与スケジュールの表における表記揺れも併せて整備
以上
20