総-8個別事項について(その5)がん対策・難病対策・透析医療・緩和ケア[6.7MB] (27 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_65606.html |
| 出典情報 | 中央社会保険医療協議会 総会(第624回 11/5)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
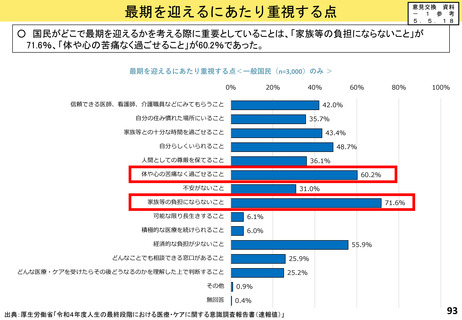
○
○
C-CATより医療機関に提供される調査結果の改訂のイメージは以下のとおり。
当該調査結果およびがん遺伝子パネル検査結果に基づいて、主治医において、EPの省略の可否の判断を行うことが可能となる。
例:非小細胞肺癌患者に対してがん遺伝子パネル検査を行った場合(いずれも二次的所見疑いなし)
1)国内承認薬(コンパニオン診断薬)に到達可能な場合の調査結果の例
省略可能/不可
検査結果サマリー(患者ID:01)
薬剤到達性
薬剤名
CDx
マーカー
国内承認
Osimertinib
適合
EGFR L858R
国内承認
Afatinib
適合
EGFR L858R
国内承認
Erlotinib
適合
EGFR L858R
国内承認
Dacomitinib
適合
EGFR L858R
省略可能
検査に用いた医療機器等がコンパニオン診断としての性能を有しており、当該遺伝子変異に
対応する国内承認薬が存在する等、がん遺伝子パネル検査に基づく治療の存在が明らか
2)国内承認薬がないものの、国内の治験等にアクセス可能な場合の調査結果の例
検査結果サマリー(患者ID:02)
薬剤到達性
臨床試験名
臨床試験
AMG 193 + docetaxel
マーカー
CDKN2A Loss
省略不可
3)国内承認薬やアクセス可能な治験等がない場合の調査結果の例
検査結果サマリー(患者ID:03)
薬剤到達性
該当なし
マーカー
該当なし
省略可能
使用可能な国内承認薬やアクセス可能な治験等がなく、がん遺伝子パネル検査に基づく治療
の不存在が明らか
出典:C-CAT提供資料を元に健康・生活衛生局がん・疾病対策課で作成
27