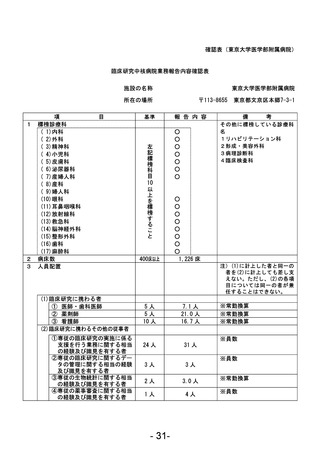
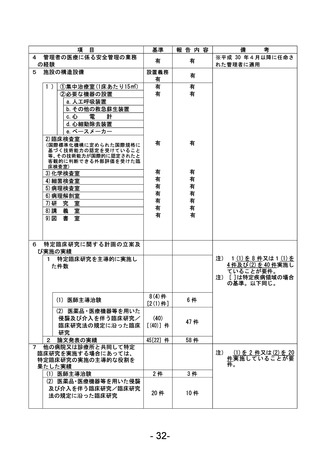
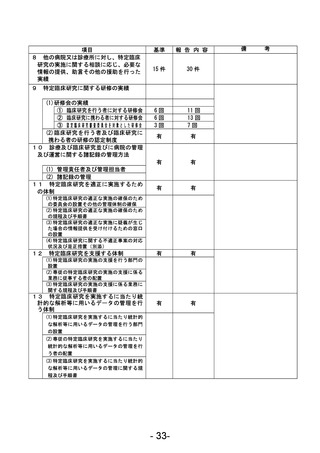
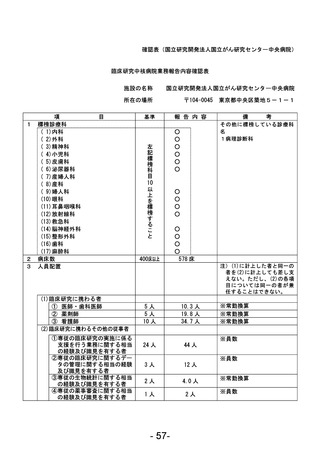
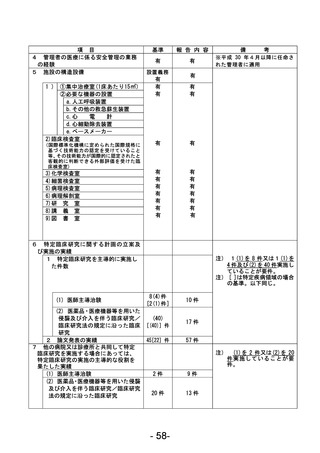
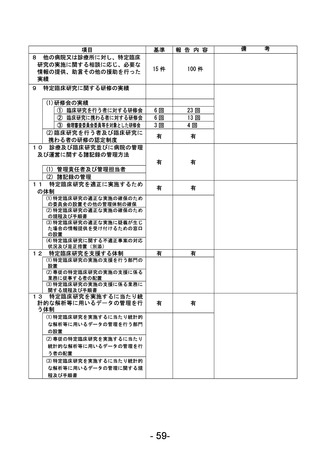
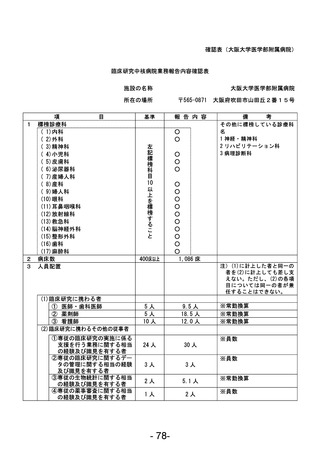
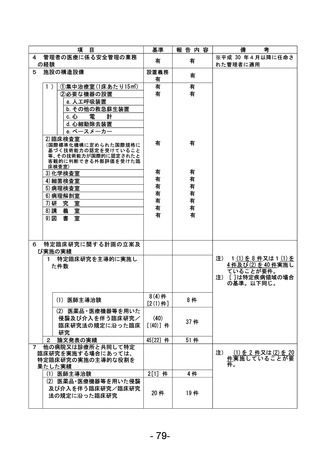
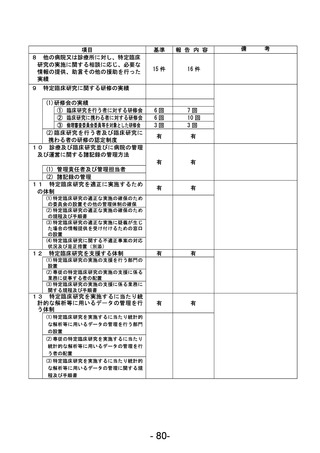
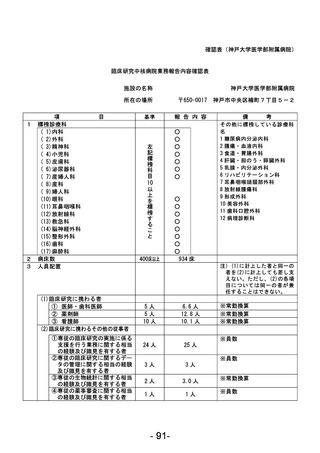
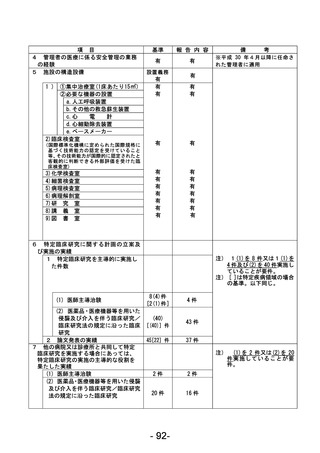
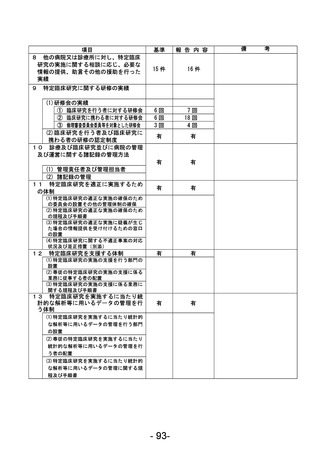
資料1 臨床研究中核病院業務報告内容確認表 (88 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62409.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第44回 8/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
なお、担当モニターは確認不足により、作成日が 2023/8/24 の ICF で外部へ印刷依頼をし、そのまま
CRC へ送付していた。また CRC は、ICF 受領時に版数は確認していたが作成日及び ICF の内容を確認
していなかった。
不適正事案に関する対応状況:
2023/10/26:被験者来院時、IRB 未承認の ICF 第 4 限(作成日 2023/8/24)を用いて同意取得していた
ことを謝罪。改訂内容を再度説明し、ICF 第 4 版(作成日 2023/9/21)にて再同意を取得。
PI は被験者に不利益はなく治験継続可能と判断。
是正措置:
・PI は同意説明文書入手時及び同意説明前に ICF の版数だけでなく、作成日、改訂内容も併せて確
認するよう CRC へ指導した。
・PI は同意取得前に ICF の版数、作成日を確認するよう担当医師へ指導した。
登録 ID 等
****
治験・臨床研究名
****
不適正事案の概要:過量投与及びそれに伴う服薬遵守率(80%)の未達
2023 年 11 月 8 日に担当 CRC が治験薬の残薬数を確認した所、予定より 12 錠が不足していたことか
ら、本事象が判明した。被験者へは、以下①~④を指導していた。①1 日 1 回 6 錠朝食後 30 分以内
に服薬すること、②服薬後すぐに電子服薬日誌に服薬した旨記録すること、③過量投与を防ぐため服
薬したか不明な場合は服薬しないこと、そのことを CRC に連絡すること。④処方時に、服薬期間(6
日間)をボトル側面に貼付し、各ボトルの予定残薬数(6 錠)を被験者に共有し、残薬数が異なる場
合は担当 CRC に連絡するよう指導していた。また規定来院が 1 週間毎のため、その都度治験薬の残薬
数を CRC が確認することで服薬過誤がないようサポートしていた。本事例は、11 月 4 日及び 11 月 5
日に、治験薬服薬後に服薬日誌を起動したが、起動に時間を要したため、その間に他の用事を行い、
その後、服薬日誌を入力する際に当日の服薬をしていないと思い、再度治験薬を服薬したために生じ
たと考えられた。服薬後すぐに服薬日誌に記録しなかった服薬手順に逸脱があった。
不適正事案に関する対応状況:
発生当日に被験者の全身状態の確認と血液・尿検査、心電図検査を実施し、結果から明らかな異常所
見を認めなかった。被験者の安全性に問題はなく、治験担当医師により治験継続可能と判断された。
被験者へ服薬についての再指導に加えて、服薬日誌を起動させてから治験薬を服薬することと、服薬
後服薬日誌へ記録するまでは他の作業を行わないことを指導した。
是正措置:
被験者へ服薬手順を遵守することの重要性を担当 CRC が説明した。治験薬を服薬したか不明な場合
は必ず担当 CRC へ連絡するよう伝えた。当該被験者を含め、本治験参加中の全被験者に対し、毎回来
院時に服薬から服薬日誌の記録までの流れを確認し、必要時診察にて再指導を行うこととした。
登録 ID 等
****
****
治験
不適正事案の概要:治験期間中に異なる PET スキャナーで撮像したことによる主要評価項目の解析・
評価に影響を与える逸脱
2023 年 12 月 6 日に被験者は外部委託機関にてアミロイド PET 検査を実施。2023 年 12 月 8 日に当院
の CRC が外部委託機関から検査終了報告書を受領した際、スクリーニング時と異なるスキャナーを
使用していたことに気づき外部委託期間に問い合わせたところ、外部委託期間の CRC の思い込みが
原因で検査技師に測定依頼したことが判明した。
不適正事案に関する対応状況:
2023 年 12 月 11 日に CRC から PI へ報告し、被験者の安全性に問題はなく、治験継続可能と判断を得
た。依頼者より、アミロイド PET のスキャナーが治験期間中で異なると、主要評価項目である脳内
- 87-