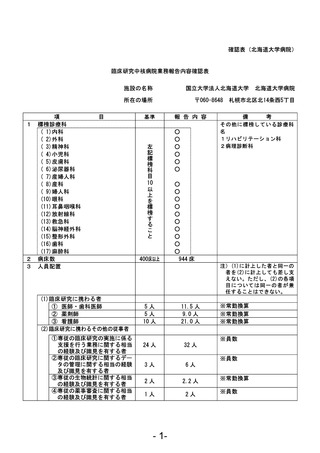
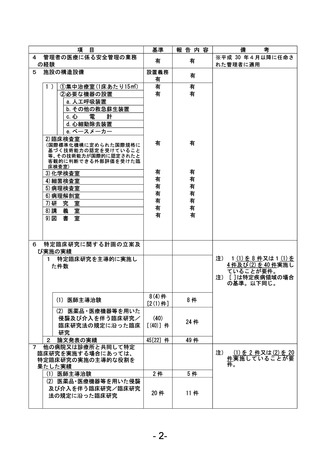
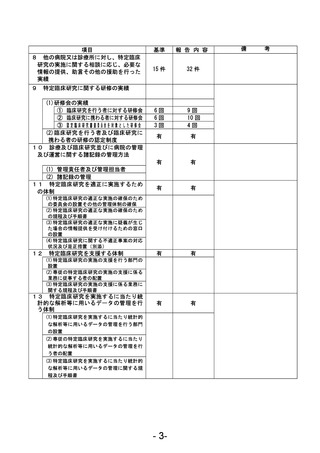
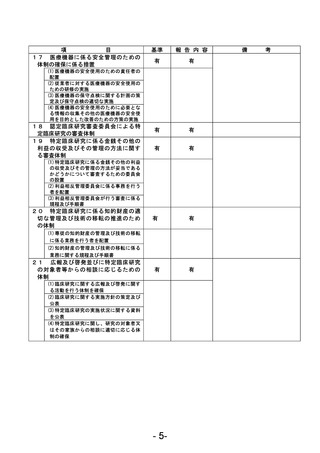
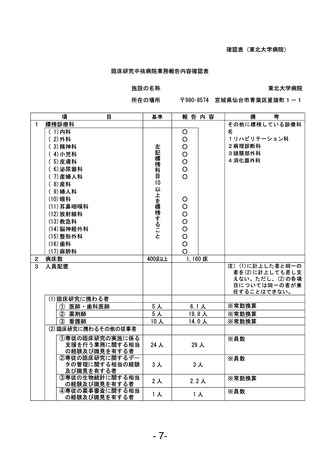
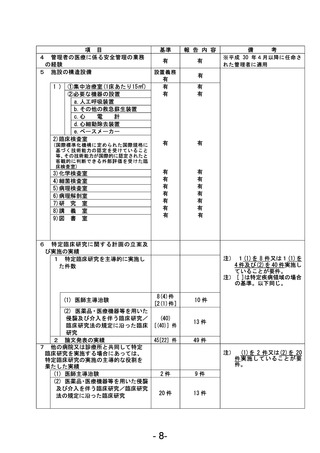
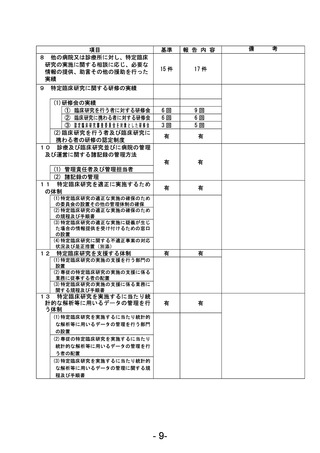
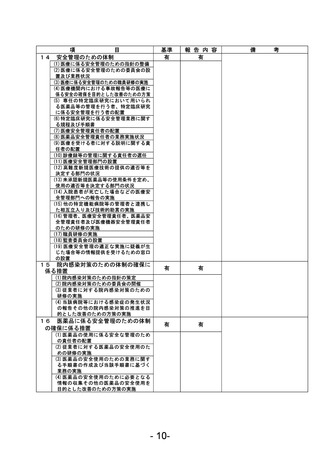
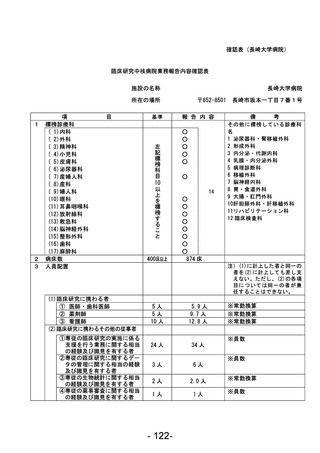
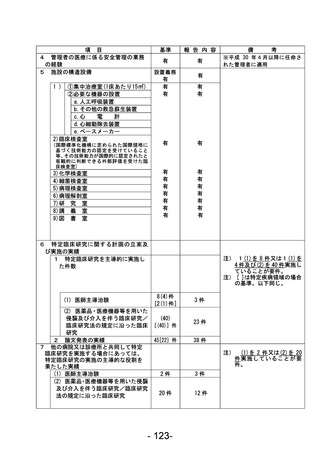
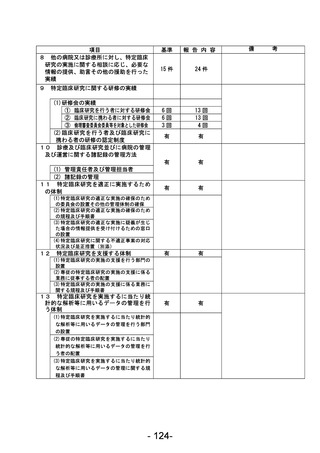
資料1 臨床研究中核病院業務報告内容確認表 (121 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62409.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第44回 8/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
登録 ID 等
****
治験・臨床研究名
****
不適正事案の概要:選択基準7)の抗がん剤のウォッシュアウト期間及び併用禁止薬の使用
被験者はセレコキシブを内服していた。依頼者より、本試験の有効性への影響リスクを踏まえ服用
中止の依頼があり、*/*/*規定来院時に患者と協議し服用を中止とした。今回依頼者より、セレ
コキシブが対象疾患に対する抗がん剤の治療にあたるという見解がでたため、PRTの抗がん剤のWash
out期間の逸脱と併用禁止薬の使用にあたると指摘され逸脱となった。
不適正事案に関する対応状況:
安全性情報管理委員会および臨床研究管理委員会へ報告を行った。
是正措置:
試験に重要な情報は、メールだけではなくレター等の発行、また CRC だけではなく、医師に連絡する
よう依頼者へ依頼した。
登録 ID 等
****
治験・臨床研究名
****
不適正事案の概要:除外基準抵触
*年*月*日 担当医が無作為化前適格性を確認し適格と判断。無作為化を実施後、治験薬投与開
始。
*年*月*日 担当医が他の症例を確認中、除外基準1-f)*について認識。当該被験者のスクリー
ング時にメディカルモニターへ相談をしていないことに気が付き、担当モニターへ連絡。担当モニ
ターよりメディカルモニターへ報告した。
2024年1月25日 担当モニターより、重大な逸脱ではあるが治験継続可能と連絡あり。
*除外基準1 医学的条件
f) 肺縮小術若しくは肺移植の既往歴がある又はスクリーニング前12ヵ月以内に肺移植若しくは肺縮小術を受ける予
定がある。治験参加者が肺線維症以外の他の疾患(肺癌等)のために肺手術を受けたことがある場合は、メディカ
ルモニターに相談すること。
不適正事案に関する対応状況:
*年*月*日 担当医は除外基準抵触と今後の治験治療についてご本人へ説明を行い、被験者の希
望により治験継続となった。
是正措置:
適格除外基準ワークシートを改訂し、スクリーニング適格性確認用と投与前適格性確認用の 2 種類
を使用する。CRC では判断が難しい項目は、特に注意して確認いただくよう医師へ依頼する。プロト
コルを再確認する。
登録 ID 等
****
治験・臨床研究名
****
不適正事案の概要:併用禁止薬使用
*年*月*日 ご本人より*月*日夕方に倦怠感のため自己判断でキューピーコーワゴールドを
服薬したことを聴取した。
*年*月*日 SDV実施後、担当モニターからの「Site Monitoring Visit Follow up Letter」に
てキューピーコーワゴールドが併用禁止に該当する旨連絡を受けた。
- 120-