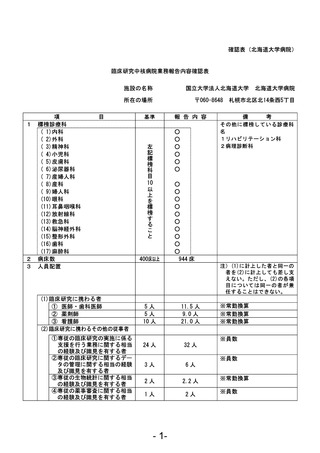
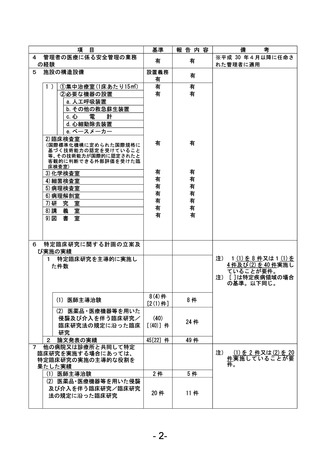
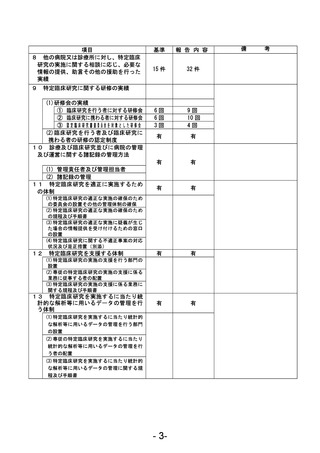
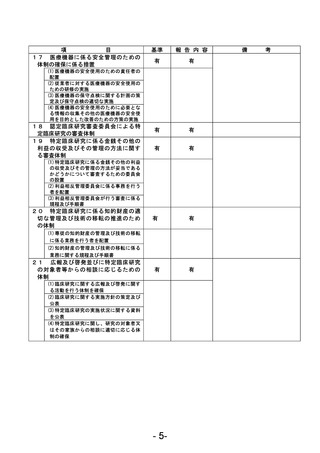
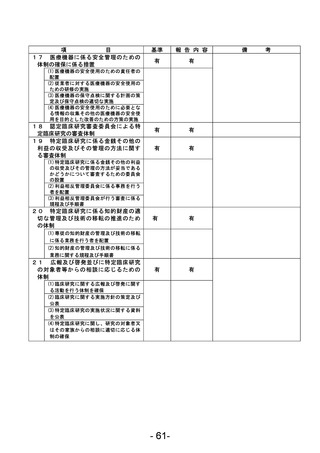
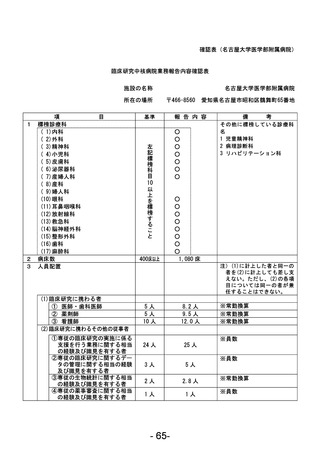
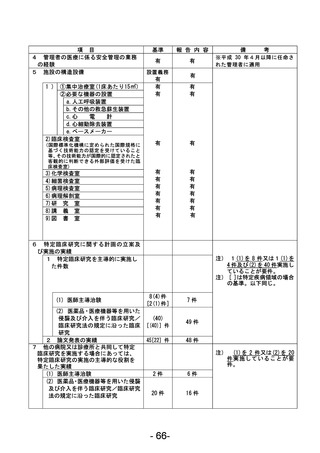
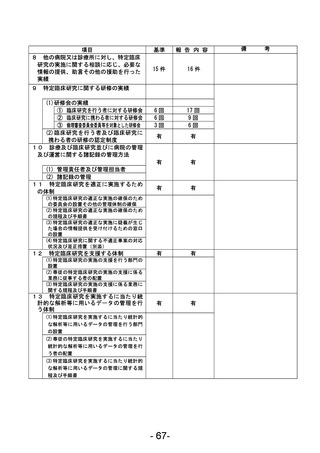
資料1 臨床研究中核病院業務報告内容確認表 (22 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62409.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第44回 8/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
治 療 に 関 す る 単 群 検 証 的 試 験
(JCOG1807C)
不適正事案の概要:
当該研究計画では適応外使用となる術前デュルバルマブ療法において試験薬提供者からの提供薬(
試験薬)を使用することとしていた。2023年5月16日及び5月30日に研究対象者1名において、研究分
担医師の理解が十分でなく、保険診療用の市販の薬剤を処方し、使用した。また、保険請求され、
研究対象者が一部負担金の支払いを行った。2023年8月29日に薬剤部にて在庫確認を行っていた際に
発覚し、9月1日に研究責任医師に報告された。
不適正事案に関する対応状況:
試験薬と同一成分、投与量であり研究対象者への身体への影響は無い。
2023年9月8日に研究対象者本人に説明、謝罪され、経緯について了承された。また、保険請求を取
り下げし、2023年9月15日の外来通院時に、研究対象者に一部負担金が返金された。
当該事案は2023年9月12日に臨床研究適正実施推進部会(同日に病院長)に報告された。
2023 年 10 月 4 日に臨床研究適正実施推進部会の部会員(臨床研究支援部門長、臨床研究企画部長及
び品質管理担当者)が当該研究分担医師に不適合の内容、原因及び当該実施診療科としての再発防止
策に関してインタビューを行い、病院長及び副院長(研究担当)にその結果を報告した。
発生原因としては、プロトコール規定上手術実施の有無に応じて、手術が実施される場合は試験薬
が投与され(適応外使用)、手術が実施されない場合は市販の同じ薬剤が保険診療で投与されるこ
とになっており複雑であり、そのチェック体制が十分でなかったことが考えられた。また、試験薬
と投与された市販薬の有効成分は同じものであり研究対象者の安全性に問題はなかったものの、誤
った薬剤を投与したことを重大と判断して研究者として報告を行ったとのことであった。
当該事案は、上記インタビュー結果も含め、再度、2023年10月10日に臨床研究適正実施推進部会に
報告され、承認された。また、2023年10月18日に臨床研究管理委員会に報告され、承認された。
研究代表医師は、2023年9月20日に認定臨床研究審査委員会に重大な不適合報告にて当該事案を報告
し、2023年10月12日に認定臨床研究審査委員会にて審査され、承認された。
当該事案について、2023 年 12 月 21 日に東病院公式 HP で公開された。
当該研究は先進医療B制度下で実施しているため、厚生労働省医政局研究開発政策課へ報告を行った
。2023年11月9日の第155回先進医療技術審査部会にて本件については議論が行われ、承認された。
(再発防止策などに対してのコメントは無し)
是正措置:
・処方する可能性のある院内の医師に再度、下記運用の周知を行い、再発防止に努める。
適応外部分のデュルバルマブの投与は術前の2コースと手術が行われた後の術後補助療法としての
デュルバルマブ投与22コースである。これらの処方の際は、呼吸器外科ファイルに保存されてい
るレジメン登録されている「先進B)デュルバルマブ」のファイルを適用すれば処方箋にも先進B
と記載される運用になっている。ただし、手術が行われなかった研究対象者においては、追加22
コースのデュルバルマブ療法は通常の保険診療として処方する必要がある。
・研究対象者の登録後、デュルバルマブの投与まで期間が空くため、初回投与日が決まり次第、呼
吸器外科秘書より薬剤部へ情報共有を行い、投与日を確実に把握していく。また、研究対象者が登
録された時点で、研究補助員が電子カルテの患者掲示板に赤字太文字で「JCOG1807C(先進B)本登
録患者の術前と術後のデュルバルマブは研究用の薬剤を処方すること」と記載する。また、電子カ
- 21-