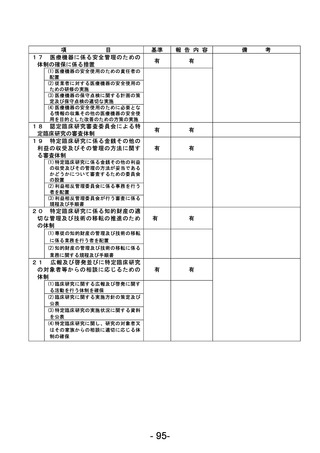
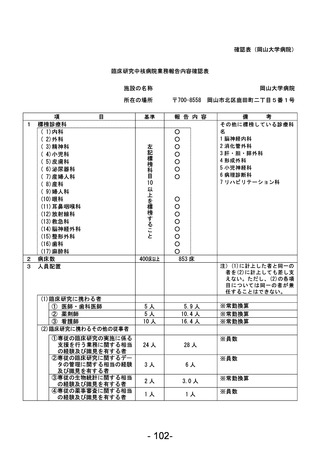
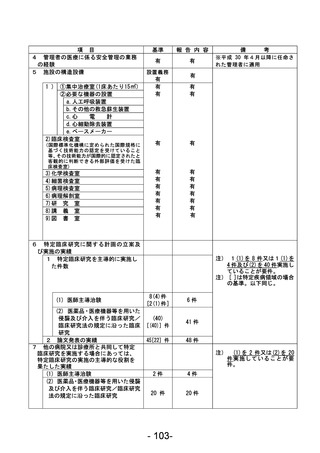
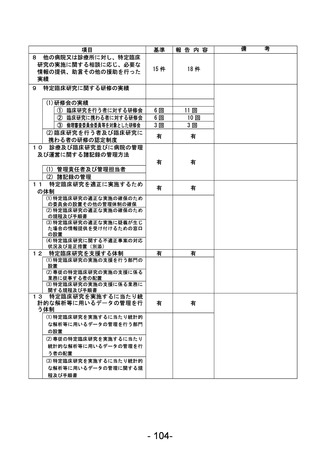
資料1 臨床研究中核病院業務報告内容確認表 (63 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62409.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第44回 8/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
3
特定臨床研究に関する不適正事案
登録 ID 等
****
治験・臨床研究名
****
不適正事案の概要:
除外基準に「脳転移を有するもの」と定められていたところ、基準を満たさない脳転移のある患者を
登録し、治験薬投与を開始した。
2023 年 10 月 20 日に Module1 コホートの同意を取得した。同年 10 月 31 日にスクリーニング検査を
実施したところ、無症候性の現時点で治療不要な脳転移を認めた。除外基準に「脳転移を有する者。
ただし、治療を受け、症状がなく、安定しており、AZD9592 の初回投与前 2 週間以上にわたり、
prednisone 換算で 10mg/ 日を超えるステロイド剤の継続投与を必要としない場合を除く。」と規
定されていたことから、11 月 7 日に治験依頼者の当院担当者へ当該症例が登録可能か問い合わせし
た。担当者から、「無症候性で直近の治療を必要としない脳転移であればこれまで無治療であっても
組み入れ可能」と回答を得た。登録可能と回答を得たことから、同年 11 月 14 日、治験薬投与を開始
した。しかし、同年 12 月 11 日に、治験依頼者内で Global Study Team から共有される資料を再確認
したところ、治験依頼者の担当者が確認した脳転移の見解は、Module1 以外のコホートに適応される
ものであり、Module1 の場合は治験参加以前に脳転移に対し無治療な患者は組み入れ不可であること
が発覚した。同日、担当モニターより、除外基準に抵触する連絡があり、逸脱対応で治験継続となっ
た。
不適正事案に関する対応状況:
被験者へ説明し、謝罪した。治験継続の意思を確認し、治験を継続した。
除外基準の抵触に伴う有害事象は認めず、同年 12 月 25 日の有効性画像評価において、脳転移の縮小
を認めた。事案発覚後から 2024 年 2 月 7 日まで関係部門で原因分析を行い、同年 2 月 7 日に病院長
へ報告し、同年 3 月 19 日の治験・臨床研究運営委員会で周知した。
是正措置:
治験責任医師から、Module1の無治療の脳転移患者の組み入れは不可であることを、治験分担医師や
関係者へ周知した。
登録 ID 等
****
治験・臨床研究名
****
不適正事案の概要:
先進医療 B として実施している特定臨床研究において、予定登録期間(2023 年 2 月末まで)を過ぎ
ていたが、当初の研究実施計画書に記載されていた総研究期間内(2025 年 2 月末まで)ではあった
ことから、予定登録期間および総研究期間の延長手続きが承認される前に 2 例の症例登録を行った。
2023 年 6 月に予定登録期間および総研究期間の延長について先進医療会議に変更申請をしたところ、
予定登録期間が過ぎていることについて指摘を受けた。
不適正事案に関する対応状況:
厚生労働省および先進医療会議より指摘を受け、2023 年 8 月に全施設で症例登録を停止した。2024
年 9 月 4 日に病院長ならびに CRB に不適合報告を行うとともに、原因分析・是正措置の検討を行っ
- 62-