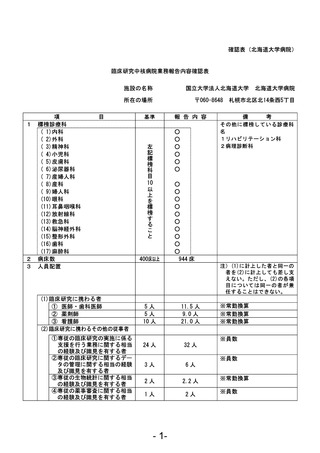
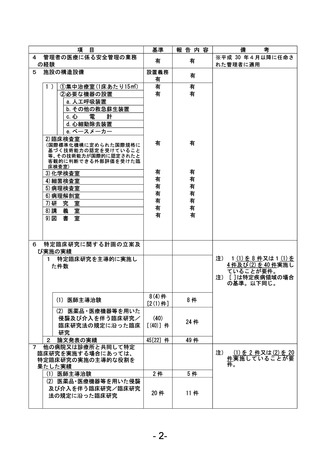
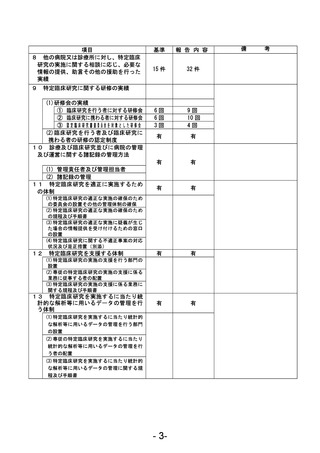
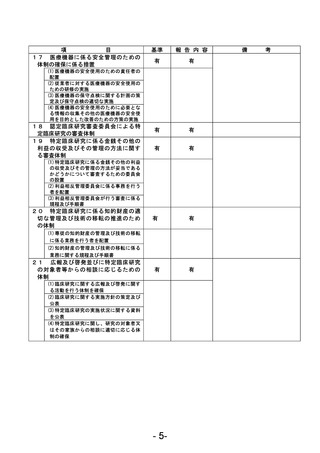
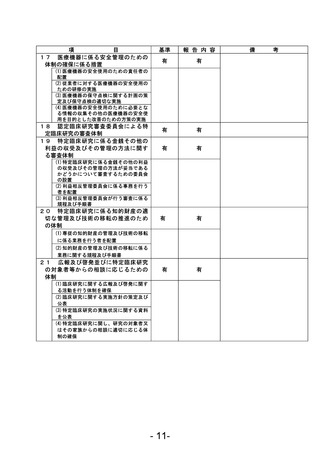
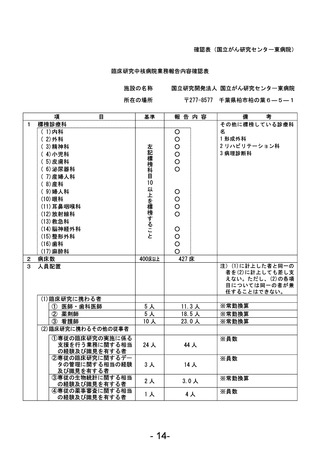
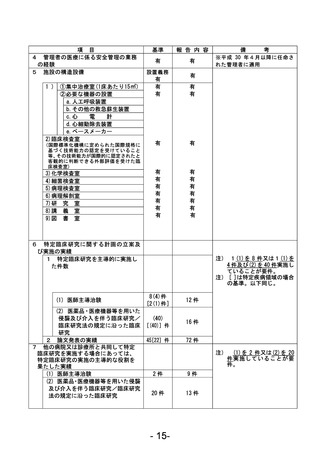
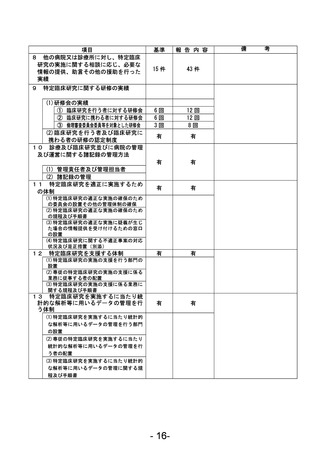
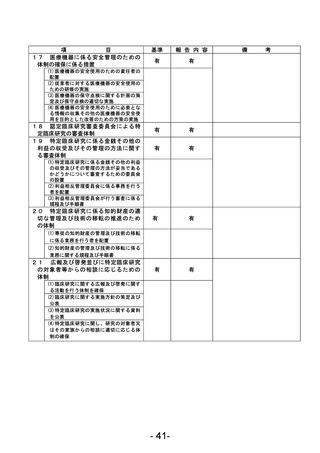
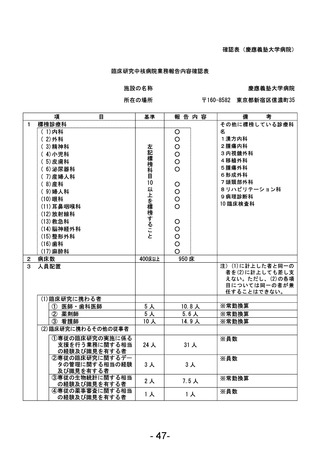
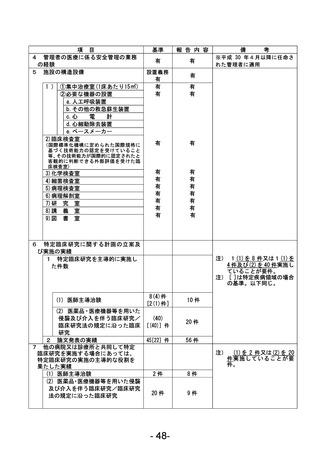
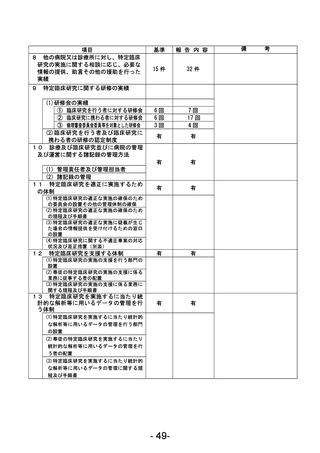
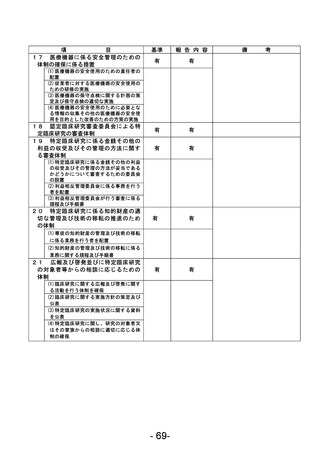
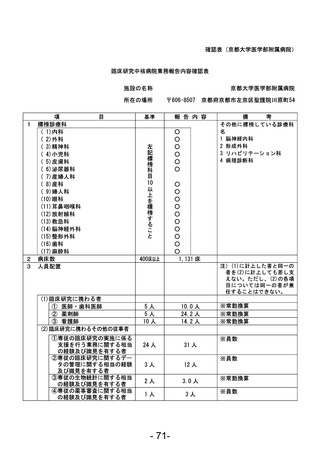
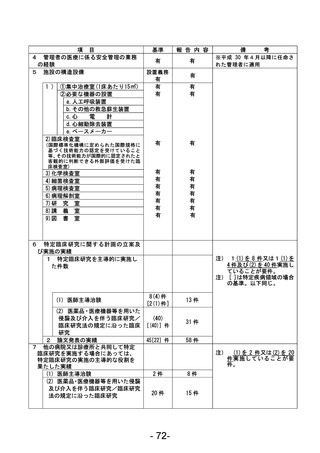
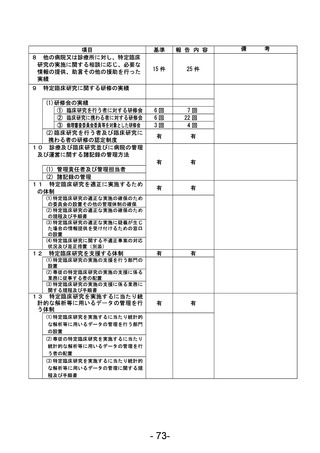
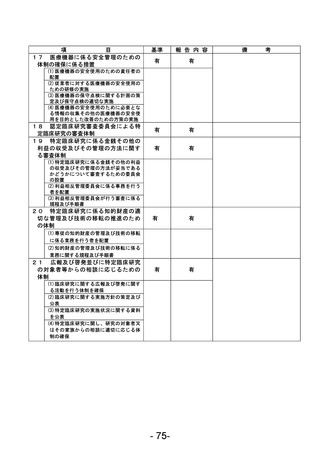
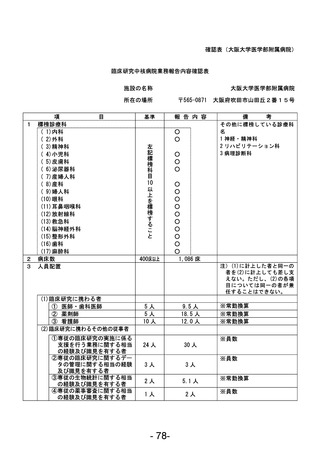
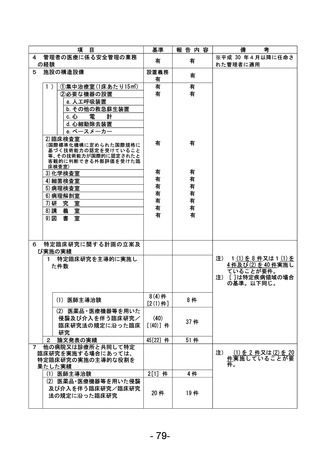
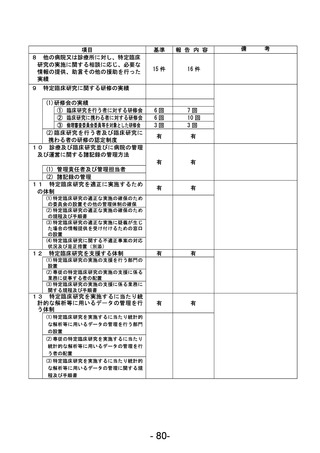
資料1 臨床研究中核病院業務報告内容確認表 (120 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62409.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第44回 8/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
安全性情報管理委員会、臨床研究管理委員会にて報告した。
是正措置:
併用禁止薬が多数あること、薬剤処方時は治験責任医師、分担医師に確認が必要であることを、改め
て電子カルテ上の掲示板に目につきやすいよう具体的に表示する。併用禁止薬を記載する際によく
使う薬剤が想定される場合は、一部掲示板に挙げておくことも検討する。
登録 ID 等
****
治験・臨床研究名
****
不適正事案の概要:併用禁止薬使用
*年*月*日 被験者より電話にて「咽頭痛のためロキソニンを内服してよいか」との問い合わせ
あり。経口鎮痛剤は使用不可であることを伝えたところ、*日(*)にカロナール200㎎2錠を1回使
用していたことが発覚した。
不適正事案に関する対応状況:
依頼者に報告し、体調不良等なければ治験責任医師の判断で治験薬継続可の見解あり、投与継続と
した。被験者には鎮痛剤内服は控えるよう説明し、了承を得た。
安全性情報管理委員会および臨床研究管理委員会へ報告を行った。
是正措置:
被験者へ併用禁止薬について再度説明を行い、引き続き内服希望の薬剤がある場合は、連絡してい
ただく旨を伝えた。併せて、土日祝日の連絡先についても改めて確認を行った。
登録 ID 等
****
治験・臨床研究名
****
不適正事案の概要:併用禁止薬使用後の検査未実施での治験薬投与再開
*年*月*日 他院にて、脊柱管狭窄症に対して、左L1/2椎弓形成術、左L2/3外側ヘルニア摘出術
、L3/4/5左側進入両側開窓術実施。安全性を考慮し手術前の *月*日から休薬し、*月*日に電
話連絡にて術後経過を確認したうえで治験薬を再開し、術後経過問題なく *月*日に退院した。
*/*/*他院から手紙にて、手術時に併用禁止薬(プロポフォール)が使用されていることが分か
った。
プロトコルには、「QTを延長することが知られている薬剤の併用投与が必要で他の治療法に変更で
きない場合は、ニロチニブ(治験薬)の投与を中断しなければならない。ニロチニブ療法を再開す
る場合は、再開前に心電図検査を実施しなければならない。」と規定されており、心電図を実施せ
ず治験薬投与を再開したため、逸脱となった。
不適正事案に関する対応状況:
*/*/*に治験規定のため来院し、12 誘導心電図実施、安全性について問題はなく、治験薬投与継
続可能と判断し、投与継続となった。
安全性情報管理委員会および臨床研究管理委員会へ報告を行った。
是正措置:
併用禁止薬を使用する可能性がある場合には、来院し、12 誘導心電図実施し、安全性を確認した上
で、治験薬再開することを徹底するとともに、使用する薬剤については可能な限り早めに情報収集す
るよう努める。
- 119-