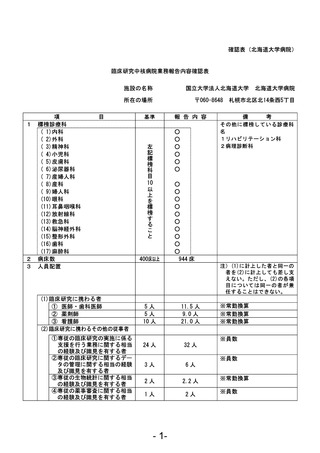
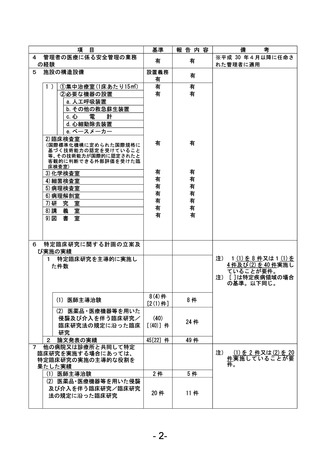
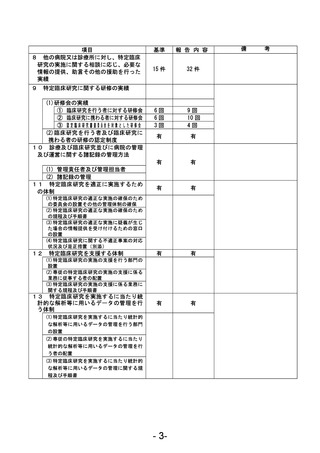
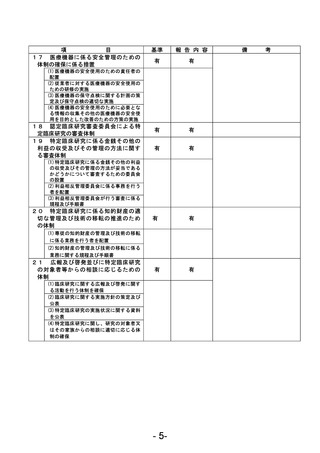
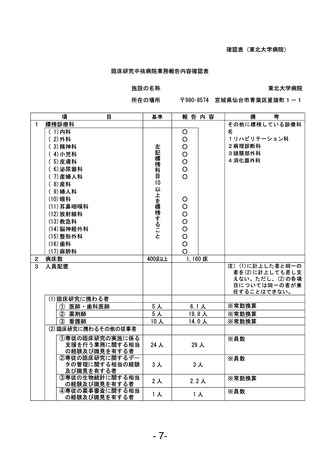
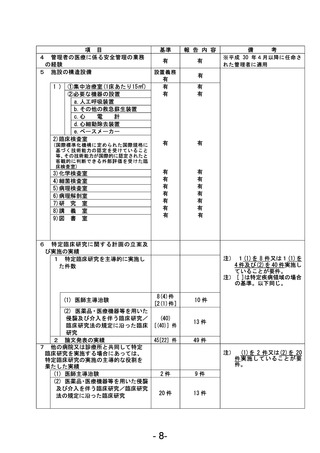
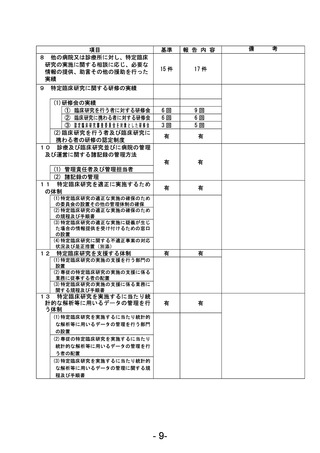
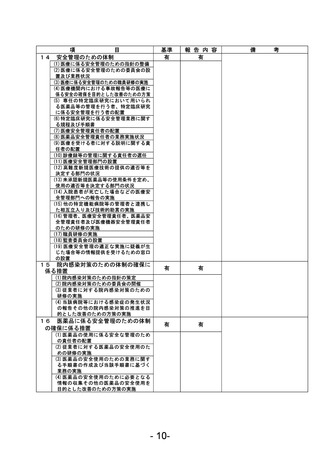
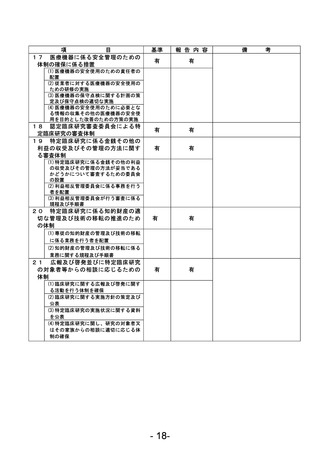
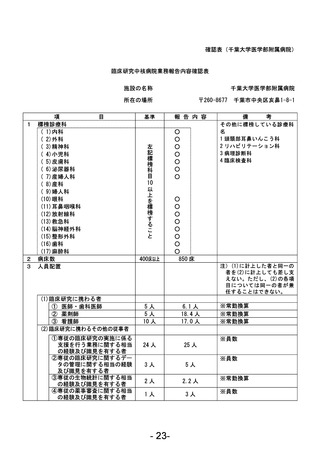
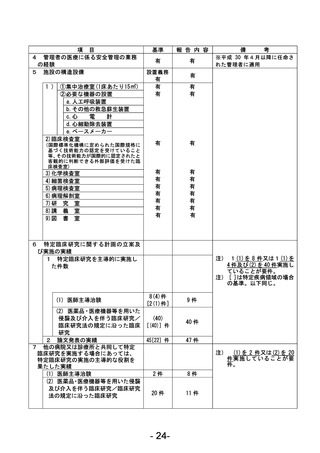
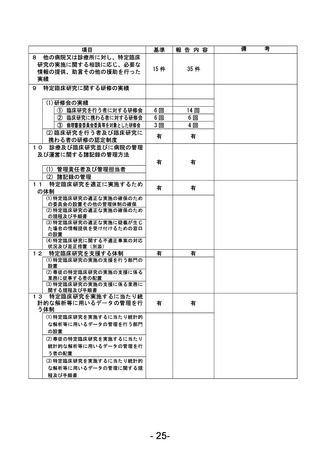
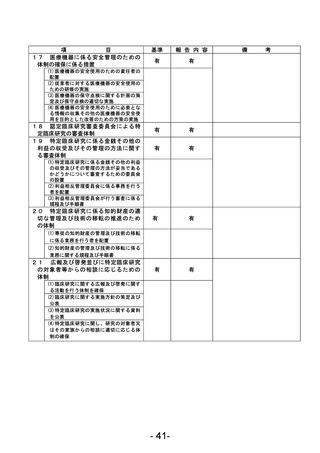
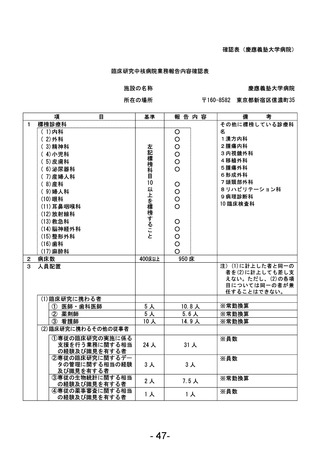
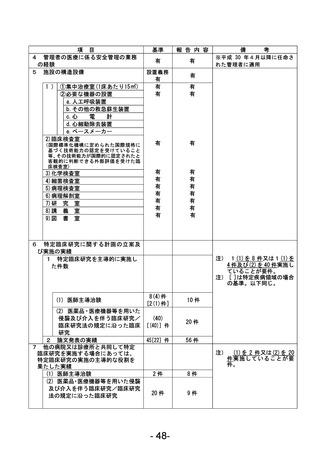
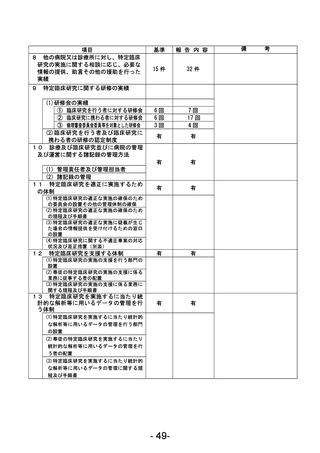
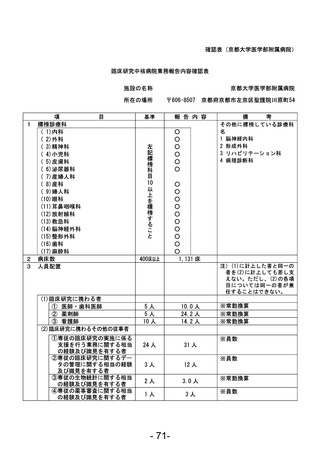
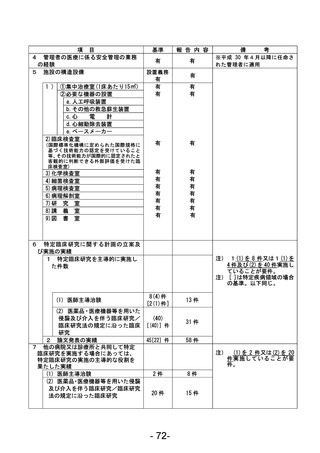
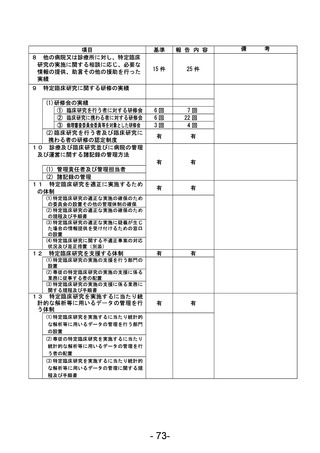
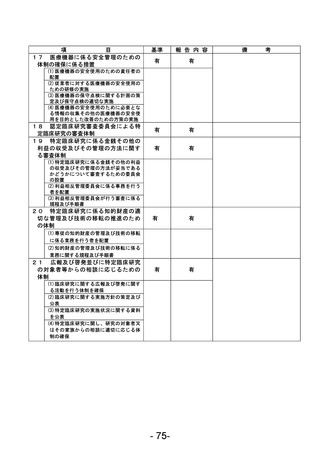
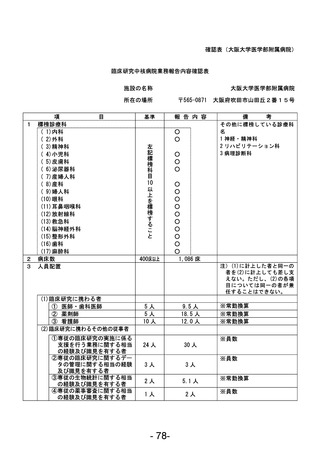
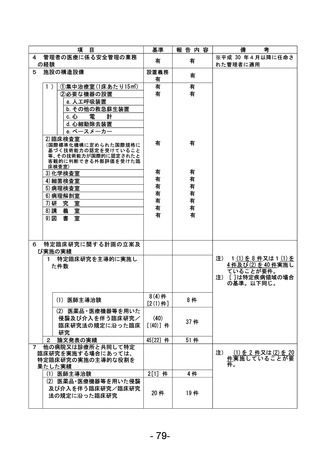
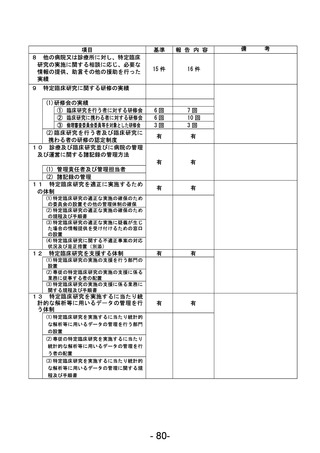
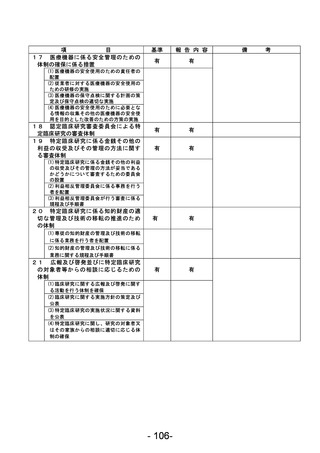
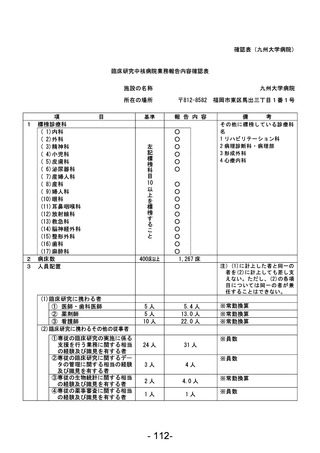
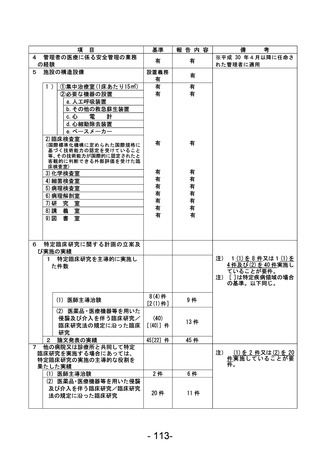
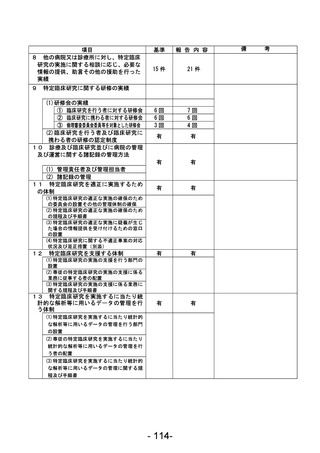
資料1 臨床研究中核病院業務報告内容確認表 (78 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62409.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第44回 8/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
不適正事案に関する対応状況:
不適合報告を京都大学臨床研究審査委員会(CRB)へ提出した。 ****に CRB での審査の結
果、不適合報告における再発防止策について妥当であると判断された。なお CRB より、今後も症
例に対する他院・他科の状況を確認し、併用禁忌薬を注意することの指示があった。 ****
に特定臨床研究等実施管理委員会へ報告された。
是正措置:
入院患者については、病棟薬剤師の協力のもと、薬剤師の持参薬・処方薬の確認とそのカルテ
記載が済んでから MRI 検査を行う順とし、被験者への問診に加えてカルテでも薬剤リストを確認
する運用に変更した。外来患者についてはミオコールスプレーを使用しない。
(注)1
2
不適正事案に関する調査の概要(方法、期間、結果等)を記載すること。
調査報告書その他関係書類が取りまとめられている場合は、添付すること。
- 77-