よむ、つかう、まなぶ。
令和6年度 医療用医薬品の販売情報提供活動調査事業報告書 (23 ページ)
出典
| 公開元URL | https://www.jshp.or.jp/content/2025/0725-1.html |
| 出典情報 | 令和6年度販売情報提供活動調査事業報告書について(7/25付 事務連絡)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
同様に、
「医療用医薬品の広告活動監視モニター事業報告書」
(三菱 UFJ リサーチ&コンサ
ルティング株式会社、平成 29 年 3 月、平成 30 年 3 月、平成 31 年 3 月)
、「
(医療用医薬品
の)販売情報提供活動監視事業報告書」
(三菱 UFJ リサーチ&コンサルティング株式会社、
令和 2 年 3 月、令和 3 年 3 月、令和 4 年 3 月、令和 5 年 3 月、令和 6 年 3 月)で適切性に
疑いがあるとして紹介された事例も、判断基準の参考とした。
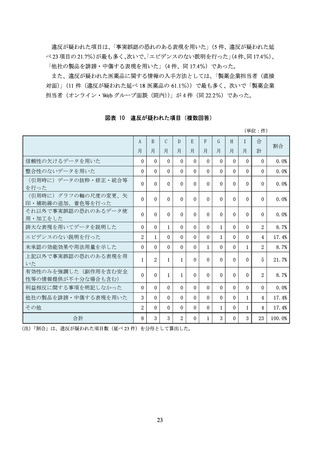
図表 8 適切性に疑いのある主な販売情報提供活動事例
(未承認の効能効果や用法用量を示した事例)
「A 社の MR が、モニター医療機関を訪問し、自社製品である高リン血症治療剤に特有
の副作用(栄養成分**が過剰になること等)を注意喚起するパンフレットを提供した。
MR はこのパンフレットをもとに、本来の効能効果であるリンの抑制効果を説明した上
で、
『この薬を使用すれば血液透析患者の**症状に対し栄養成分**の補充が可能にな
る』
、『臨床検査値の**の上昇が期待できる』といった副作用を逆手にとったプロモー
ションを行った。実際に、モニター医療機関では透析患者に対して、経口製剤や点滴に
よる特定成分**の補充療法を実施しているが、MR からはそれらの補充療法が不要に
なるという説明がなされており、処方への影響が懸念されるものだった」
「B 社の MR とのオンライン面談において、内用薬を服用してから注射剤へと切替が必
要な薬剤について、注射剤にのみ新たに適応追加が承認されたため、注射剤にしか適応
となっていない疾患の患者に対する導入方法について質問したところ、
『本剤の注射剤に
ある適応については内用薬でも適応が認められる』といった説明を受けた」
(事実誤認の恐れのあるデータ使用・加工を行った事例)
「C 社が主催する Web セミナーにおいて、医薬品の有効性を示すために、実薬対象比較
試験の結果の説明がなされた。主要評価項目である『中等度又は重度の疾患の増悪回数』
のグラフについて、スライド上で差が大きく見えるようにグラフの縦軸の一部を拡大し
て、効果を強調する場面があった。なお、製品情報概要には通常のグラフが掲載されて
おり、スライドのみが視覚的に差を強調したものとなっていた。画面が切り替わるタイ
ミングが早ければ、データを正確に読み取れない危険性があった」
(事実誤認の恐れのある表現を用いた事例)
「D 社の代謝調節剤について追加の適応が承認されたので、モニター医療機関で勉強会
が開催された。D 社の担当 MR が当該医薬品と腫瘍崩壊症候群に関する説明をする中、
1 スライドだけではあるが、既存薬との比較試験のデータを示し、
『既存薬に対し当該医
薬品は優位性を持っている』と説明した。しかし、このデータは従来の適応のものであ
って、追加された適応のものではなく、さらには追加された適応では既存薬に対する非
劣性のデータしかなかった。勉強会のテーマとは若干外れた内容のスライドをプレゼン
テーションの中で紹介されることで、誤認の恐れがあった」
19
「医療用医薬品の広告活動監視モニター事業報告書」
(三菱 UFJ リサーチ&コンサ
ルティング株式会社、平成 29 年 3 月、平成 30 年 3 月、平成 31 年 3 月)
、「
(医療用医薬品
の)販売情報提供活動監視事業報告書」
(三菱 UFJ リサーチ&コンサルティング株式会社、
令和 2 年 3 月、令和 3 年 3 月、令和 4 年 3 月、令和 5 年 3 月、令和 6 年 3 月)で適切性に
疑いがあるとして紹介された事例も、判断基準の参考とした。
図表 8 適切性に疑いのある主な販売情報提供活動事例
(未承認の効能効果や用法用量を示した事例)
「A 社の MR が、モニター医療機関を訪問し、自社製品である高リン血症治療剤に特有
の副作用(栄養成分**が過剰になること等)を注意喚起するパンフレットを提供した。
MR はこのパンフレットをもとに、本来の効能効果であるリンの抑制効果を説明した上
で、
『この薬を使用すれば血液透析患者の**症状に対し栄養成分**の補充が可能にな
る』
、『臨床検査値の**の上昇が期待できる』といった副作用を逆手にとったプロモー
ションを行った。実際に、モニター医療機関では透析患者に対して、経口製剤や点滴に
よる特定成分**の補充療法を実施しているが、MR からはそれらの補充療法が不要に
なるという説明がなされており、処方への影響が懸念されるものだった」
「B 社の MR とのオンライン面談において、内用薬を服用してから注射剤へと切替が必
要な薬剤について、注射剤にのみ新たに適応追加が承認されたため、注射剤にしか適応
となっていない疾患の患者に対する導入方法について質問したところ、
『本剤の注射剤に
ある適応については内用薬でも適応が認められる』といった説明を受けた」
(事実誤認の恐れのあるデータ使用・加工を行った事例)
「C 社が主催する Web セミナーにおいて、医薬品の有効性を示すために、実薬対象比較
試験の結果の説明がなされた。主要評価項目である『中等度又は重度の疾患の増悪回数』
のグラフについて、スライド上で差が大きく見えるようにグラフの縦軸の一部を拡大し
て、効果を強調する場面があった。なお、製品情報概要には通常のグラフが掲載されて
おり、スライドのみが視覚的に差を強調したものとなっていた。画面が切り替わるタイ
ミングが早ければ、データを正確に読み取れない危険性があった」
(事実誤認の恐れのある表現を用いた事例)
「D 社の代謝調節剤について追加の適応が承認されたので、モニター医療機関で勉強会
が開催された。D 社の担当 MR が当該医薬品と腫瘍崩壊症候群に関する説明をする中、
1 スライドだけではあるが、既存薬との比較試験のデータを示し、
『既存薬に対し当該医
薬品は優位性を持っている』と説明した。しかし、このデータは従来の適応のものであ
って、追加された適応のものではなく、さらには追加された適応では既存薬に対する非
劣性のデータしかなかった。勉強会のテーマとは若干外れた内容のスライドをプレゼン
テーションの中で紹介されることで、誤認の恐れがあった」
19