よむ、つかう、まなぶ。
08参考資料1 ヒトパピローマウイルス(HPV)ワクチンファクトシート追補版 (35 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_63875.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第31回 9/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
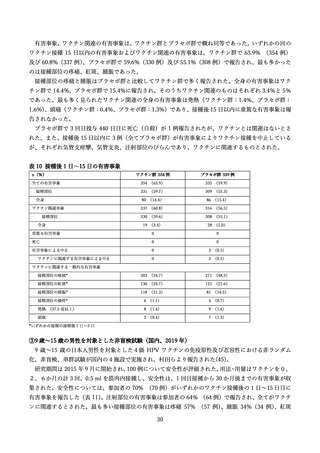
のワクチン接種時に、ワクチン接種報告カードに、接種日の夕方と接種後 4 日間の口腔内体温を記録し
た。また、各回のワクチン接種後、接種日を含む合計 15 日間、注射部位および全身性の有害事象、併用
薬、併用したワクチン接種を記録した。有害事象による接種の中止は合計 5 件とまれで、ワクチンに関
連する重篤な有害事象は存在しなかった。試験中に死亡した被験者はいなかった。少なくとも 1 つの注
射部位または全身性の有害事象を報告した参加者の割合は、女性よりも男性で少なかった。最も一般的な
(発生率 2%以上)注射部位の症状は疼痛、腫脹、紅斑およびそう痒症であり、そのほとんどは軽度から
中程度であった。若い男性(HM および MSM)で最も多かった(発生率 2%以上)ワクチン関連の全身
性の症状は、頭痛および発熱であった。いずれかの接種から 5 日以内に発熱(≧37.8℃)を起こした参加
者の割合は、HM と MSM の 2 つのコホート間で同等であった。
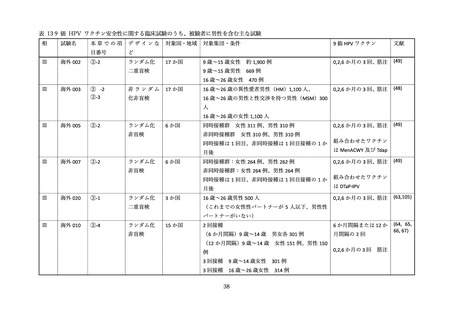
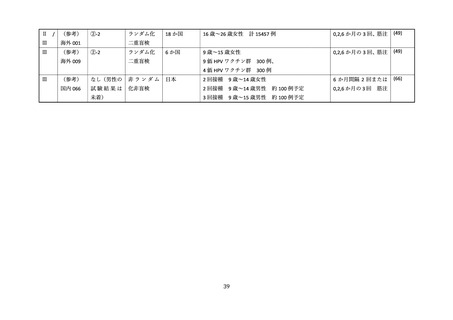
海外 010 試験において(64, 65, 66, 67)、9 価 HPV ワクチン接種の 14 日後までの注射部位及び非注射
部位の有害事象、並びに試験終了時点までの死亡、重篤な有害事象及び妊娠の転帰について情報収集され
た。9 歳~14 歳群(男女それぞれ 301 名登録、12 月間隔の 2 回接種)で接種部位副反応は 36 例(12.3%)
見られ、そのうち女性が 29 例と大半であった。接種部位の痛みが女性では 16.7%、男性では 9.5%で見
られた(65)。非注射部位症状は、同じ 9 歳~14 歳男女の 2 回接種群(12 か月間隔)で 12 例(4.1%)
にみられ、そのうち女性が 8 例であった。全体で合計 34 名の参加者が重篤な副反応を経験したが、接
種中止に至った事象は、9 歳~14 歳男女の 2 回接種群(12 か月間隔)では 2 例(内、女性 1 例)に認
められ、蕁麻疹(因果関係あり:女性)及び神経根障害(因果関係なし:男性)が各 1 例であった。試
験終了時点までに認められた重篤な副反応及び中止に至った副反応は、いずれも転帰は回復であった。
②アメリカにおける有害事象報告
ア)アメリカワクチン有害事象報告システム;VAERS からの報告(1)(68)
2014 年 12 月から 2017 年 12 月までのアメリカ VAERS から、9 価 HPV ワクチン接種後の報告につい
て検索し集計した。計 7,244 件の報告で性別の内訳は女性 31.2%、男性 21.6%であり、47.2%について
は性別報告なしであった。全体として報告の 97.4%は非重篤であった。めまい、失神、頭痛、注射部位反
応が多く報告され、それらの有害事象の頻度は女性と男性の間で同様であった。9 価 HPV ワクチン接種
後の死亡例は 2 件確認されたが、ワクチン関連ではなかった。臨床的に重要な有害事象を伴う安全性に
関する新規または予期せぬ懸念や報告は検出されなかった。9 価 HPV の安全性プロファイルは、認可前
の試験データおよび 4 価 HPV ワクチンの市販後安全性データと一致していた。
【そのほかの重要な症候群についての報告】
同報告から、以下の症候群についての情報を抽出した。いずれも報告で大半を占めるのは女性であっ
た。ただし、アメリカ VAERS からの報告は、時間経過としてのワクチン接種後の有害事象をまとめてい
るが、必ずしもワクチンと報告有害事象の因果関係を示唆するものではないことに留意が必要である。
▪
ギラン・バレー症候群;Guillain-Barre Syndrome(GBS)
GBS の報告は、女性 4 件、男性 2 件、性別が特定されない 2 件の計 8 件を確認した。8 件のうち、4
件は Brighton 基準を満たさないか、診断に十分な情報を含んでいなかった。残りの 4 件は、GBS の
Brighton 分類*におけるレベル 1(n = 1)または Brighton 分類レベル 2(n = 3)のいずれかを満た
していたが、いずれも女性での報告であった。
*GBS の Brighton 分類について(69): レベル 1>2>3 の順に診断確実性が高く、レベル 1 は以下
35
た。また、各回のワクチン接種後、接種日を含む合計 15 日間、注射部位および全身性の有害事象、併用
薬、併用したワクチン接種を記録した。有害事象による接種の中止は合計 5 件とまれで、ワクチンに関
連する重篤な有害事象は存在しなかった。試験中に死亡した被験者はいなかった。少なくとも 1 つの注
射部位または全身性の有害事象を報告した参加者の割合は、女性よりも男性で少なかった。最も一般的な
(発生率 2%以上)注射部位の症状は疼痛、腫脹、紅斑およびそう痒症であり、そのほとんどは軽度から
中程度であった。若い男性(HM および MSM)で最も多かった(発生率 2%以上)ワクチン関連の全身
性の症状は、頭痛および発熱であった。いずれかの接種から 5 日以内に発熱(≧37.8℃)を起こした参加
者の割合は、HM と MSM の 2 つのコホート間で同等であった。
海外 010 試験において(64, 65, 66, 67)、9 価 HPV ワクチン接種の 14 日後までの注射部位及び非注射
部位の有害事象、並びに試験終了時点までの死亡、重篤な有害事象及び妊娠の転帰について情報収集され
た。9 歳~14 歳群(男女それぞれ 301 名登録、12 月間隔の 2 回接種)で接種部位副反応は 36 例(12.3%)
見られ、そのうち女性が 29 例と大半であった。接種部位の痛みが女性では 16.7%、男性では 9.5%で見
られた(65)。非注射部位症状は、同じ 9 歳~14 歳男女の 2 回接種群(12 か月間隔)で 12 例(4.1%)
にみられ、そのうち女性が 8 例であった。全体で合計 34 名の参加者が重篤な副反応を経験したが、接
種中止に至った事象は、9 歳~14 歳男女の 2 回接種群(12 か月間隔)では 2 例(内、女性 1 例)に認
められ、蕁麻疹(因果関係あり:女性)及び神経根障害(因果関係なし:男性)が各 1 例であった。試
験終了時点までに認められた重篤な副反応及び中止に至った副反応は、いずれも転帰は回復であった。
②アメリカにおける有害事象報告
ア)アメリカワクチン有害事象報告システム;VAERS からの報告(1)(68)
2014 年 12 月から 2017 年 12 月までのアメリカ VAERS から、9 価 HPV ワクチン接種後の報告につい
て検索し集計した。計 7,244 件の報告で性別の内訳は女性 31.2%、男性 21.6%であり、47.2%について
は性別報告なしであった。全体として報告の 97.4%は非重篤であった。めまい、失神、頭痛、注射部位反
応が多く報告され、それらの有害事象の頻度は女性と男性の間で同様であった。9 価 HPV ワクチン接種
後の死亡例は 2 件確認されたが、ワクチン関連ではなかった。臨床的に重要な有害事象を伴う安全性に
関する新規または予期せぬ懸念や報告は検出されなかった。9 価 HPV の安全性プロファイルは、認可前
の試験データおよび 4 価 HPV ワクチンの市販後安全性データと一致していた。
【そのほかの重要な症候群についての報告】
同報告から、以下の症候群についての情報を抽出した。いずれも報告で大半を占めるのは女性であっ
た。ただし、アメリカ VAERS からの報告は、時間経過としてのワクチン接種後の有害事象をまとめてい
るが、必ずしもワクチンと報告有害事象の因果関係を示唆するものではないことに留意が必要である。
▪
ギラン・バレー症候群;Guillain-Barre Syndrome(GBS)
GBS の報告は、女性 4 件、男性 2 件、性別が特定されない 2 件の計 8 件を確認した。8 件のうち、4
件は Brighton 基準を満たさないか、診断に十分な情報を含んでいなかった。残りの 4 件は、GBS の
Brighton 分類*におけるレベル 1(n = 1)または Brighton 分類レベル 2(n = 3)のいずれかを満た
していたが、いずれも女性での報告であった。
*GBS の Brighton 分類について(69): レベル 1>2>3 の順に診断確実性が高く、レベル 1 は以下
35