よむ、つかう、まなぶ。
08参考資料1 ヒトパピローマウイルス(HPV)ワクチンファクトシート追補版 (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_63875.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第31回 9/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
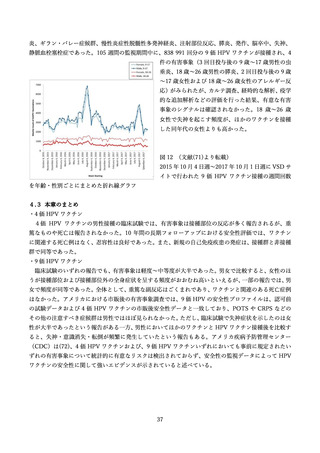
31%(31 例)であった。全身性の有害事象は 3%(3 例)で報告され、全て軽度の発熱で接種後 2 日以内
に消退した。接種部位の紅斑や腫脹の多くは 0 インチ~2 インチであり、そのほかの有害事象の多くは軽
度であった。接種後 1 日目から7か月目において、死亡、重篤な有害事象、接種中止に至った有害事象は
報告されなかった(表 12)
。また、全ての有害事象が消退し、消退までの期間は多くが2週間以内にであ
った。
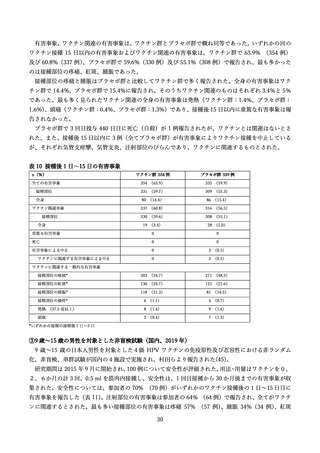
表 11 接種後1日~15 日の有害事象
有害事象
n(%)
一つ以上の非重篤な有害事象
70 (70.0)
接種部位関連の有害事象
64 (64.0)
疼痛*
57 (57.0)
腫脹
34 (34.0)
紅斑
31 (31.0)
掻痒
5 (5.0)
硬結
2 (2.0)
全身の有害事象(接種部位とは関連しない)
21 (21.0)
ウイルス性の上気道炎
9 (9.0)
発熱
6 (6.0)
頭痛
2 (2.0)
インフルエンザ
2 (2.0)
消化不良
1 (1.0)
胃腸炎
1 (1.0)
マイコプラズマ気管支炎
1 (1.0)
打撲
1 (1.0)
靭帯損傷
1 (1.0)
鼻詰まり
1 (1.0)
咽頭痛
1 (1.0)
痤瘡
1 (1.0)
ワクチン関連の有害事象**
64 (64.0)
接種部位
64 (64.0)
全身性の有害事象(接種部位とは関連しない)
3 (3.0)
発熱
3 (3.0)
重篤な有害事象
1 (1.0)
死亡
1 (1.0)
有害事象による接種中止
1 (1.0)
*
1 例で疼痛の程度が重篤とされた
**
ワクチンに関連があるかは研究者により決定された。
表 12 接種部位の有害事象(接種後1日~5日)及びワクチン関連有害事象(接種後 1 日~15 日)
有害事象
n(%)
全ての接種部位有害事象
57 (57.0)
軽度
45 (45.0)
中等度
11 (11.0)
重度
1 (1.0)
疼痛
57 (57.0)
軽度
46 (46.0)
中等度
10 (10.0)
重度
1 (1.0)
31
に消退した。接種部位の紅斑や腫脹の多くは 0 インチ~2 インチであり、そのほかの有害事象の多くは軽
度であった。接種後 1 日目から7か月目において、死亡、重篤な有害事象、接種中止に至った有害事象は
報告されなかった(表 12)
。また、全ての有害事象が消退し、消退までの期間は多くが2週間以内にであ
った。
表 11 接種後1日~15 日の有害事象
有害事象
n(%)
一つ以上の非重篤な有害事象
70 (70.0)
接種部位関連の有害事象
64 (64.0)
疼痛*
57 (57.0)
腫脹
34 (34.0)
紅斑
31 (31.0)
掻痒
5 (5.0)
硬結
2 (2.0)
全身の有害事象(接種部位とは関連しない)
21 (21.0)
ウイルス性の上気道炎
9 (9.0)
発熱
6 (6.0)
頭痛
2 (2.0)
インフルエンザ
2 (2.0)
消化不良
1 (1.0)
胃腸炎
1 (1.0)
マイコプラズマ気管支炎
1 (1.0)
打撲
1 (1.0)
靭帯損傷
1 (1.0)
鼻詰まり
1 (1.0)
咽頭痛
1 (1.0)
痤瘡
1 (1.0)
ワクチン関連の有害事象**
64 (64.0)
接種部位
64 (64.0)
全身性の有害事象(接種部位とは関連しない)
3 (3.0)
発熱
3 (3.0)
重篤な有害事象
1 (1.0)
死亡
1 (1.0)
有害事象による接種中止
1 (1.0)
*
1 例で疼痛の程度が重篤とされた
**
ワクチンに関連があるかは研究者により決定された。
表 12 接種部位の有害事象(接種後1日~5日)及びワクチン関連有害事象(接種後 1 日~15 日)
有害事象
n(%)
全ての接種部位有害事象
57 (57.0)
軽度
45 (45.0)
中等度
11 (11.0)
重度
1 (1.0)
疼痛
57 (57.0)
軽度
46 (46.0)
中等度
10 (10.0)
重度
1 (1.0)
31