よむ、つかう、まなぶ。
総-11参考2 (43 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_72294.html |
| 出典情報 | 中央社会保険医療協議会 総会(第649回 4/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
品目概要
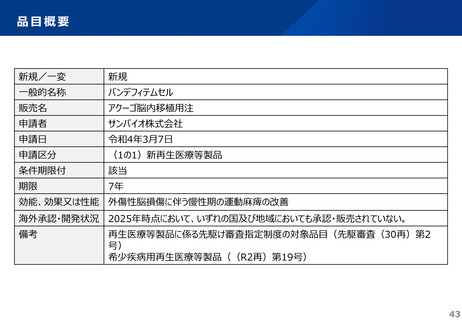
新規/一変
新規
一般的名称
バンデフィテムセル
販売名
アクーゴ脳内移植用注
申請者
サンバイオ株式会社
申請日
令和4年3月7日
申請区分
(1の1)新再生医療等製品
条件期限付
該当
期限
7年
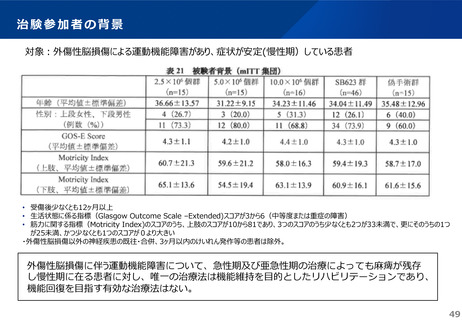
効能、効果又は性能 外傷性脳損傷に伴う慢性期の運動麻痺の改善
海外承認・開発状況 2025年時点において、いずれの国及び地域においても承認・販売されていない。
備考
再生医療等製品に係る先駆け審査指定制度の対象品目(先駆審査(30再)第2
号)
希少疾病用再生医療等製品((R2再)第19号)
43
新規/一変
新規
一般的名称
バンデフィテムセル
販売名
アクーゴ脳内移植用注
申請者
サンバイオ株式会社
申請日
令和4年3月7日
申請区分
(1の1)新再生医療等製品
条件期限付
該当
期限
7年
効能、効果又は性能 外傷性脳損傷に伴う慢性期の運動麻痺の改善
海外承認・開発状況 2025年時点において、いずれの国及び地域においても承認・販売されていない。
備考
再生医療等製品に係る先駆け審査指定制度の対象品目(先駆審査(30再)第2
号)
希少疾病用再生医療等製品((R2再)第19号)
43