よむ、つかう、まなぶ。
総-11参考2 (25 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_72294.html |
| 出典情報 | 中央社会保険医療協議会 総会(第649回 4/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
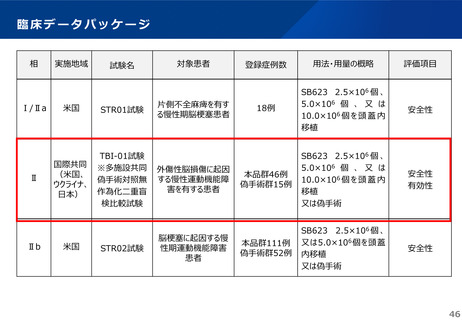
臨床データパッケージ(医師主導治験として実施)
相
試験名
(jRCT番号)
対象患者
用法・用量の概略
観察期間
評価項目
【4~7例目】 →高用量群
本品移植後
安全性
両側の被殻内に8.4×106~10.8×106個移植
24カ月間
有効性
移植症例数
<本品>
【1例目】→安全性のみを確認
片側の被殻に2.4×106 個移植後安全を確認して、
反対側に同量を移植。
IACT16049-01試
【2~3例目】→低用量群
両 側 の 被 殻 内 に 4.8×106 個 移 植 ( 片 側
験
2.4×106個ずつ)
(jRCT20902203
Ⅰ/Ⅱ
84)
※非盲検非対照、単
施設
PD患者
7例
(片側4.2~5.4×106個ずつ)
<タクロリムス>
本品移植日から52週間、経口投与する。0.03~
0.15 mg/kg(標準用量として0.06 mg/kg)
を1日2回投与で開始し、目標血中濃度はトラフ値
で5~10 ng/mLの範囲で調整する。その後12週
かけて漸減する。
偽手術の侵襲性による倫理的な問題、有効性評価時に治療薬を休薬して評価することによる患者負担の大きさ等
のため、対照群の設定は困難。
25
相
試験名
(jRCT番号)
対象患者
用法・用量の概略
観察期間
評価項目
【4~7例目】 →高用量群
本品移植後
安全性
両側の被殻内に8.4×106~10.8×106個移植
24カ月間
有効性
移植症例数
<本品>
【1例目】→安全性のみを確認
片側の被殻に2.4×106 個移植後安全を確認して、
反対側に同量を移植。
IACT16049-01試
【2~3例目】→低用量群
両 側 の 被 殻 内 に 4.8×106 個 移 植 ( 片 側
験
2.4×106個ずつ)
(jRCT20902203
Ⅰ/Ⅱ
84)
※非盲検非対照、単
施設
PD患者
7例
(片側4.2~5.4×106個ずつ)
<タクロリムス>
本品移植日から52週間、経口投与する。0.03~
0.15 mg/kg(標準用量として0.06 mg/kg)
を1日2回投与で開始し、目標血中濃度はトラフ値
で5~10 ng/mLの範囲で調整する。その後12週
かけて漸減する。
偽手術の侵襲性による倫理的な問題、有効性評価時に治療薬を休薬して評価することによる患者負担の大きさ等
のため、対照群の設定は困難。
25