よむ、つかう、まなぶ。
総-11参考2 (36 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_72294.html |
| 出典情報 | 中央社会保険医療協議会 総会(第649回 4/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
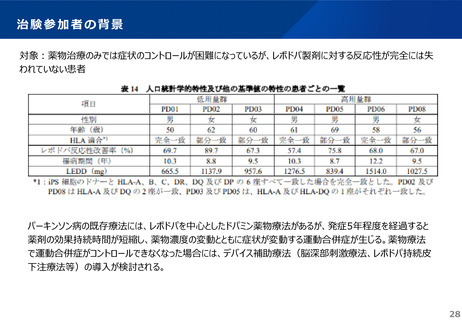
安全性評価について①
本品は、他家由来のiPS細胞由来であり、 ① iPS細胞の高い増殖能と分化能による、移植細胞ががん化するリスク
② 他家細胞を移植することによる免疫拒絶が懸念された。
① がん化リスクについて:
製造過程の各段階で腫瘍化にかかるゲノム変異が起きていないこと、未分化細胞が混入していないことを確認
このように製造された本品を用いた免疫不全マウスの造腫瘍性試験※において、腫瘍形成が認められなかった。
※免疫不全マウスに移植後26~52週後に全身の臓器を対象とした病理組織学的検査等を実施
• 臨床試験においても、悪性腫瘍に該当する有害事象は認められず、PET検査で移植片の腫瘍化が認められてないことを確認した。
•
•
対応
•
•
製品においてがん化の原因となる未分化iPS細胞の混入率を極めて低い割合(%)とすることを規定(出荷の要件)
定期的なMRI等による観察の実施、変化や症状への適切な処置を注意喚起
<MRI検査の頻度について>
・治験では、移植翌日、移植後4 週、12 週、6ヵ月、12ヵ月、 16ヵ月、 18ヵ月、24ヵ月。
・製造販売後臨床試験では移植翌日、移植後12週、6ヵ月、12ヵ月、16ヵ月、18ヵ月、24ヵ月。
⇒治験時の移植後12ヵ月、24ヵ月のMRIでは移植細胞の生着を確認。製造販売後臨床試験では、マウスでは本細胞の原料とは異
なる未分化iPS細胞を移植後、16週までに腫瘤体積増加が認められていることから、最初のMRIをこれより短い12週で設定。
・適正使用ガイドにおいて、製造販売後臨床試験の実施時期を紹介しつつ、定期的な確認を規定。
•
移植部位にがんが発生した場合の対応方法
・治験では移植手術後、頭部MRIの評価にて、移植片が増大し3cm3を超えた場合には、Xナイフによる定位放射線治療を行うことを
規定。当該情報を製販後は医療従事者向け資材で使用者に情報共有。
⇒iPS由来で生じうる腫瘍については、特異性は認められず一般的な脳腫瘍と同様の対応が可能と想定されるため、日本脳神経外科
学会のガイドラインを参照して対応を規定。
36
本品は、他家由来のiPS細胞由来であり、 ① iPS細胞の高い増殖能と分化能による、移植細胞ががん化するリスク
② 他家細胞を移植することによる免疫拒絶が懸念された。
① がん化リスクについて:
製造過程の各段階で腫瘍化にかかるゲノム変異が起きていないこと、未分化細胞が混入していないことを確認
このように製造された本品を用いた免疫不全マウスの造腫瘍性試験※において、腫瘍形成が認められなかった。
※免疫不全マウスに移植後26~52週後に全身の臓器を対象とした病理組織学的検査等を実施
• 臨床試験においても、悪性腫瘍に該当する有害事象は認められず、PET検査で移植片の腫瘍化が認められてないことを確認した。
•
•
対応
•
•
製品においてがん化の原因となる未分化iPS細胞の混入率を極めて低い割合(%)とすることを規定(出荷の要件)
定期的なMRI等による観察の実施、変化や症状への適切な処置を注意喚起
<MRI検査の頻度について>
・治験では、移植翌日、移植後4 週、12 週、6ヵ月、12ヵ月、 16ヵ月、 18ヵ月、24ヵ月。
・製造販売後臨床試験では移植翌日、移植後12週、6ヵ月、12ヵ月、16ヵ月、18ヵ月、24ヵ月。
⇒治験時の移植後12ヵ月、24ヵ月のMRIでは移植細胞の生着を確認。製造販売後臨床試験では、マウスでは本細胞の原料とは異
なる未分化iPS細胞を移植後、16週までに腫瘤体積増加が認められていることから、最初のMRIをこれより短い12週で設定。
・適正使用ガイドにおいて、製造販売後臨床試験の実施時期を紹介しつつ、定期的な確認を規定。
•
移植部位にがんが発生した場合の対応方法
・治験では移植手術後、頭部MRIの評価にて、移植片が増大し3cm3を超えた場合には、Xナイフによる定位放射線治療を行うことを
規定。当該情報を製販後は医療従事者向け資材で使用者に情報共有。
⇒iPS由来で生じうる腫瘍については、特異性は認められず一般的な脳腫瘍と同様の対応が可能と想定されるため、日本脳神経外科
学会のガイドラインを参照して対応を規定。
36