よむ、つかう、まなぶ。
総-11参考2 (38 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_72294.html |
| 出典情報 | 中央社会保険医療協議会 総会(第649回 4/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
製造販売後の検討事項について(製造販売後臨床試験)
主要目的:主コホートにおいて、65歳以下の対象患者に本品を被殻内に移植したときの有効性を検証する。
目的
副次的目的:副コホートにおいて、対象患者のうち、65歳超の高齢のPD患者に本品を被殻内に移植したときの有効
性を評価する。主コホート及び副コホートにおいて、対象患者に本品を被殻内に移植したときの安全性を評価する。
試験デザイン
非盲検非対照多施設共同
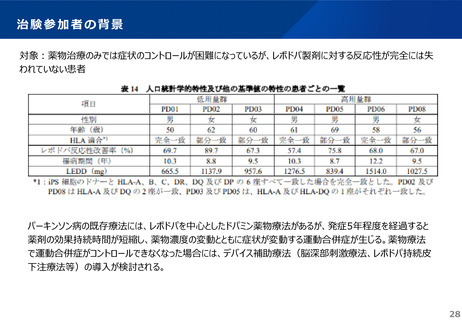
対象患者
レボドパ含有製剤を含む既存の薬物療法で十分な効果が得られないPD患者
観察期間
本品移植後96週間(別途、ベースライン検査期間として4週間)
目標症例数
[主コホート]:65歳以下の患者30例 [副コホート]:65歳超の患者5例
試験実施施設数
6~10施設(治験実施施設を含め条件に合致する施設に対して、今後本品や製造販売後臨床試験について説明予定)
主要評価項目
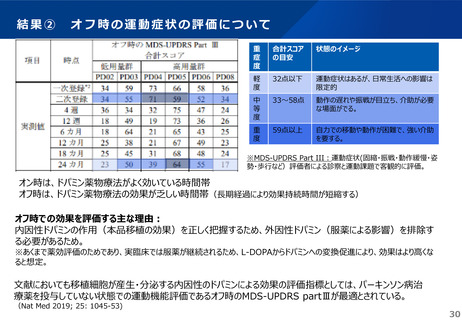
本品移植後96週時のオフ時のMDS-UPDRS Part Ⅲ合計スコアのベースラインからの変化量
(オフ時:practically defined offの状態。)
副次評価項目
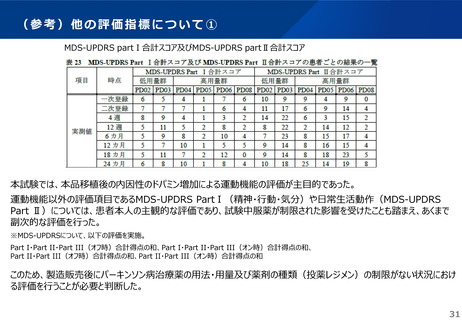
MDS-UPDRSの各指標(オフ時。Part Ⅲはオン時及びオフ時)、オン時間及びオフ時間、PDQ-39※Summary
Indexスコア及びドメイン別スコアのベースラインからの変化量等
※PD患者が自身でQOLを評価するために開発された疾患特異的評価尺度
本品は患者毎にiPSの分化誘導段階から製造を始めるため供給に限界があるが、7年間で35例程度の使用を想定している
ことから、患者の組入れは問題なく行われる。条件期限付き承認期間中に製造販売後臨床試験の目標症例数を超えた場
合には、全例を使用成績調査に組み入れ観察を行う(90~130例を想定)。
38
主要目的:主コホートにおいて、65歳以下の対象患者に本品を被殻内に移植したときの有効性を検証する。
目的
副次的目的:副コホートにおいて、対象患者のうち、65歳超の高齢のPD患者に本品を被殻内に移植したときの有効
性を評価する。主コホート及び副コホートにおいて、対象患者に本品を被殻内に移植したときの安全性を評価する。
試験デザイン
非盲検非対照多施設共同
対象患者
レボドパ含有製剤を含む既存の薬物療法で十分な効果が得られないPD患者
観察期間
本品移植後96週間(別途、ベースライン検査期間として4週間)
目標症例数
[主コホート]:65歳以下の患者30例 [副コホート]:65歳超の患者5例
試験実施施設数
6~10施設(治験実施施設を含め条件に合致する施設に対して、今後本品や製造販売後臨床試験について説明予定)
主要評価項目
本品移植後96週時のオフ時のMDS-UPDRS Part Ⅲ合計スコアのベースラインからの変化量
(オフ時:practically defined offの状態。)
副次評価項目
MDS-UPDRSの各指標(オフ時。Part Ⅲはオン時及びオフ時)、オン時間及びオフ時間、PDQ-39※Summary
Indexスコア及びドメイン別スコアのベースラインからの変化量等
※PD患者が自身でQOLを評価するために開発された疾患特異的評価尺度
本品は患者毎にiPSの分化誘導段階から製造を始めるため供給に限界があるが、7年間で35例程度の使用を想定している
ことから、患者の組入れは問題なく行われる。条件期限付き承認期間中に製造販売後臨床試験の目標症例数を超えた場
合には、全例を使用成績調査に組み入れ観察を行う(90~130例を想定)。
38