よむ、つかう、まなぶ。
05資料2-1森野委員提出資料(RSウイルス母子免疫ワクチンと抗体製剤ファクトシート) (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64997.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第32回 10/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
の原因は不明であるが、タンパク質喪失を生じうる基礎疾患の併発が影響した可能性が示唆された。ニル
セビマブ投与後の幾何平均抗体上昇率は、モノクローナル抗体製剤として先行して使用されていたパリ
ビズマブと比較し、初回および 2 回目の RSV 感染症流行期において高いことが示された。
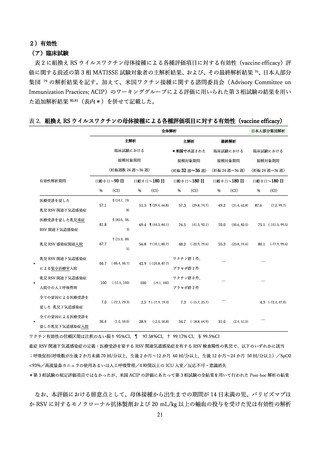
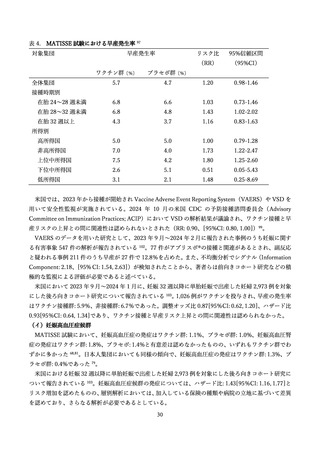
早産児での RSV 関連下気道感染症の発症率はニルセビマブ群 2.6%、プラセボ群 9.5%と、ニルセビマ
ブ群で 70%の減少が認められ、入院の発生率はニルセビマブ群 0.8%、プラセボ群 4.1%と、ニルセビマ
ブ群で 78%の減少が認められた。正期産児の 150 日目までの RSV による下気道感染に対する有効性は、
74.5%、RSV による入院に対する有効性は、62.1%であった。在胎週数 29 週以上の乳児において 180 日
目までの RSV による入院に対する有効性は 82.7%、重症な入院に対する有効性は 75.3%であった。
ニルセビマブの効果は標的となる F タンパク質の保存性が重要である。in vitro での研究においてニル
セビマブ存在下での耐性変異株出現が確認され、臨床試験参加者からの分離株の配列解析においても耐
性変異株が確認されているが、大部分の変異はニルセビマブへの感受性があり、逃避株は現在のところ極
めてまれとされている。変異株に対するサーベイランスが重要である。
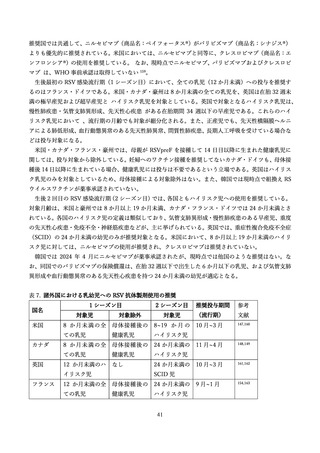
リアルワールドデータでは、スペインの研究において、RSV 関連下気道感染症による入院に対するニ
ルセビマブ投与の有効性は 80.2%であった。フランスの研究では RSV 関連下気道感染症による入院に対
するニルセビマブ投与の有効性は 83.0%であった。
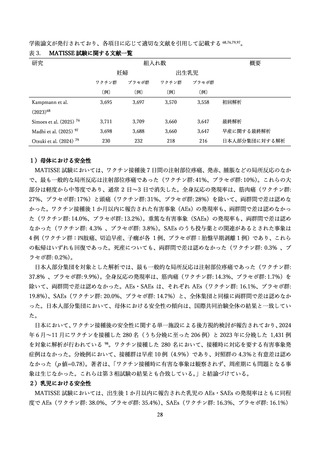
母子免疫ワクチンの安全性
妊婦を対象とした RSV 母子免疫ワクチン(アブリスボ®)の安全性については、主に国際共同多施設無
作為化二重盲検試験において評価されている。最も多くみられた副反応は注射部位の痛みなどの局所反
応で、その大部分は軽度から中等度であり、通常 2 日~3 日で自然に消失した。筋肉痛や頭痛などの全身
性の副反応や、母子における重篤な有害事象の発生率は、ワクチン群とプラセボ群で有意差は認めなかっ
た。早産・妊娠高血圧症候群については、統計的な有意差はないものの、ワクチン群でわずかに高い傾向
であった。いずれも、現時点でワクチンと関連があるとされていないが、市販後調査などを通じて、積極
的な安全性の監視が継続して実施されている。
抗体製剤の安全性
ニルセビマブの局所の副反応としては発赤や紫斑がみられ、全身の副反応としてはアナフィラキシー
を含む過敏反応、免疫複合体疾患、血小板減少、倦怠感、発熱、胃腸症状が起こりうるが、一般的に安全
で忍容性の高い製剤である。市販後調査およびリアルワールドデータでも、入院加療を必要とする重篤な
副反応は報告されていない。母体への RSV ワクチンとの併用や複数回投与に対する安全性の報告は現時
点ではない。
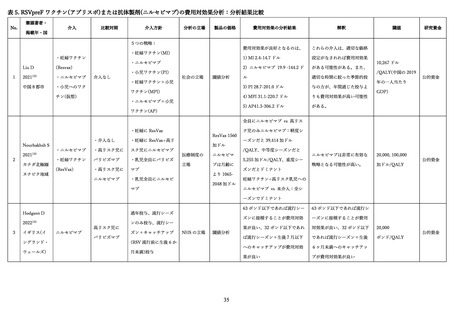
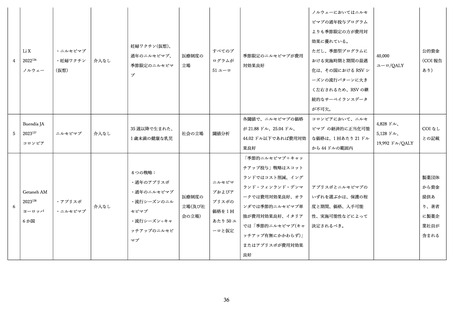
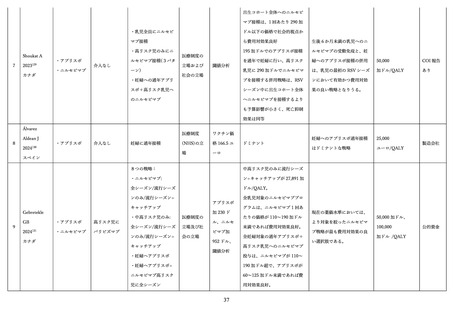
医療経済学的な観点
妊婦に対する RSVpreF ワクチン(アブリスボ)または乳児に対する抗体製剤(ニルセビマブ)を対象
とし、質調整生存年(QALY)を効果指標として費用対効果を検討した研究 18 件をレビューした。これ
らの研究には、価格を事前に定めずに費用対効果が良好となる価格の閾値を分析した研究が多く含まれ
ていた。また、価格を仮定して実施された費用効果分析においても、各製品の価格設定や有効性に関する
前提条件の置き方によって結果が大きく変化しており、統一的な結論を導くことは困難であった。今後は
6
セビマブ投与後の幾何平均抗体上昇率は、モノクローナル抗体製剤として先行して使用されていたパリ
ビズマブと比較し、初回および 2 回目の RSV 感染症流行期において高いことが示された。
早産児での RSV 関連下気道感染症の発症率はニルセビマブ群 2.6%、プラセボ群 9.5%と、ニルセビマ
ブ群で 70%の減少が認められ、入院の発生率はニルセビマブ群 0.8%、プラセボ群 4.1%と、ニルセビマ
ブ群で 78%の減少が認められた。正期産児の 150 日目までの RSV による下気道感染に対する有効性は、
74.5%、RSV による入院に対する有効性は、62.1%であった。在胎週数 29 週以上の乳児において 180 日
目までの RSV による入院に対する有効性は 82.7%、重症な入院に対する有効性は 75.3%であった。
ニルセビマブの効果は標的となる F タンパク質の保存性が重要である。in vitro での研究においてニル
セビマブ存在下での耐性変異株出現が確認され、臨床試験参加者からの分離株の配列解析においても耐
性変異株が確認されているが、大部分の変異はニルセビマブへの感受性があり、逃避株は現在のところ極
めてまれとされている。変異株に対するサーベイランスが重要である。
リアルワールドデータでは、スペインの研究において、RSV 関連下気道感染症による入院に対するニ
ルセビマブ投与の有効性は 80.2%であった。フランスの研究では RSV 関連下気道感染症による入院に対
するニルセビマブ投与の有効性は 83.0%であった。
母子免疫ワクチンの安全性
妊婦を対象とした RSV 母子免疫ワクチン(アブリスボ®)の安全性については、主に国際共同多施設無
作為化二重盲検試験において評価されている。最も多くみられた副反応は注射部位の痛みなどの局所反
応で、その大部分は軽度から中等度であり、通常 2 日~3 日で自然に消失した。筋肉痛や頭痛などの全身
性の副反応や、母子における重篤な有害事象の発生率は、ワクチン群とプラセボ群で有意差は認めなかっ
た。早産・妊娠高血圧症候群については、統計的な有意差はないものの、ワクチン群でわずかに高い傾向
であった。いずれも、現時点でワクチンと関連があるとされていないが、市販後調査などを通じて、積極
的な安全性の監視が継続して実施されている。
抗体製剤の安全性
ニルセビマブの局所の副反応としては発赤や紫斑がみられ、全身の副反応としてはアナフィラキシー
を含む過敏反応、免疫複合体疾患、血小板減少、倦怠感、発熱、胃腸症状が起こりうるが、一般的に安全
で忍容性の高い製剤である。市販後調査およびリアルワールドデータでも、入院加療を必要とする重篤な
副反応は報告されていない。母体への RSV ワクチンとの併用や複数回投与に対する安全性の報告は現時
点ではない。
医療経済学的な観点
妊婦に対する RSVpreF ワクチン(アブリスボ)または乳児に対する抗体製剤(ニルセビマブ)を対象
とし、質調整生存年(QALY)を効果指標として費用対効果を検討した研究 18 件をレビューした。これ
らの研究には、価格を事前に定めずに費用対効果が良好となる価格の閾値を分析した研究が多く含まれ
ていた。また、価格を仮定して実施された費用効果分析においても、各製品の価格設定や有効性に関する
前提条件の置き方によって結果が大きく変化しており、統一的な結論を導くことは困難であった。今後は
6