よむ、つかう、まなぶ。
参考資料 持続可能な社会保障制度の構築(財政各論Ⅱ)(参考資料) (44 ページ)
出典
| 公開元URL | https://www.mof.go.jp/about_mof/councils/fiscal_system_council/sub-of_fiscal_system/proceedings/material/20250423zaiseia.html |
| 出典情報 | 財政制度等審議会 財政制度分科会(4/23)《財務省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
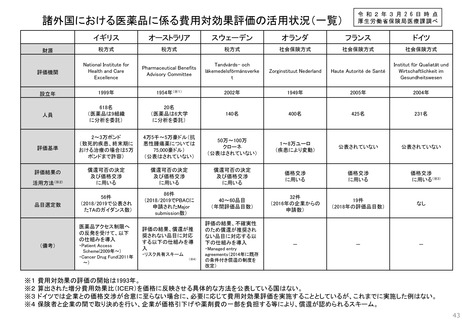
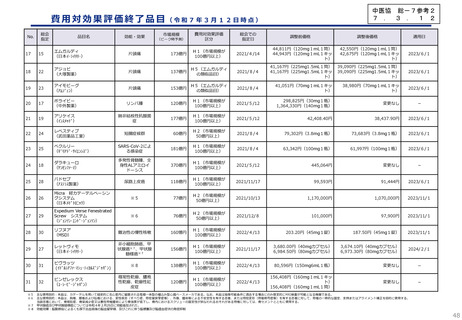
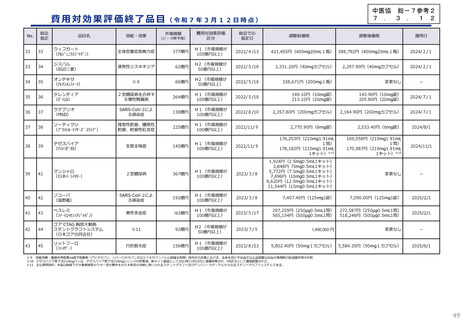
諸外国における医薬品に係る費用対効果評価の活用状況(一覧)
令 和 2 年 3 月 2 6 日 時 点
厚生労働省保険局医療課調べ
イギリス
オーストラリア
スウェーデン
オランダ
フランス
ドイツ
財源
税方式
税方式
税方式
社会保険方式
社会保険方式
社会保険方式
評価機関
National Institute for
Health and Care
Excellence
Pharmaceutical Benefits
Advisory Committee
Tandvårds- och
läkemedelsförmånsverke
t
Zorginstituut Nederland
Haute Autorité de Santé
Institut für Qualiatät und
Wirtschaftlichkeit im
Gesundheitswesen
設立年
1999年
1954年(※1)
2002年
1949年
2005年
2004年
人員
618名
(医薬品は9組織
に分析を委託)
20名
(医薬品は6大学
に分析を委託)
140名
400名
425名
231名
評価基準
2~3万ポンド
(致死的疾患、終末期に
おける治療の場合は5万
ポンドまで許容)
4万5千~5万豪ドル(抗
悪性腫瘍薬については
75,000豪ドル)
(公表はされていない)
50万~100万
クローネ
(公表はされていない)
1~8万ユーロ
(疾患により変動)
公表されていない
公表されていない
償還可否の決定
及び価格交渉
に用いる
償還可否の決定
及び価格交渉
に用いる
償還可否の決定
及び価格交渉
に用いる
価格交渉
に用いる
価格交渉
に用いる
56件
(2018/2019で公表され
たTAのガイダンス数)
86件
(2018/2019でPBACに
申請されたMajor
submission数)
40~60品目
(年間評価品目数)
32件
(2016年の企業からの
申請数)
19件
(2018年の評価品目数)
なし
-
-
-
評価結果の
活用方法(※2)
品目選定数
医薬品アクセス制限へ
の反発を受けて、以下
の仕組みを導入
(備考)
・Patient Access
Scheme(2009年~)
・Cancer Drug Fund(2011年
~)
評価の結果、償還が推
奨されない品目に対応
する以下の仕組みを導
入
・リスク共有スキーム
(※4)
評価の結果、不確実性
のため償還が推奨され
ない品目に対応する以
下の仕組みを導入
・Managed entry
agreements(2014年に既存
の条件付き償還の制度を
改定)
価格交渉
に用いる(※3)
※1 費用対効果の評価の開始は1993年。
※2 算出された増分費用効果比(ICER)を価格に反映させる具体的な方法を公表している国はない。
※3 ドイツでは企業との価格交渉が合意に至らない場合に、必要に応じて費用対効果評価を実施することとしているが、これまでに実施した例はない。
※4 保険者と企業の間で取り決めを行い、企業が価格引下げや薬剤費の一部を負担する等により、償還が認められるスキーム。
43
令 和 2 年 3 月 2 6 日 時 点
厚生労働省保険局医療課調べ
イギリス
オーストラリア
スウェーデン
オランダ
フランス
ドイツ
財源
税方式
税方式
税方式
社会保険方式
社会保険方式
社会保険方式
評価機関
National Institute for
Health and Care
Excellence
Pharmaceutical Benefits
Advisory Committee
Tandvårds- och
läkemedelsförmånsverke
t
Zorginstituut Nederland
Haute Autorité de Santé
Institut für Qualiatät und
Wirtschaftlichkeit im
Gesundheitswesen
設立年
1999年
1954年(※1)
2002年
1949年
2005年
2004年
人員
618名
(医薬品は9組織
に分析を委託)
20名
(医薬品は6大学
に分析を委託)
140名
400名
425名
231名
評価基準
2~3万ポンド
(致死的疾患、終末期に
おける治療の場合は5万
ポンドまで許容)
4万5千~5万豪ドル(抗
悪性腫瘍薬については
75,000豪ドル)
(公表はされていない)
50万~100万
クローネ
(公表はされていない)
1~8万ユーロ
(疾患により変動)
公表されていない
公表されていない
償還可否の決定
及び価格交渉
に用いる
償還可否の決定
及び価格交渉
に用いる
償還可否の決定
及び価格交渉
に用いる
価格交渉
に用いる
価格交渉
に用いる
56件
(2018/2019で公表され
たTAのガイダンス数)
86件
(2018/2019でPBACに
申請されたMajor
submission数)
40~60品目
(年間評価品目数)
32件
(2016年の企業からの
申請数)
19件
(2018年の評価品目数)
なし
-
-
-
評価結果の
活用方法(※2)
品目選定数
医薬品アクセス制限へ
の反発を受けて、以下
の仕組みを導入
(備考)
・Patient Access
Scheme(2009年~)
・Cancer Drug Fund(2011年
~)
評価の結果、償還が推
奨されない品目に対応
する以下の仕組みを導
入
・リスク共有スキーム
(※4)
評価の結果、不確実性
のため償還が推奨され
ない品目に対応する以
下の仕組みを導入
・Managed entry
agreements(2014年に既存
の条件付き償還の制度を
改定)
価格交渉
に用いる(※3)
※1 費用対効果の評価の開始は1993年。
※2 算出された増分費用効果比(ICER)を価格に反映させる具体的な方法を公表している国はない。
※3 ドイツでは企業との価格交渉が合意に至らない場合に、必要に応じて費用対効果評価を実施することとしているが、これまでに実施した例はない。
※4 保険者と企業の間で取り決めを行い、企業が価格引下げや薬剤費の一部を負担する等により、償還が認められるスキーム。
43