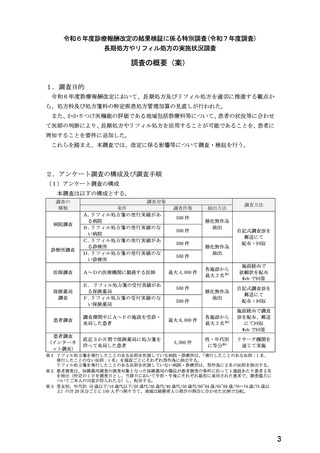
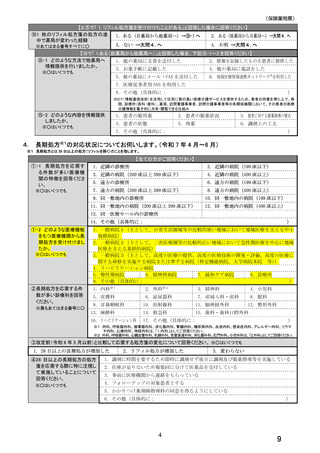
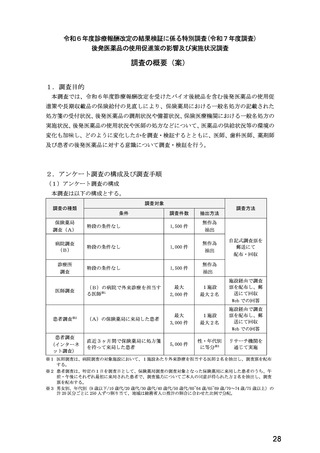
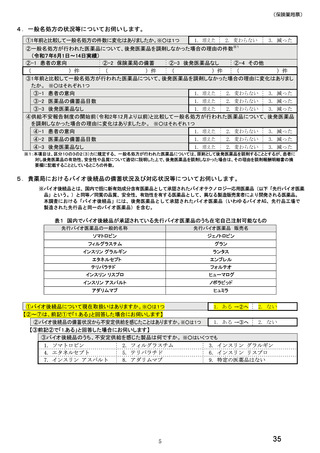
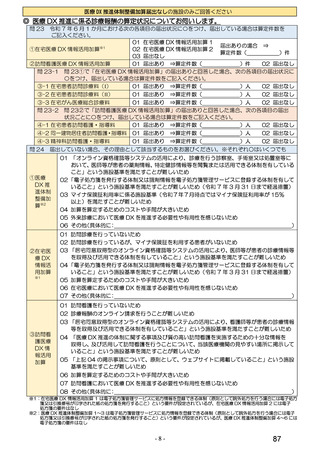
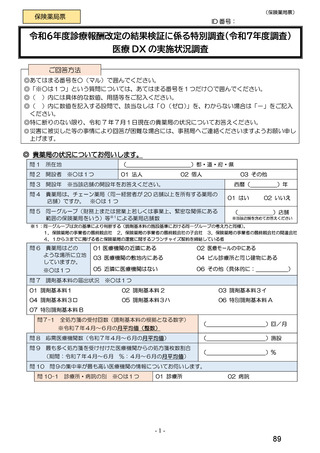
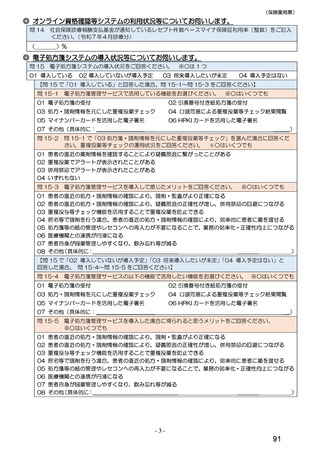
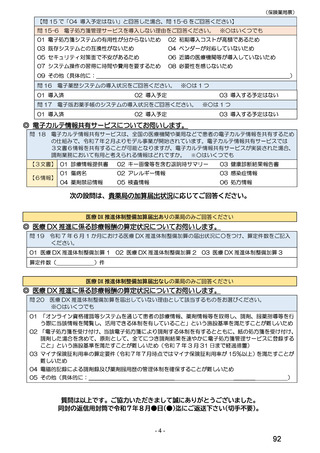
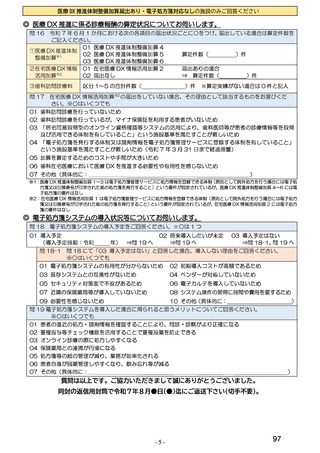
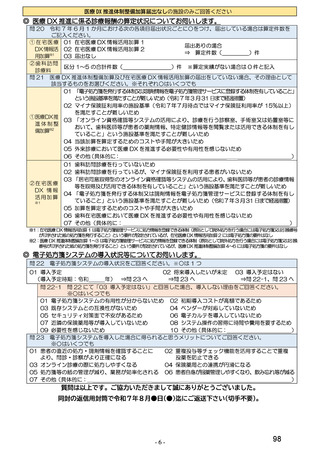
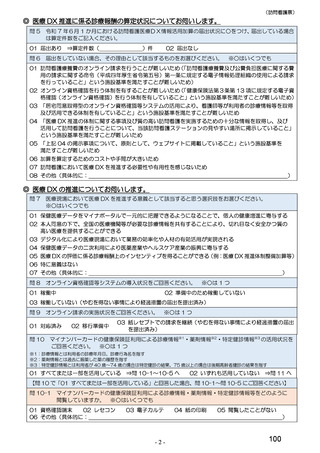
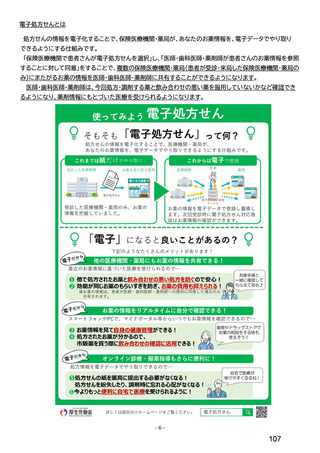
総-4令和6年度診療報酬改定の結果検証に係る特別調査(令和7年度調査)の調査票案について (55 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59377.html |
| 出典情報 | 中央社会保険医療協議会 総会(第611回 7/9)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
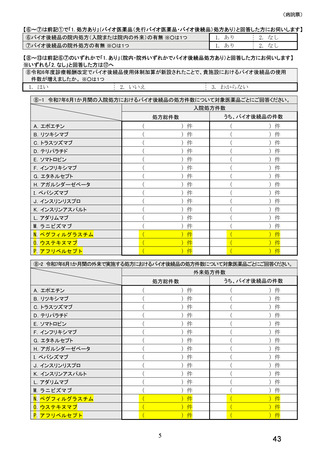
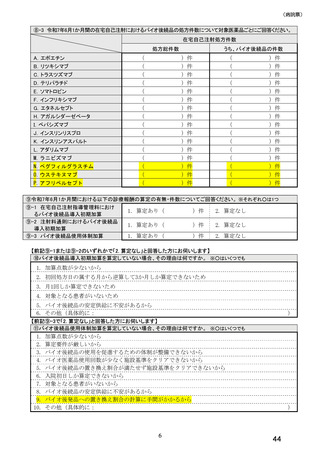
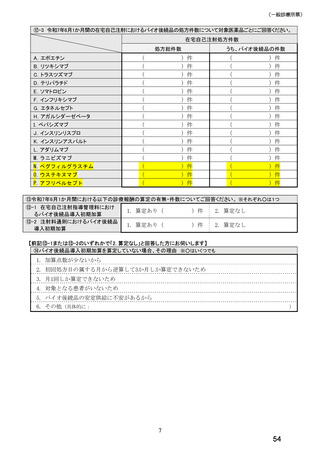
⑮バイオ後続品の採用が進んでいない医薬品についてご回答ください。 ※○はいくつでも
1. インスリン製剤
2. ヒト成長ホルモン剤
3. エタネルセプト製剤
4. テリパラチド製剤
5. リツキシマブ製剤
6. トラスツズマブ製剤
7. ベバシズマブ製剤
8. インフリキシマブ製剤
9. アダリムマブ製剤
10. ラニビズマブ製剤
11. アガルシダーゼ ベータ製剤
12. ペグフィルグラスチム製剤
13. ウステキヌマブ製剤 14. アフリベルセプト製剤
15. バイオ後続品の採用状況の差は、医薬品ごとにあまりない
→バイオ後続品の院外処方ありの場合、⑱へ
→バイオ後続品の院外処方なしの場合、㉑へ
16. バイオ後続品を採用していない →㉑へ
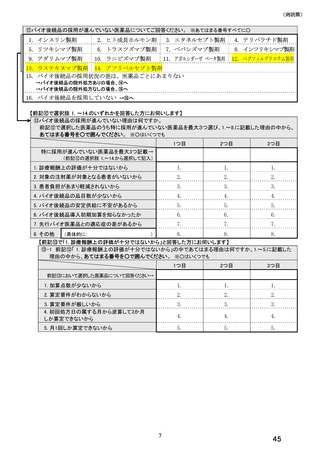
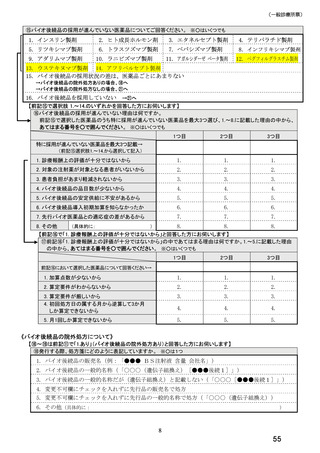
【前記⑮で選択肢 1.~14.のいずれかを回答した方にお伺いします】
⑯バイオ後続品の採用が進んでいない理由は何ですか。
前記⑮で選択した医薬品のうち特に採用が進んでいない医薬品を最大3つ選び、1.~8.に記載した理由の中から、
あてはまる番号を○で囲んでください。 ※○はいくつでも
1つ目
2つ目
3つ目
1. 診療報酬上の評価が十分ではないから
1.
1.
1.
2. 対象の注射薬が対象となる患者がいないから
2.
2.
2.
3. 患者負担があまり軽減されないから
3.
3.
3.
4. バイオ後続品の品目数が少ないから
4.
4.
4.
5. バイオ後続品の安定供給に不安があるから
5.
5.
5.
6. バイオ後続品導入初期加算を知らなかったか
6.
6.
6.
7. 先行バイオ医薬品との適応症の差があるから
7.
7.
7.
8.
8.
8.
特に採用が進んでいない医薬品を最大3つ記載→
(前記⑮選択肢1.~14.から選択して記入)
8. その他
(具体的に:
)
【前記⑯で「1. 診療報酬上の評価が十分ではないから」と回答した方にお伺いします】
⑰前記⑯「1. 診療報酬上の評価が十分ではないから」の中であてはまる理由は何ですか。1.~5.に記載した理由
の中から、あてはまる番号を○で囲んでください。 ※○はいくつでも
1つ目
2つ目
3つ目
1. 加算点数が少ないから
1.
1.
1.
2. 算定要件がわからないから
2.
2.
2.
3. 算定要件が厳しいから
4. 初回処方日の属する月から逆算して3か月
しか算定できないから
3.
3.
3.
4.
4.
4.
5. 月1回しか算定できないから
5.
5.
5.
前記⑯において選択した医薬品について回答ください→
《バイオ後続品の院外処方について》
【⑱~⑲は前記⑪で「1.あり」(バイオ後続品の院外処方あり)と回答した方にお伺いします】
⑱発行する際、処方箋にどのように表記していますか。 ※○は1つ
1. バイオ後続品の販売名(例:「●●● BS注射液 含量 会社名」)
2. バイオ後続品の一般的名称(「○○○(遺伝子組換え)[●●●後続1]」)
3. バイオ後続品の一般的名称だが(遺伝子組換え)と記載しない(「○○○[●●●後続1]」)
4. 変更不可欄にチェックを入れずに先行品の販売名で処方
5. 変更不可欄にチェックを入れずに先行品の一般的名称で処方(「○○○(遺伝子組換え))
6. その他(具体的に:
)
8
55