よむ、つかう、まなぶ。
参考資料3 有効性評価に基づく大腸がん検診ガイドライン2024年度版 (41 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71872.html |
| 出典情報 | がん検診のあり方に関する検討会(第46回 3/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
補足説明:代替指標評価の概念
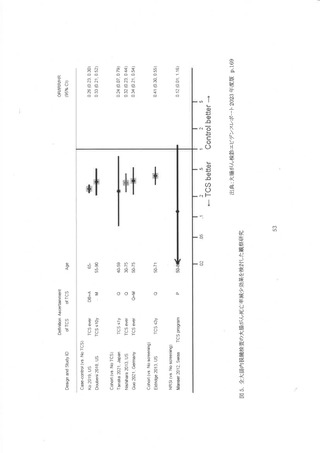
2019 年 7 月文献レビューが開始された時点では全大腸内視鏡の有効性を評価した RCT の報
告がなく、 本ガイドライン作成中の 2022 年 10 月に北欧諸国の NordICC 研究から中間解析が公
表されているのみである 39。 その他の ROT からも死亡率減少効果に関する報告がないため、本
ガイドラインでは観祭研究による評価に追加して WEO の代奉指標評価を行い、全大腸内視鏡の
有効性を評価した。 この議論の中で、 WEO の代次指標評価ではなく、 感度・特異度で判断する方
法や8 状結腸鏡の RCT の結果を外挿して判断する方法も提案された。
がん検診に新しい検査技術(以後、新技術)を採用する場合、RCT による有効性評価が長く用
いられてきた。 しかし、RCT は確実な科学的根拠が得られる一方、多くの費用や時間を要する。 そ
こで、中間アウトカムによる新技術の有効性を評価することが長年期待され、 議論さんてきた。 ここ
では、 中間アウトカムによる新技術の有効性評価の議論をまとめ、 全大腸内視鏡の有効性評価に
WEO の提唱する代奉指標評価を用いた理由を説明する。
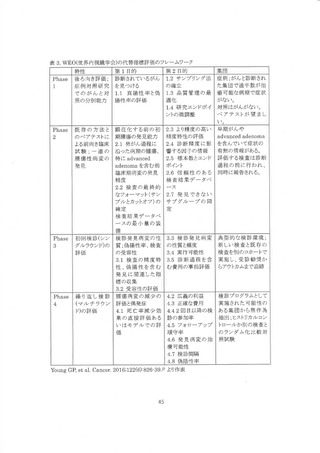
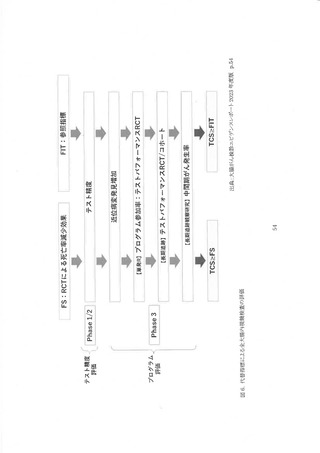
新技術の開発からがん検診への実装に至るプロセスには段階的な評価が必要である。 WEO の
代替指標評価以前に、Pepe らはバイオマーカーの開発とがん検診への応用を見据え、その評価
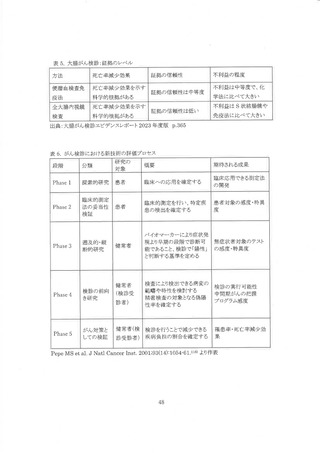
プロセスを表 6 のように 5 段階で示した。 具体的には、 患者集団における臨床的な有効性を確認
する初期段階(Phase1/2)に続いて、Phase3 以後は検診の有効性評価として健常者を対象に評
価を行う。 Phase3 ではバイオマーカーの感度・特異度が測定され、 検診において「陽性」と判断す
る基準を定める。 Phase4 では前向き研究により検診プログラムとしてテストパフォーマンス RCOT を
評価し、 検診の実効性を見据えてカットオフ値や偽陽性率、中間期がん発生率などを測定し、
Phase5 において死亡率をアウトカムとした RCT を行い、 検診プログラムとしての閑技術の評価が
最終的に決定されるとしている 1@9。 Pepe の Phase3 は WEO の代替指標評価のテスト精度に相
当し、テストパフォーマンスは Phase4 に相当する。 また、TPhase4 には中間期がん発生率も含まれ
る。
Lord らは代奉指標評価を行う条件を示した。 新技術の感度・特異度の測定は必須とし、さらに
新技術により追加的に検出される病変スペクトラム、 治療効果、 安全性・費用の検討を条件に挙げ
ている 17?。 標準方法で発見された病変と新技術によって追加で発見される病変のスペクトラムが
異なると治療の価値が異なる可能性があるため、 病変スペクトラムの比較検討は重要視されている。
また、 WEO は代装指標評価を実施する前提人条件として、(Q1)RCT で死亡率減少効果が確立され、
(②生物学的機護が類似した検査方法を参照基準とすることを挙げている 2.。 条件(2⑫)は、 検出病変
が異なる方法をテスト精度だけで判断することが難しいことを示している。
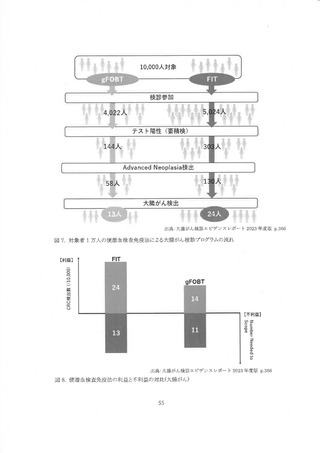
もし、 感度・特虹度のみで全大腸内視鏡の有効性評価を行うならば、 前提条件として化学法と免
疫法のように 18、 標準方法と新しい検査法によって検出される病変スペクトラムが生物学的に同
ーーである必要がある。 Grobbeeらの研究では、serrated polyp検出率は8状結腸鏡のほうが高く、
non-advanced adenoma 検出率は全大腸内視鏡のほうが高く、 両者の検出病変スペクトラムが異
なることを報告している 29。 また、近年公的データベースを用いた大型研究で病理組織型別の大
41
2019 年 7 月文献レビューが開始された時点では全大腸内視鏡の有効性を評価した RCT の報
告がなく、 本ガイドライン作成中の 2022 年 10 月に北欧諸国の NordICC 研究から中間解析が公
表されているのみである 39。 その他の ROT からも死亡率減少効果に関する報告がないため、本
ガイドラインでは観祭研究による評価に追加して WEO の代奉指標評価を行い、全大腸内視鏡の
有効性を評価した。 この議論の中で、 WEO の代次指標評価ではなく、 感度・特異度で判断する方
法や8 状結腸鏡の RCT の結果を外挿して判断する方法も提案された。
がん検診に新しい検査技術(以後、新技術)を採用する場合、RCT による有効性評価が長く用
いられてきた。 しかし、RCT は確実な科学的根拠が得られる一方、多くの費用や時間を要する。 そ
こで、中間アウトカムによる新技術の有効性を評価することが長年期待され、 議論さんてきた。 ここ
では、 中間アウトカムによる新技術の有効性評価の議論をまとめ、 全大腸内視鏡の有効性評価に
WEO の提唱する代奉指標評価を用いた理由を説明する。
新技術の開発からがん検診への実装に至るプロセスには段階的な評価が必要である。 WEO の
代替指標評価以前に、Pepe らはバイオマーカーの開発とがん検診への応用を見据え、その評価
プロセスを表 6 のように 5 段階で示した。 具体的には、 患者集団における臨床的な有効性を確認
する初期段階(Phase1/2)に続いて、Phase3 以後は検診の有効性評価として健常者を対象に評
価を行う。 Phase3 ではバイオマーカーの感度・特異度が測定され、 検診において「陽性」と判断す
る基準を定める。 Phase4 では前向き研究により検診プログラムとしてテストパフォーマンス RCOT を
評価し、 検診の実効性を見据えてカットオフ値や偽陽性率、中間期がん発生率などを測定し、
Phase5 において死亡率をアウトカムとした RCT を行い、 検診プログラムとしての閑技術の評価が
最終的に決定されるとしている 1@9。 Pepe の Phase3 は WEO の代替指標評価のテスト精度に相
当し、テストパフォーマンスは Phase4 に相当する。 また、TPhase4 には中間期がん発生率も含まれ
る。
Lord らは代奉指標評価を行う条件を示した。 新技術の感度・特異度の測定は必須とし、さらに
新技術により追加的に検出される病変スペクトラム、 治療効果、 安全性・費用の検討を条件に挙げ
ている 17?。 標準方法で発見された病変と新技術によって追加で発見される病変のスペクトラムが
異なると治療の価値が異なる可能性があるため、 病変スペクトラムの比較検討は重要視されている。
また、 WEO は代装指標評価を実施する前提人条件として、(Q1)RCT で死亡率減少効果が確立され、
(②生物学的機護が類似した検査方法を参照基準とすることを挙げている 2.。 条件(2⑫)は、 検出病変
が異なる方法をテスト精度だけで判断することが難しいことを示している。
もし、 感度・特虹度のみで全大腸内視鏡の有効性評価を行うならば、 前提条件として化学法と免
疫法のように 18、 標準方法と新しい検査法によって検出される病変スペクトラムが生物学的に同
ーーである必要がある。 Grobbeeらの研究では、serrated polyp検出率は8状結腸鏡のほうが高く、
non-advanced adenoma 検出率は全大腸内視鏡のほうが高く、 両者の検出病変スペクトラムが異
なることを報告している 29。 また、近年公的データベースを用いた大型研究で病理組織型別の大
41