よむ、つかう、まなぶ。
資料1‐2 令和6年度 業務実績概要説明資料 (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59553.html |
| 出典情報 | 厚生労働省国立研究開発法人等審議会 高度専門医療研究評価部会(第40回 8/7)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
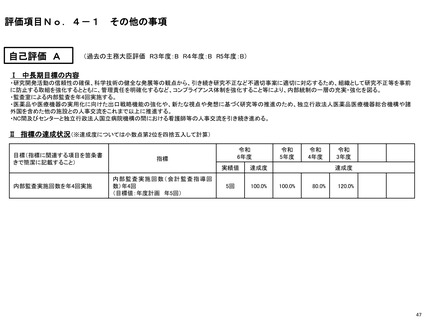
評価項目1-2
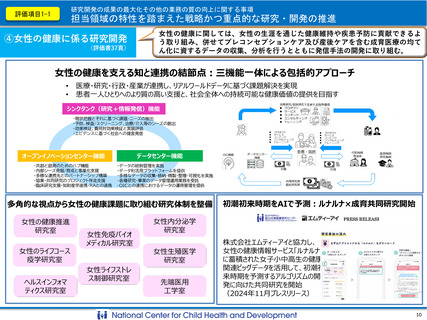
研究開発の成果の最大化その他の業務の質の向上に関する事項
実用化を目指した研究・開発の推進及び基盤整備
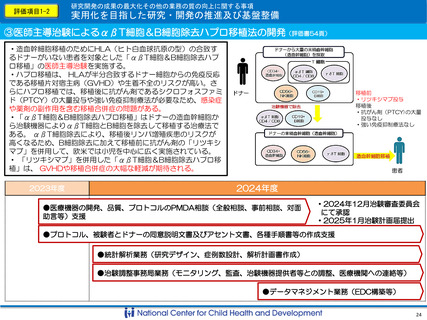
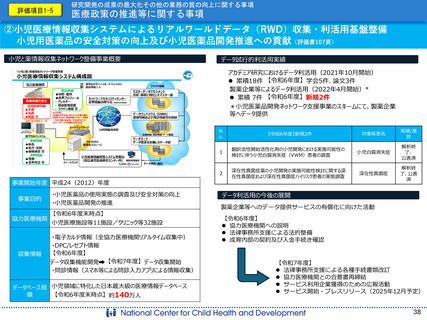
②国際共同ランダム化比較試験(国内医師主導治験)による小児及び若年成人再発急性骨髄性白
血病に対する新規治療薬の開発とドラッグ・ラグ/ロス解消(評価書54頁)
・小児急性骨髄性白血病は小児で2番目に多い白血病であり、再発後の予後は不良(寛解導入率60%以下、生存率30~40%)。
・ベネトクラクス(VEN)は、 BCL-2タンパク質を阻害して白血病細胞の細胞死を促す経口薬であり、化学療法に本剤を併用
する国際共同第Ⅲ相ランダム化比較試験がオランダ Princess Maxima Centerを中心に計画された。
・海外承認と同時に日本で承認取得するため、日本も本試験に参加し、本試験を日本における医師主導治験としても実施する。
・国立成育医療研究センターは、国際共同試験における日本のNational Coordinating Centerを務める(国内参加は数施設)。
・このような同時開発国際共同多施設医師主導治験の体制構築は、今後のドラッグ・ラグ/ロスに対する方策として重要である。
化学療法
最大2サイクル
A群
ランダム
割付
1:1
B群
米国グループ
欧州グループ
後治療
PedAL LLS
追跡
調査
化学療法+VEN
最大2サイクル
2022年度
後治療
2023年度
+他4医療機関
2024年度
2025年度
●日本のNational Coordinating Centerとしての業務
・欧州グループの治験調整事務局(オランダ)と国際会議を定期開催→海外の進捗確認、国内進捗報告
・日本と欧米の治験制度の違いの説明と合意
・国内参加施設の治験実施体制の整備(施設選定、契約締結)
●国内医師主導治験における治験調整事務局業務
・実施計画書の日本語訳レビュー、国内同意説明文書及びアセント文書、国内手順書等の作成・改訂
・国内での実施体制に係る調整(国内でのモニタリング、監査の調整、治験使用薬、検体の配送手配)、当局への副作用報告
・2024年6月治験審査委員会(小児治験NW活用)
にて承認
・2024年7月治験計画届提出、登録開始
・2025年2月国内1例目登録
23
研究開発の成果の最大化その他の業務の質の向上に関する事項
実用化を目指した研究・開発の推進及び基盤整備
②国際共同ランダム化比較試験(国内医師主導治験)による小児及び若年成人再発急性骨髄性白
血病に対する新規治療薬の開発とドラッグ・ラグ/ロス解消(評価書54頁)
・小児急性骨髄性白血病は小児で2番目に多い白血病であり、再発後の予後は不良(寛解導入率60%以下、生存率30~40%)。
・ベネトクラクス(VEN)は、 BCL-2タンパク質を阻害して白血病細胞の細胞死を促す経口薬であり、化学療法に本剤を併用
する国際共同第Ⅲ相ランダム化比較試験がオランダ Princess Maxima Centerを中心に計画された。
・海外承認と同時に日本で承認取得するため、日本も本試験に参加し、本試験を日本における医師主導治験としても実施する。
・国立成育医療研究センターは、国際共同試験における日本のNational Coordinating Centerを務める(国内参加は数施設)。
・このような同時開発国際共同多施設医師主導治験の体制構築は、今後のドラッグ・ラグ/ロスに対する方策として重要である。
化学療法
最大2サイクル
A群
ランダム
割付
1:1
B群
米国グループ
欧州グループ
後治療
PedAL LLS
追跡
調査
化学療法+VEN
最大2サイクル
2022年度
後治療
2023年度
+他4医療機関
2024年度
2025年度
●日本のNational Coordinating Centerとしての業務
・欧州グループの治験調整事務局(オランダ)と国際会議を定期開催→海外の進捗確認、国内進捗報告
・日本と欧米の治験制度の違いの説明と合意
・国内参加施設の治験実施体制の整備(施設選定、契約締結)
●国内医師主導治験における治験調整事務局業務
・実施計画書の日本語訳レビュー、国内同意説明文書及びアセント文書、国内手順書等の作成・改訂
・国内での実施体制に係る調整(国内でのモニタリング、監査の調整、治験使用薬、検体の配送手配)、当局への副作用報告
・2024年6月治験審査委員会(小児治験NW活用)
にて承認
・2024年7月治験計画届提出、登録開始
・2025年2月国内1例目登録
23