よむ、つかう、まなぶ。
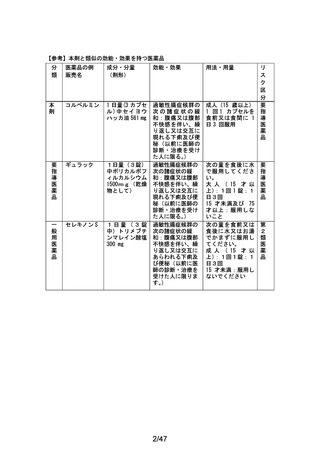
資料1-2 セイヨウハッカ油のリスク評価について (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59995.html |
| 出典情報 | 令和7年度第4回薬事審議会医薬品等安全対策部会安全対策調査会 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
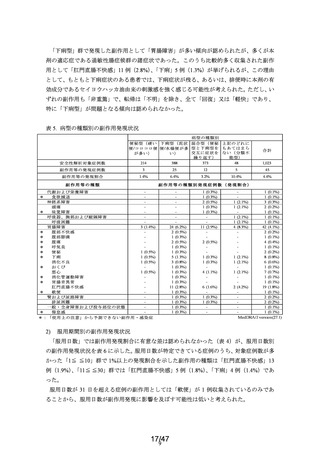
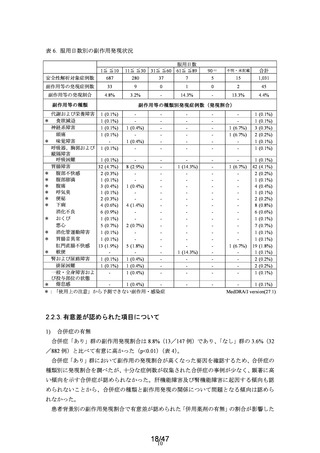
表 6. 服用日数別の副作用発現状況
1≦ ≦10
11≦ ≦30
31≦ ≦60
服用日数
61≦ ≦89
90=
不明・未記載
安全性解析対象症例数
687
280
37
7
5
15
合計
1,031
副作用等の発現症例数
33
9
0
1
0
2
45
副作用等の発現割合
4.8%
3.2%
-
14.3%
-
13.3%
4.4%
副作用等の種類
代謝および栄養障害 1 (0.1%)
食欲減退
1 (0.1%)
神経系障害
1 (0.1%)
頭痛
1 (0.1%)
* 味覚障害
呼吸器、胸郭および 1 (0.1%)
縦隔障害
呼吸困難
1 (0.1%)
胃腸障害
32 (4.7%)
* 腹部不快感
2 (0.3%)
* 腹部膨満
1 (0.1%)
* 腹痛
3 (0.4%)
* 呼気臭
1 (0.1%)
* 便秘
2 (0.3%)
* 下痢
4 (0.6%)
消化不良
6 (0.9%)
* おくび
1 (0.1%)
悪心
5 (0.7%)
* 消化管運動障害
1 (0.1%)
* 胃腸音異常
1 (0.1%)
肛門直腸不快感
13 (1.9%)
* 軟便
腎および尿路障害
1 (0.1%)
排尿困難
1 (0.1%)
一般・全身障害およ
び投与部位の状態
* 倦怠感
*
副作用等の種類別発現症例数(発現割合)
1 (0.4%)
1 (0.4%)
-
-
-
-
1 (6.7%)
1 (6.7%)
-
1 (0.1%)
1 (0.1%)
3 (0.3%)
2 (0.2%)
1 (0.1%)
1 (0.1%)
8 (2.9%)
1 (0.4%)
4 (1.4%)
2 (0.7%)
5 (1.8%)
1 (0.4%)
1 (0.4%)
1 (0.4%)
-
1 (14.3%)
1 (14.3%)
-
-
1 (6.7%)
1 (6.7%)
-
1 (0.1%)
42 (4.1%)
2 (0.2%)
1 (0.1%)
4 (0.4%)
1 (0.1%)
2 (0.2%)
8 (0.8%)
6 (0.6%)
1 (0.1%)
7 (0.7%)
1 (0.1%)
1 (0.1%)
19 (1.8%)
1 (0.1%)
2 (0.2%)
2 (0.2%)
1 (0.1%)
1 (0.4%)
-
-
-
-
1 (0.1%)
*:「使用上の注意」から予測できない副作用・感染症
MedDRA/J version(27.1)
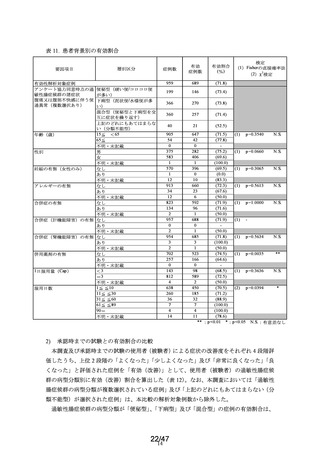
2.2.3. 有意差が認められた項目について
1)
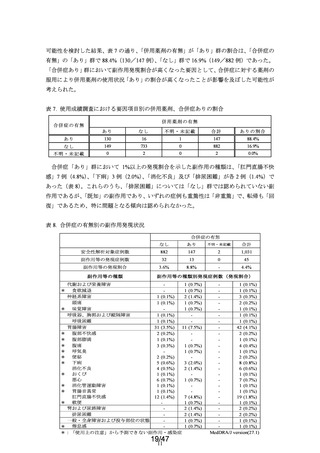
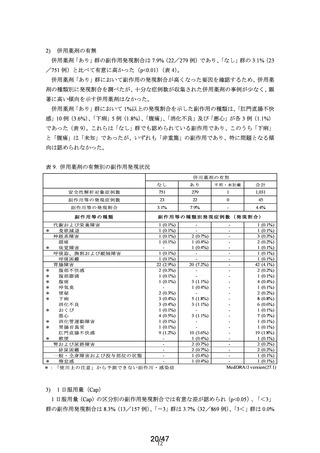
合併症の有無
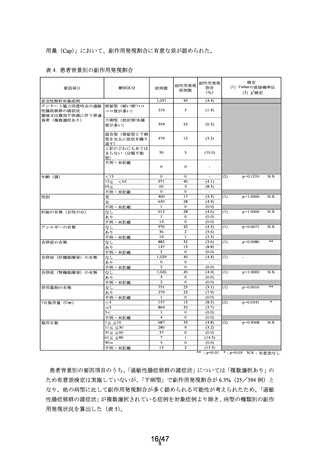
合併症「あり」群の副作用発現割合は 8.8%(13/147 例)であり、
「なし」群の 3.6%(32
/882 例)と比べて有意に高かった(p<0.01)(表 4)。
合併症「あり」群において副作用の発現割合が高くなった要因を確認するため、合併症の
種類別に発現割合を調べたが、十分な症例数が収集された合併症の事例が少なく、顕著に高
い傾向を示す合併症が認められなかった。肝機能障害及び腎機能障害に起因する傾向も認
められないことから、合併症の種類と副作用発現の関係について問題となる傾向は認めら
れなかった。
患者背景別の副作用発現割合で有意差が認められた「併用薬剤の有無」の割合が影響した
18/47
10
1≦ ≦10
11≦ ≦30
31≦ ≦60
服用日数
61≦ ≦89
90=
不明・未記載
安全性解析対象症例数
687
280
37
7
5
15
合計
1,031
副作用等の発現症例数
33
9
0
1
0
2
45
副作用等の発現割合
4.8%
3.2%
-
14.3%
-
13.3%
4.4%
副作用等の種類
代謝および栄養障害 1 (0.1%)
食欲減退
1 (0.1%)
神経系障害
1 (0.1%)
頭痛
1 (0.1%)
* 味覚障害
呼吸器、胸郭および 1 (0.1%)
縦隔障害
呼吸困難
1 (0.1%)
胃腸障害
32 (4.7%)
* 腹部不快感
2 (0.3%)
* 腹部膨満
1 (0.1%)
* 腹痛
3 (0.4%)
* 呼気臭
1 (0.1%)
* 便秘
2 (0.3%)
* 下痢
4 (0.6%)
消化不良
6 (0.9%)
* おくび
1 (0.1%)
悪心
5 (0.7%)
* 消化管運動障害
1 (0.1%)
* 胃腸音異常
1 (0.1%)
肛門直腸不快感
13 (1.9%)
* 軟便
腎および尿路障害
1 (0.1%)
排尿困難
1 (0.1%)
一般・全身障害およ
び投与部位の状態
* 倦怠感
*
副作用等の種類別発現症例数(発現割合)
1 (0.4%)
1 (0.4%)
-
-
-
-
1 (6.7%)
1 (6.7%)
-
1 (0.1%)
1 (0.1%)
3 (0.3%)
2 (0.2%)
1 (0.1%)
1 (0.1%)
8 (2.9%)
1 (0.4%)
4 (1.4%)
2 (0.7%)
5 (1.8%)
1 (0.4%)
1 (0.4%)
1 (0.4%)
-
1 (14.3%)
1 (14.3%)
-
-
1 (6.7%)
1 (6.7%)
-
1 (0.1%)
42 (4.1%)
2 (0.2%)
1 (0.1%)
4 (0.4%)
1 (0.1%)
2 (0.2%)
8 (0.8%)
6 (0.6%)
1 (0.1%)
7 (0.7%)
1 (0.1%)
1 (0.1%)
19 (1.8%)
1 (0.1%)
2 (0.2%)
2 (0.2%)
1 (0.1%)
1 (0.4%)
-
-
-
-
1 (0.1%)
*:「使用上の注意」から予測できない副作用・感染症
MedDRA/J version(27.1)
2.2.3. 有意差が認められた項目について
1)
合併症の有無
合併症「あり」群の副作用発現割合は 8.8%(13/147 例)であり、
「なし」群の 3.6%(32
/882 例)と比べて有意に高かった(p<0.01)(表 4)。
合併症「あり」群において副作用の発現割合が高くなった要因を確認するため、合併症の
種類別に発現割合を調べたが、十分な症例数が収集された合併症の事例が少なく、顕著に高
い傾向を示す合併症が認められなかった。肝機能障害及び腎機能障害に起因する傾向も認
められないことから、合併症の種類と副作用発現の関係について問題となる傾向は認めら
れなかった。
患者背景別の副作用発現割合で有意差が認められた「併用薬剤の有無」の割合が影響した
18/47
10