会議資料 (89 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00045.html |
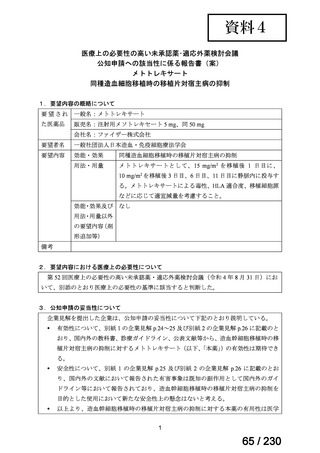
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第67回 2/6)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
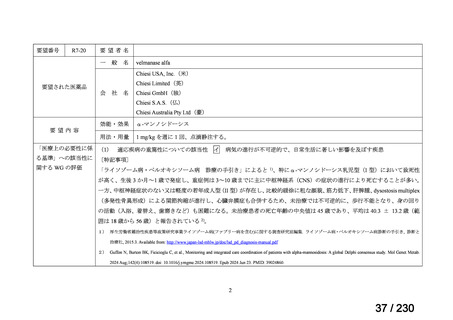
要望番号;IV-112
2. MTX 単独
MTX: 15 mg/m2(i.v.)
10 mg/m2(i.v.)
day 1
day 3, 6, 11
and weekly, until day 102
3. TAC + MTX
MTX: 15-10 mg/m2(i.v.)
10-7 mg/m2(i.v.)
day 1
day 3, 6, (11)
TAC: 0.02-0.03 mg/kg(cont. i.v.) day -1~
0.15 mg/kg(p.o.)
経口投与可能になった時点より day 50 まで
以降,週に 5%ずつ減量し,慢性 GVHD が発症していなければ 6 ヵ月で中止。
p41. 資料 4.免疫抑制剤の使用法 1.MTX
1) 用法・用量
① 15 mg/m2(day 1)
,10 mg/m2(day 3,6,11)が原法。
② 10 mg/m2(day 1)
,7 mg/m2(day 3,6,11)あるいは day 11 投与を省略する方法も HLA
適合同胞間移植時は採用されている。5 mg/m2 の少量投与も行われている。
③ 以下の場合は MTX の投与の減量・中止を考慮する。
腎障害,肝障害,重症口内炎,胸水,腹水,体重増加
④ 急性 GVHD や慢性 GVHD の 2 次治療として,MTX 3~10 mg/m2 の週 1 回投与も報告さ
れている。
2) 副作用:口内炎,肝障害,骨髄抑制など。大量 MTX 使用時に用いられる Folic acid が
造血幹細胞移植での MTX の副作用軽減に有効とする報告もあるが,保険適用外であ
る。
6.本邦での開発状況(経緯)及び使用実態について
(1)要望内容に係る本邦での開発状況(経緯)等について
本邦において,要望内容に係る開発は行っていない。
(2)要望内容に係る本邦での臨床試験成績及び臨床使用実態について
1)Kanda J, Biol. Blood Marrow Transplant 2016;22:744-51. [参考文献 38]
Center for International Blood and Marrow Transplant Research(CIBMTR)のデータベースおよ
び日本の移植登録一元管理プログラム登録データベースから得られたデータに基づいて,
HLA 適合同胞から初回の同種骨髄移植または末梢血幹細胞移植を受けた北米の白人
(n = 1,300)および日本人患者(n = 1,352)を対象とした後ろ向き研究を行った。日本人患
者では重度の急性 GVHD のリスクが低く,その結果,非再発性死亡率のリスクも低かった。
21
89 / 230