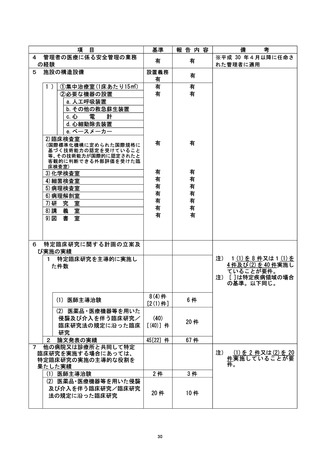
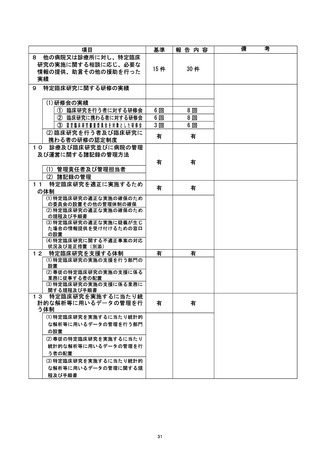
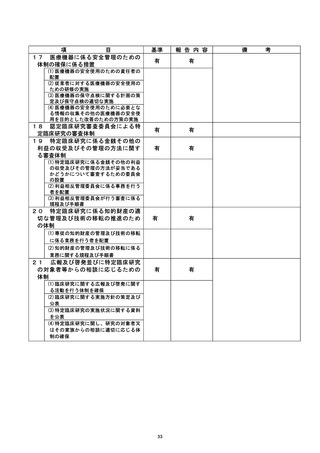
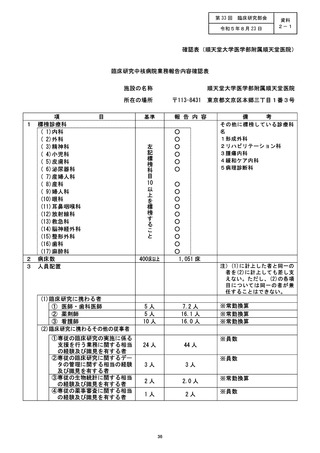
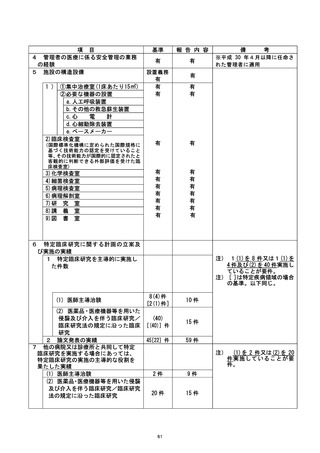
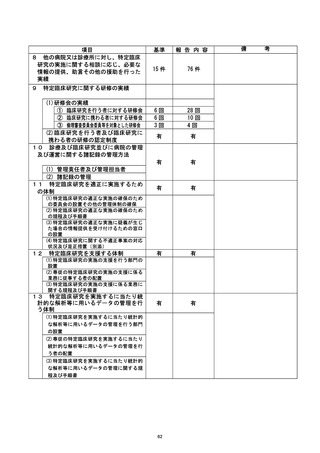
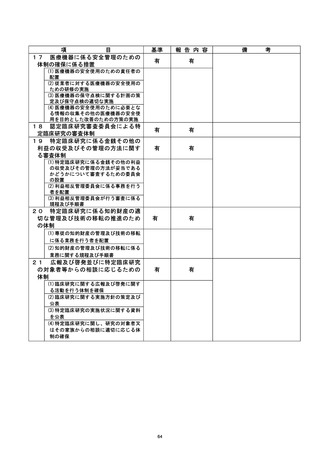
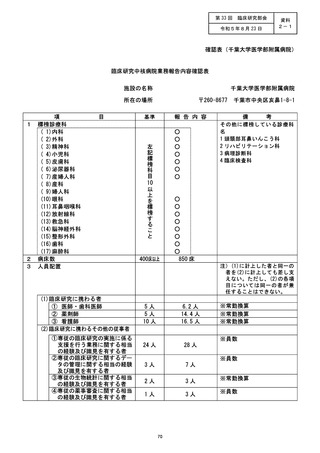
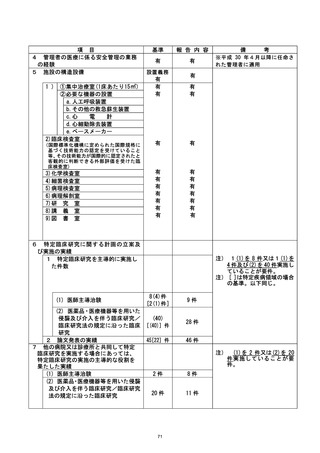
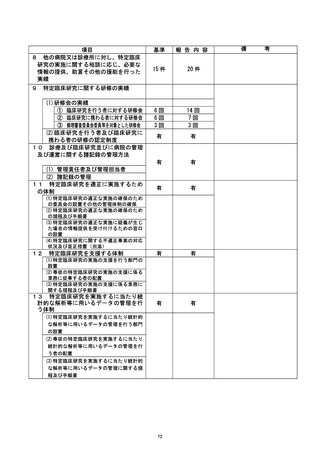
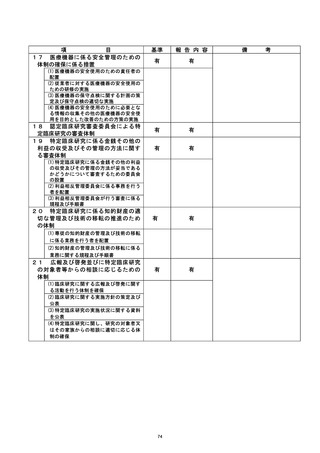
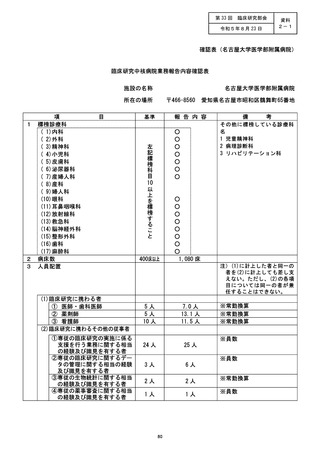
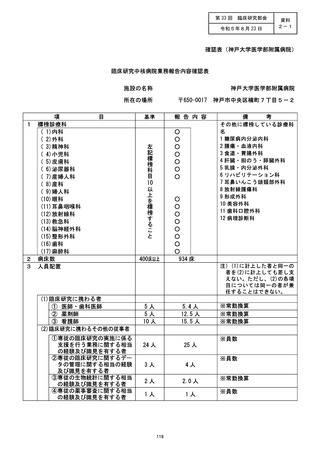
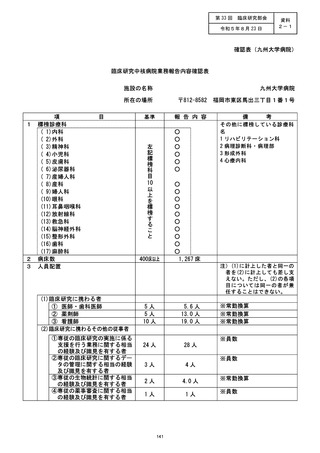
資料2:臨床研究中核病院業務報告内容確認表 (77 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34378.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第33回 8/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
| の継続が承認された。
是正措置 :
ータの提出を迅速に行い、早期にデータセンターでの確認が行われるよう運用を見
直す。 研究に参加しているすべての研究責任医師及び分担医師へ本事例を報告し、選択・
除外基準を再確認し、適格性を満たした患者を登録するよう注意喚起する。 なお、 当該
症例のデータの取り扱いについては、後日盲検下にて検討する。
登録 DD 等 に還請還詞 治験・臨床研究名
不適正事案の概要 :
除外基準に抵触する患者の登録
除外基準のひとつとして、鎮静剤に対してアレルギーを起こす可能性のある患者 (卵
アレルギー等のある患者) としたが、生卵にアレルギーを有する患者が登録されていた。
不適正事案に関する対応状況 :
生卵にアレルギーを有する患者が登録されていることが後日症例報告書を見直す際
に発覚した。同意書を取得した分担医師が、本研究の同意書を取得する件数がまだ少な
い時期であったため、その影響もあったと考えられる。
研究は予定通り終了し、本症例に関して有害事象は認めなかった。
2021 年 12 月 20 日の攻床研究審査委員会にて、 不適合の内容、 発生理由及び再発防止
索が説明された。審議の結果、本研究の継続については特に問題がないとされ、研究の
継続が承認された。
是正措置 : ー
研究分担医師には同意書取得時の手順書を配付していたが、再発防止策として、同意
取得時の見落としやすい項目を強調して記載する。また、複数名の分担医師で確認して
適格性を判断する。
き録 1 等 に還馬語詞 治験・臨床研究名
不適正事案の概要 :
選択基準に満たない愚者の登録
選択基準「2) 移やけ症状を有する(F スケール GERD 問診票の胸やけスコア 2 点以上) 」
に満たない症例を登録した。
不適正事案に関する対応状況 :
2021/11/17 内視鏡検査時 : 胸やけスコア 2点以上
2021/12/21 同意取得・症例登録時 : 胸やけスコアは1点であったが、2点以上にチ
77