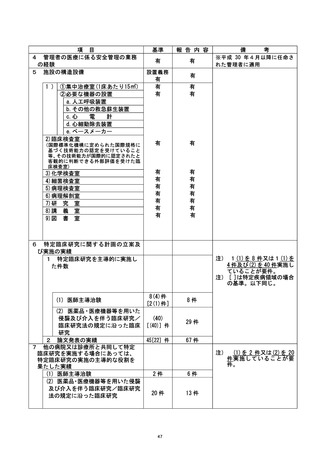
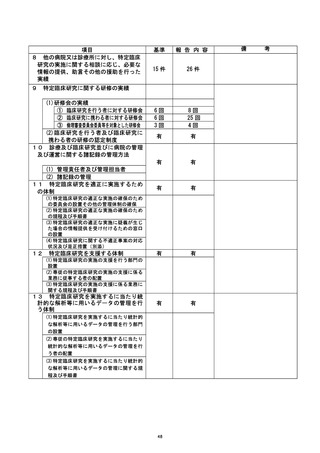
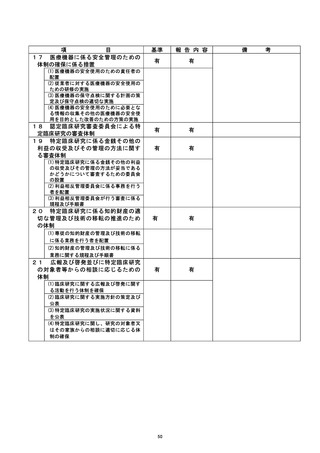
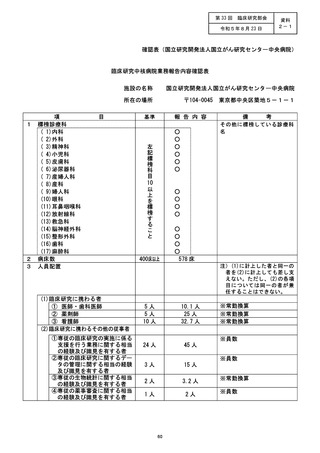
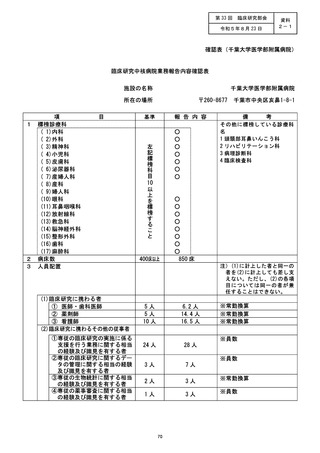
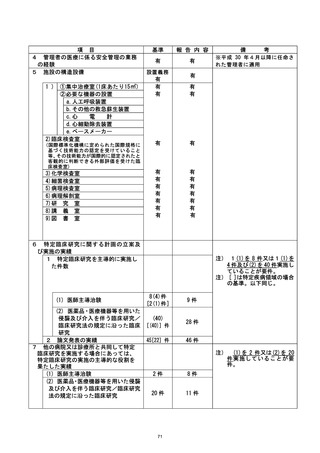
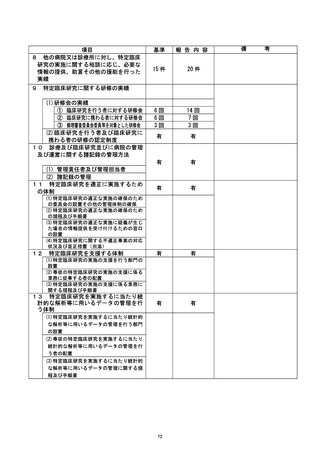
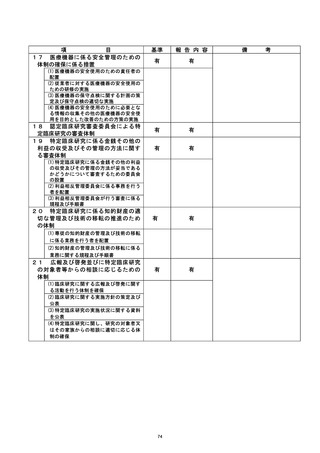
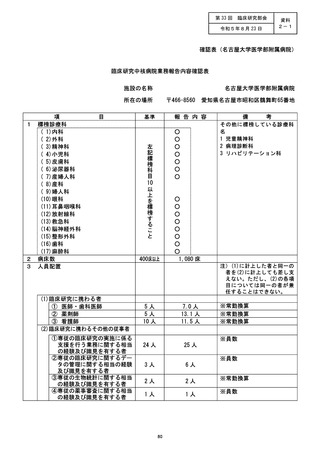
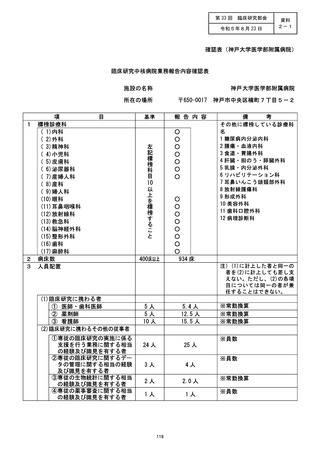
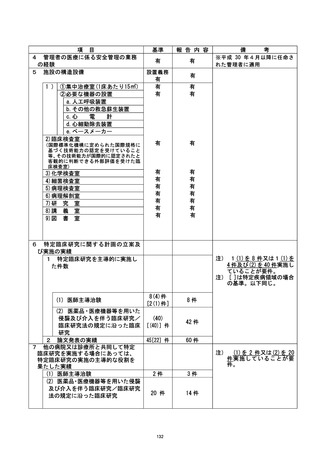
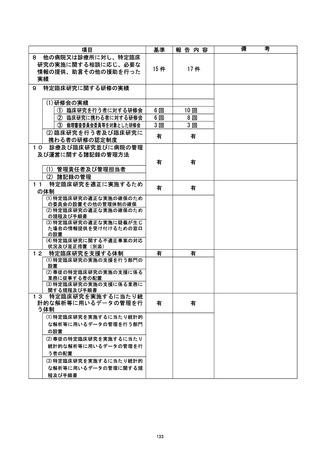
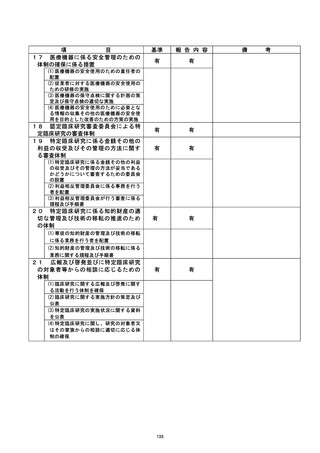
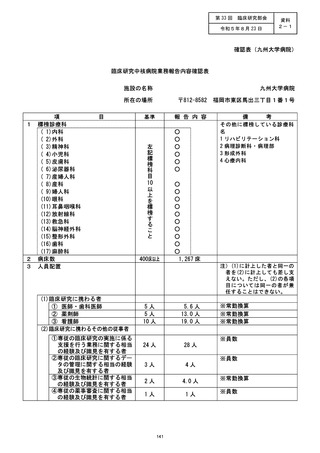
資料2:臨床研究中核病院業務報告内容確認表 (111 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34378.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第33回 8/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
聴取した。被験者から残薬を預かり、薬剤部に返却するまでの間に治験薬の紛失があっ |
たと考えられる。
不適正事案に関する対応状況 : 被験者からは残薬回収後であり、安全性に問題ないこ
を確認 した 関する衝設を反索したが上当たらなかったため和拓として名吾をする
是正措置 : 残薬は当日中に返却処理を徹底する
治験プロセスシートに残薬(治験薬) 回収後の取扱いについて明文化した。
登録D等 | 請請畔 治験名
不適正事案の概要 :
治験薬滞増期の投与量の間違い
二重盲検汰増期 (Visit8) に院内にて治験薬を服用した。その際に 4 錠中 1 錠を被験者
が落としてしまったため、担当 CRC は指定外シートから治験薬 1 錠を服用させた。同日、
指定外シートは来院日が延長した場合や指定シートの治験薬が汚染されたなど問題ヵ
ある時に使用するものであり、その際は 1 日分すべてを服用するもので、1 錠だけを服
用することはできないシートであったことを別のCRC より指摘を受け逸脱が判明した。
指定外シートの使用方法を間違ったため治験薬の服薬用量が不明となってしまった。
不適正事案に関する対応状況 :
被験者へ状況説明を行い、治験継続の意思確認を行った。 治験薬の楽物動態を考慮し服
楽 2 時間後まで院内で体調を確認し、被験者の安全性に問題ないことを確認した。治験
薬の服用は通常通り行いながら 2 日後まで本人に電話連絡し、安全性に確認を行った。
今回の服用量は実到であった場合でも 300mg であることが分かった。本治験の過量投与
規定は 400 mg以上であったため、キーオープンには至らず治験の継続は可能であること
を依頼者に確認し、被験者への安全性にも問題ないことから治験継続に問題ないという
判断に至った。
是正措置 : |
治験実施計画書にて二重盲検法による最初の潤増投与と治験薬シートの服用方法につ
いて依頼者よりレクチャーを受け、正しい服用方法 (服薬シートの使い方等) 人
と被験者へ指導した。
登録ID等 | 請還還還還還 臨床研究名
不適正事案の概要 :
モニタリンググループが実施した「研究者が実施するモニタリングに対する品質管理活
動」の結果、以下の同意に関する不備・不適合が発生していることが発覚した。
①jRCT 初回公表日より前に同意取得していた。
②全盲者の賭名欄に担当医師が代筆箸名をしていた。
③分担医師でない医師が説明者として署名していた。
④患者本人の署名なく研究が実施されていた。
111