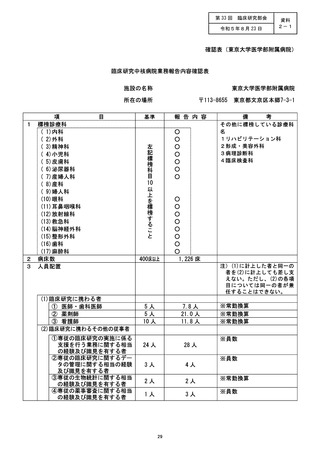
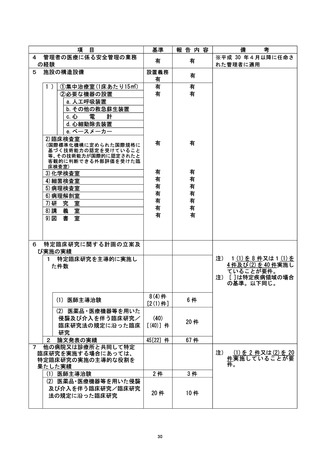
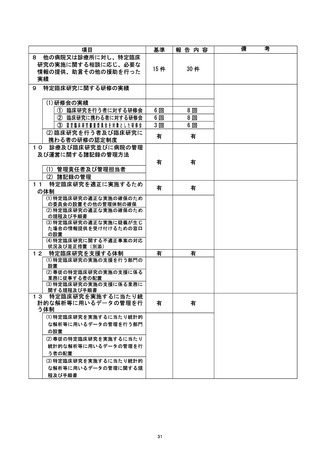
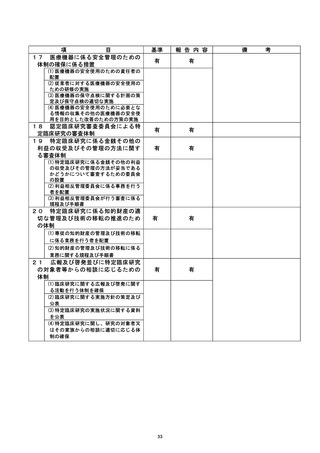
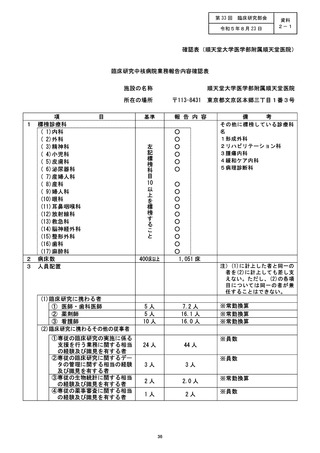
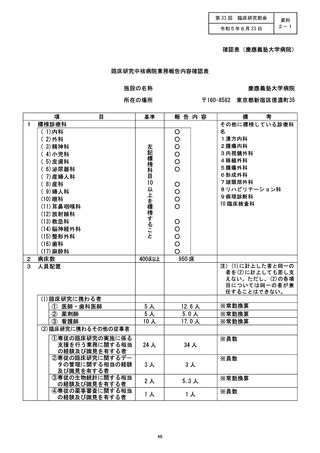
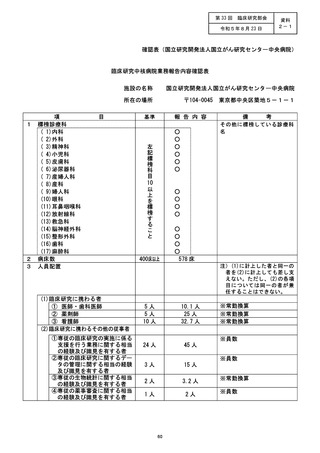
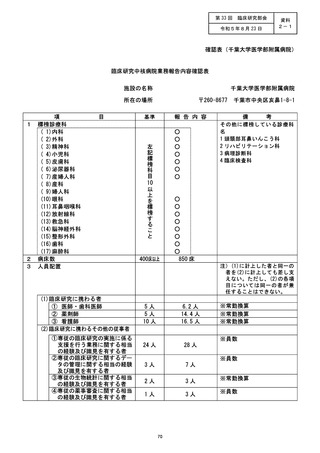
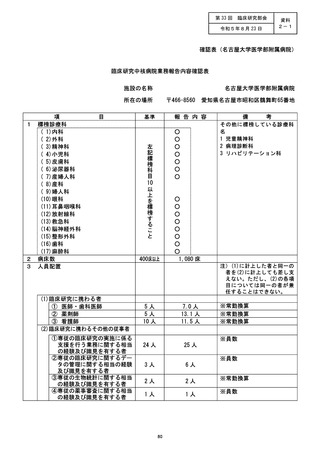
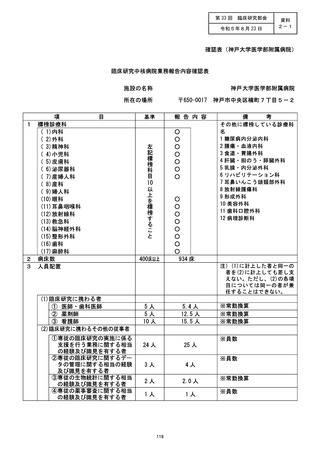
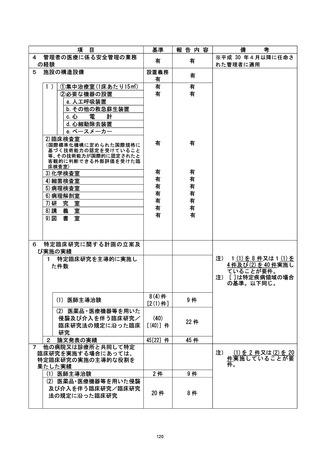
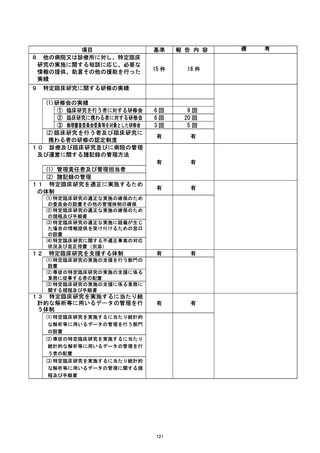
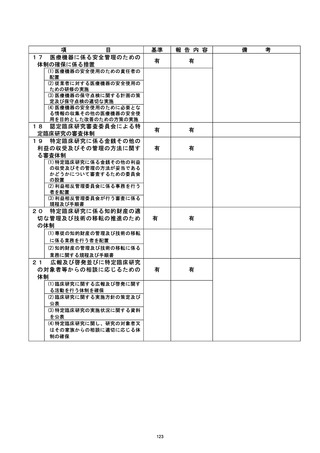
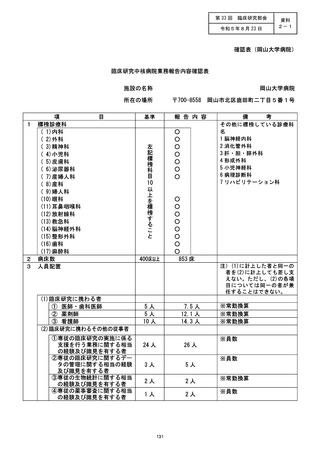
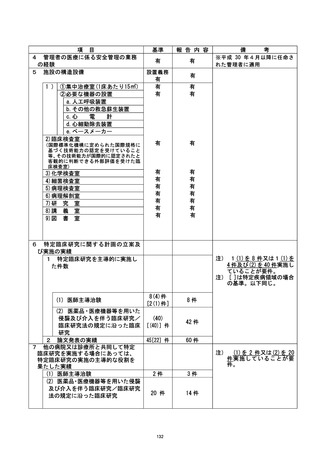
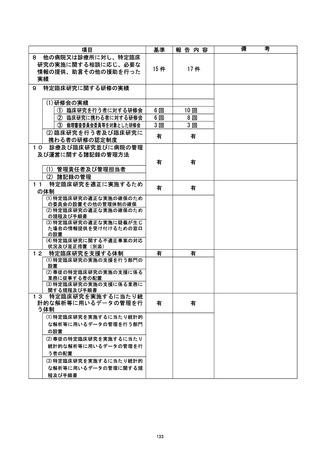
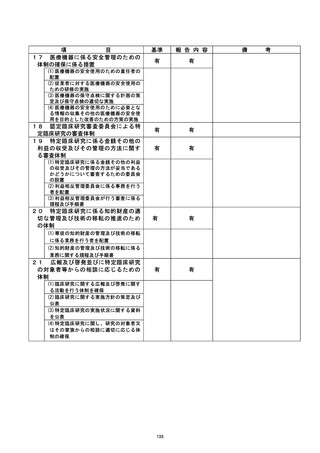
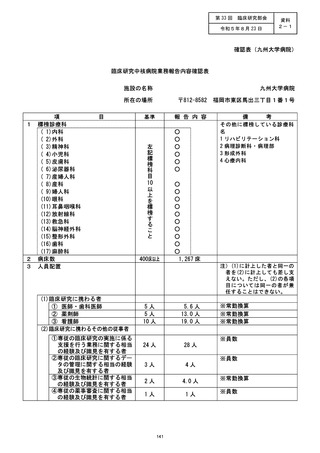
資料2:臨床研究中核病院業務報告内容確認表 (25 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34378.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第33回 8/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
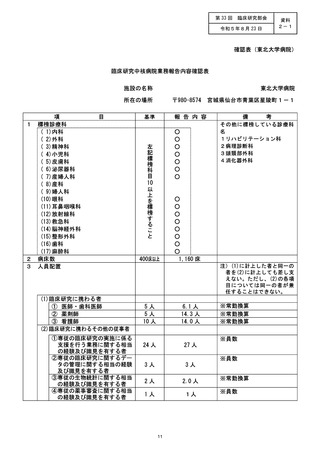
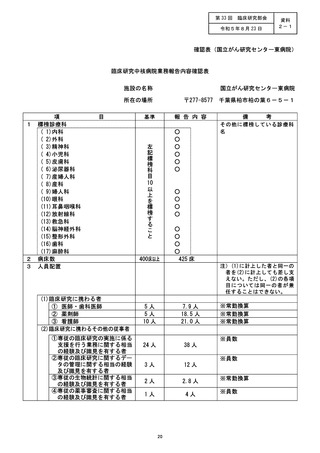
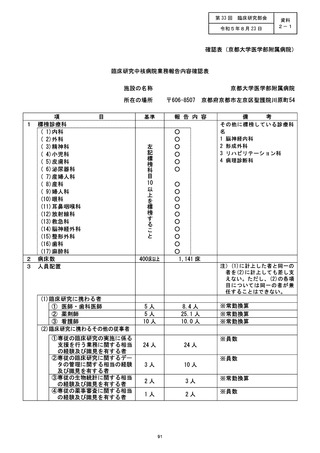
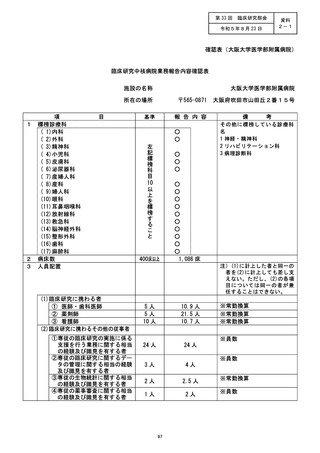
施設の名称 (国立がん研究センター東病院)
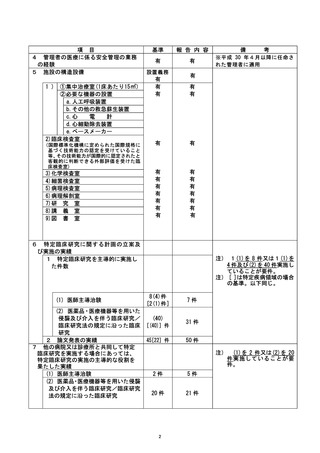
特定臨計研究に関する不適正事案
※ 当院の臨床研究適正実施推進部会及び臨床研究管理委員会にて検討を行い、病院長よ
り何らかの是正措置・予防措置等を指示した事案について掲載する。
登録 ID 等 還証還還 治験・臨床研究名 | 特定臨床研究 (先進医療 B) |
の有効性の検証
と標準化に向けた多施設
| ーーはーーニーニー | 共同研究 |
不適正事案の概要 : |
先進医療Bの試験において、同意書に関する不備が 2 例に認められた。
① 同意書未保管
② 他試験の IC 文書が保存
(多施設共同研究[他機関主導]、他機関 CRB)
本事例は、当該試験の監査により判明した。
上記同意取得は2015年6月及び2016年8月であり、監査は 2021 年3 月から実施され
た。
監査の所見を受け、他機関所属の研究代表医師は CRB に重大な不適合として報告、2021
年 6 月開催の CRB にて報告され、その結果 CRB から厚労大臣に意見が提出された。また
厚労省先進医療技術部会にて報告が行われた。
| 不適正事案に関する対応状況 :
他機関研究代表医師により、是正措置及び予防措置が策定された。
研究責任医師からは 2021 年 7 月に病院長宛て、CRB の審議結果も含む当該重大な不適合
に関する報告が行われた。 報告後、 直ちに適正実施推進部会委員 (臨床研究支援部門長、
研究企画室長、研究監倉室長) が当該研究責任医師に不適合の内容、原因、及び当該実
施診療科としての再発防止策に関してインタビューにて確認を行い、 病院長及び副院長
(研究担当) にその結果を報告した。
本事案はその後、上臨床研究適正実施推進部会、臨床研究管理委員会にて審議された。ま
た医療安全報告事象検討も行われた。 なお、先進医療技術部会の審議後、2022 年5 月の
想床研究適正実施推進部会及び臨床研究管理委員会にて同部会の審議内容の確認・共有
を行った。
是正措置 :
臨床研究適正実施推進部会で当該研究の研究代表医師及び研究貢任医師が立案した是
正措置案を確認し、了床研究管理委員会においても確認を行った。
病院長の指示により、全研究者への周知のため緊急セミナーを eLearning にて開催
した。また当該事案発生時には設置されていなかったローカル支援室員にも周知を
行うこととした。
研究責任医師は以下を行った。
> 研究責任医師は、 当該 2 例の患者に対して電話にて謝罪後、 外来受診時の 2021
年/月及び8月に再度説明文書を用いて説明の上、再同意を取得した。
と 診療科内での情報共有を行い、 改めて同意の経緯を診療録に記録することを徹
25