よむ、つかう、まなぶ。
資 料4-2 令和4年度第1回安全技術調査会の審議結果について (95 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26025.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第1回 6/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
※注4
検査項目の中には核酸増幅検査(以下「NAT」という。
)等外注が必要なもの
※注2
検査項目の中には核酸増幅検査(以下「NAT」という。
)等外注が必要なもの
もあることから、衛生検査所における感度及び特異度の確認も求められる(8
もあることから、衛生検査所における感度及び特異度の確認も求められる(7
(1)及び(2)イ参照)
。
(1)及び(2)イ参照)
。
※注5
(略)
※注3
(略)
※注6
(略)
※注4
(略)
※注7
(略)
※注5
(略)
※注8
(略)
※注6
(略)
※注9
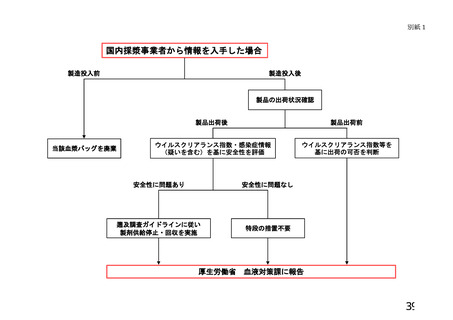
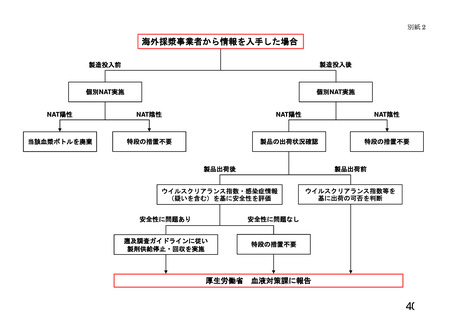
原料血漿については個別 NAT で陰性と判明した時点で、供給を再開する。
※注7
原料血漿については保管検体の個別 NAT で陰性と判明した時点で、供給を
再開する。
※注 10
(略)
※注8
(略)
※注 11
(略)
※注9
(略)
※注 12
血液製剤等の生物由来製品については、最新の科学的知見に基づく安全対
※注 10
策を講じたとしても感染症を伝播するおそれを完全には否定できないこと
血液製剤等の生物由来製品については、最新の科学的知見に基づく安全対
策を講じたとしても感染症を伝播するおそれを完全には否定できないこと
24
93
検査項目の中には核酸増幅検査(以下「NAT」という。
)等外注が必要なもの
※注2
検査項目の中には核酸増幅検査(以下「NAT」という。
)等外注が必要なもの
もあることから、衛生検査所における感度及び特異度の確認も求められる(8
もあることから、衛生検査所における感度及び特異度の確認も求められる(7
(1)及び(2)イ参照)
。
(1)及び(2)イ参照)
。
※注5
(略)
※注3
(略)
※注6
(略)
※注4
(略)
※注7
(略)
※注5
(略)
※注8
(略)
※注6
(略)
※注9
原料血漿については個別 NAT で陰性と判明した時点で、供給を再開する。
※注7
原料血漿については保管検体の個別 NAT で陰性と判明した時点で、供給を
再開する。
※注 10
(略)
※注8
(略)
※注 11
(略)
※注9
(略)
※注 12
血液製剤等の生物由来製品については、最新の科学的知見に基づく安全対
※注 10
策を講じたとしても感染症を伝播するおそれを完全には否定できないこと
血液製剤等の生物由来製品については、最新の科学的知見に基づく安全対
策を講じたとしても感染症を伝播するおそれを完全には否定できないこと
24
93