よむ、つかう、まなぶ。
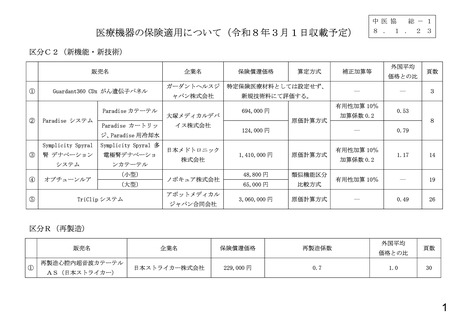
総-1医療機器及び臨床検査の保険適用について (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_69213.html |
| 出典情報 | 中央社会保険医療協議会 総会(第644回 1/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
製品概要
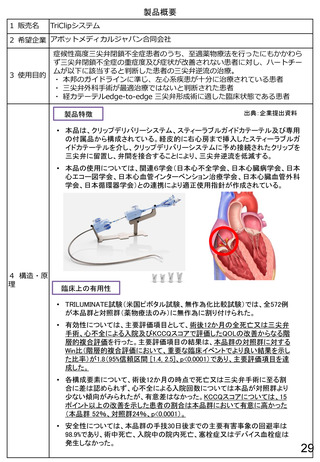
1 販売名
エクルーシス試薬 Anti-AAVrh74
2 希望企業
ロシュ・ダイアグノスティックス株式会社
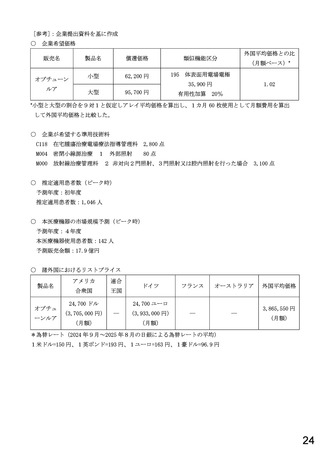
血清又は血漿中の抗アデノ随伴ウイルス血清型rh74(抗AAVrh74)抗
体の検出(デランジストロゲン モキセパルボベクのデュシェンヌ型筋
ジストロフィー患者への適応を判定するための補助)
3 使用目的
出典:企業提出資料
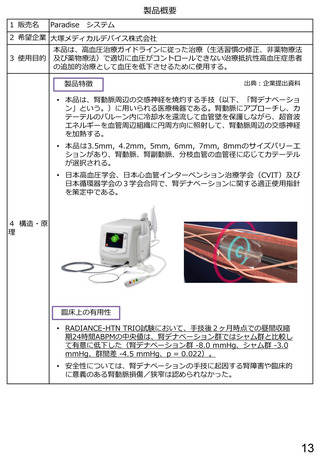
製品特徴
•
本品は、血清又は血漿中の抗アデノ随伴ウイルス血清型
rh74(抗AAVrh74)抗体の検出(デランジストロゲン モキセパル
ボベク(以下、「同剤」という。)のデュシェンヌ型筋ジスト
ロフィー患者への適応を判定するための補助)を目的として使用
する体外診断用医薬品である。測定原理はECLIA法である。
臨床上の有用性
4 構造・原
理
•
同剤は、抗AAVrh74抗体を保有している患者に対しては、免疫
応答反応により薬効の減弱等をもたらす可能性があるため、同
剤の投与に当たっては、抗AAVrh74抗体が陰性であることを確
認する必要がある。
•
本品の性能について、同剤の第Ⅲ相臨床試験で使用した146検
体を用いて、同試験における患者の組み入れに用いられた検査
(ELISA法)と本品の同等性の比較を行った試験の結果は以下
のとおりであり、本品が同剤の適応判定を行うための十分な性
能を示すことが示された。
ELISA法
本品
(ECLIA法)
陽性
陰性
陽性
14
0
陰性
4
128
陽性一致率:77.8% (95 % CI: 54.8-91.0%)
陰性一致率:100% .(95 % CI: 97.1-100%)
全体一致率:97.3% (95 % CI: 93.2-98.9%)
46
1 販売名
エクルーシス試薬 Anti-AAVrh74
2 希望企業
ロシュ・ダイアグノスティックス株式会社
血清又は血漿中の抗アデノ随伴ウイルス血清型rh74(抗AAVrh74)抗
体の検出(デランジストロゲン モキセパルボベクのデュシェンヌ型筋
ジストロフィー患者への適応を判定するための補助)
3 使用目的
出典:企業提出資料
製品特徴
•
本品は、血清又は血漿中の抗アデノ随伴ウイルス血清型
rh74(抗AAVrh74)抗体の検出(デランジストロゲン モキセパル
ボベク(以下、「同剤」という。)のデュシェンヌ型筋ジスト
ロフィー患者への適応を判定するための補助)を目的として使用
する体外診断用医薬品である。測定原理はECLIA法である。
臨床上の有用性
4 構造・原
理
•
同剤は、抗AAVrh74抗体を保有している患者に対しては、免疫
応答反応により薬効の減弱等をもたらす可能性があるため、同
剤の投与に当たっては、抗AAVrh74抗体が陰性であることを確
認する必要がある。
•
本品の性能について、同剤の第Ⅲ相臨床試験で使用した146検
体を用いて、同試験における患者の組み入れに用いられた検査
(ELISA法)と本品の同等性の比較を行った試験の結果は以下
のとおりであり、本品が同剤の適応判定を行うための十分な性
能を示すことが示された。
ELISA法
本品
(ECLIA法)
陽性
陰性
陽性
14
0
陰性
4
128
陽性一致率:77.8% (95 % CI: 54.8-91.0%)
陰性一致率:100% .(95 % CI: 97.1-100%)
全体一致率:97.3% (95 % CI: 93.2-98.9%)
46