よむ、つかう、まなぶ。
03資料1-1森野委員提出資料(高齢者に対するインフルエンザワクチンファクトシート) (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64997.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第32回 10/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(6) 諸外国の導入状況
① 高齢者における季節性インフルエンザワクチンの種類
本邦において、高齢者の定期接種に使用可能な季節性インフルエンザワクチンは、現時点で SD-IIV の
みに限られている。一方 HD-IIV は国内で承認されているものの、任意接種においてのみ使用可能であ
る。
これに対し、諸外国においては、SD-IIV および HD-IIV に加え、主に以下の 3 種類のワクチンが用い
られている。
1.
組換えタンパクインフルエンザワクチン(recombinant influenza vaccine: RIV)
2.
アジュバンド添加不活化インフルエンザワクチン(adjuvanted inactivated influenza vaccine: aIIV)
3.
細胞培養不活化インフルエンザワクチン(Cell culture-based inactivated influenza vaccine: ccIIV)
RIV は、製造工程においてワクチンウイルスや鶏卵を使用せず、製造施設内で合成的に生産される 90。
また、HD-IIV と同様に高用量ワクチンであり、SD-IIV と比較してヘマグルチニン(HA)抗原の含有量が
多い 91。
aIIV には、接種による免疫応答を強化するためにアジュバンドが添加されており、非アルミニウム系
で水中油型乳剤の MF59 が広く用いられている 92。高齢者は若年者と比較してインフルエンザワクチン
接種後の防御免疫応答が低いことから、aIIV は高齢者を主な対象として使用される 93。
ccIIV は、哺乳類細胞培養技術を用いて製造され、細胞培養由来の候補ワクチンウイルス(CVV)のみを
使用している。一方、SD-IIV や HD-IIV は鶏卵培養を用いて製造されるが、鶏卵内でのウイルス増殖過
程において抗原性の低下を引き起こす変異が生じる可能性がある。ccIIV の製造行程では、このような抗
原変異による問題を回避できるとされている 94。
② 季節性インフルエンザワクチンの推奨および導入状況
これら 5 種類のワクチンの推奨および導入状況については、各国で異なる方針が採られている。
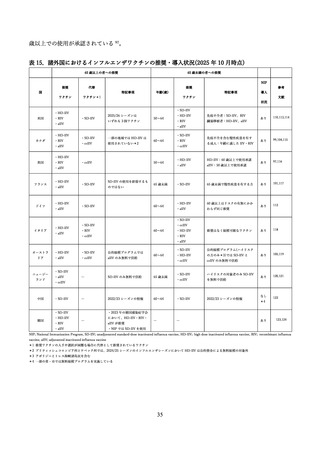
G7(Group of Seven: 主要国首脳会議)および周辺諸国における、高齢者に対する推奨インフルエンザ
ワクチンの一覧を表 15 に示す。
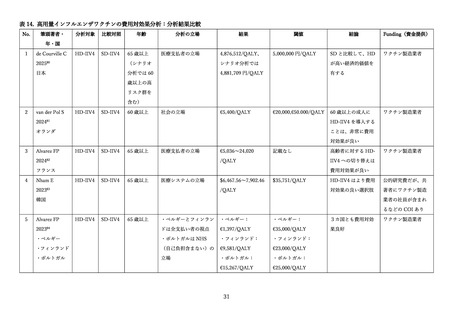
米国においては、臨床試験に基づく免疫原性、安全性の評価を踏まえ、2010/11 シーズンより、65 歳
以上の高齢者に対する HD-IIV3 の推奨および導入が決定された。ただし、当時は SD-IIV との間での推
奨の優劣はなかった 95。その後、2022/23 シーズンからは、システマティックレビューと GRADE(Grading
of Recommendations Assessment, Development and Evaluation)手法、さらに ACIP(Advisory Committee
on Immunization Practices)のフレームワークに基づく評価により、65 歳以上の高齢者に対し、HD-IIV・
RIV・aIIV(いずれも 4 価)の接種が推奨された 96。
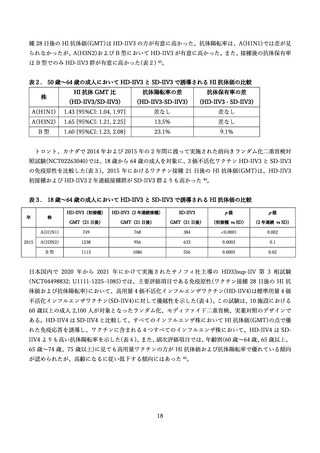
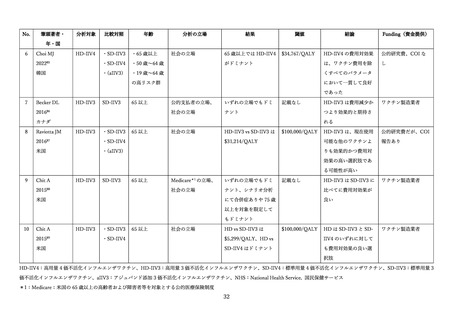
英国では、2017 年に aIIV、2018 年に HD-IIV について有効性、費用対効果の評価が行われ、これらの
結果を踏まえて両ワクチンの接種推奨が決定された 97。
カナダにおいては、2016/17 シーズンに HD-IIV の有効性と安全性が評価され、導入が決定された 98。
さらに、2024 年 7 月には文献レビューが実施され、
有効性や安全性に加え、
EEFA(ethics, equity, feasibility,
and acceptability)フレームワークに基づいて評価が行われ、HD-IIV・RIV・aIIV のいずれかの接種を推
33
① 高齢者における季節性インフルエンザワクチンの種類
本邦において、高齢者の定期接種に使用可能な季節性インフルエンザワクチンは、現時点で SD-IIV の
みに限られている。一方 HD-IIV は国内で承認されているものの、任意接種においてのみ使用可能であ
る。
これに対し、諸外国においては、SD-IIV および HD-IIV に加え、主に以下の 3 種類のワクチンが用い
られている。
1.
組換えタンパクインフルエンザワクチン(recombinant influenza vaccine: RIV)
2.
アジュバンド添加不活化インフルエンザワクチン(adjuvanted inactivated influenza vaccine: aIIV)
3.
細胞培養不活化インフルエンザワクチン(Cell culture-based inactivated influenza vaccine: ccIIV)
RIV は、製造工程においてワクチンウイルスや鶏卵を使用せず、製造施設内で合成的に生産される 90。
また、HD-IIV と同様に高用量ワクチンであり、SD-IIV と比較してヘマグルチニン(HA)抗原の含有量が
多い 91。
aIIV には、接種による免疫応答を強化するためにアジュバンドが添加されており、非アルミニウム系
で水中油型乳剤の MF59 が広く用いられている 92。高齢者は若年者と比較してインフルエンザワクチン
接種後の防御免疫応答が低いことから、aIIV は高齢者を主な対象として使用される 93。
ccIIV は、哺乳類細胞培養技術を用いて製造され、細胞培養由来の候補ワクチンウイルス(CVV)のみを
使用している。一方、SD-IIV や HD-IIV は鶏卵培養を用いて製造されるが、鶏卵内でのウイルス増殖過
程において抗原性の低下を引き起こす変異が生じる可能性がある。ccIIV の製造行程では、このような抗
原変異による問題を回避できるとされている 94。
② 季節性インフルエンザワクチンの推奨および導入状況
これら 5 種類のワクチンの推奨および導入状況については、各国で異なる方針が採られている。
G7(Group of Seven: 主要国首脳会議)および周辺諸国における、高齢者に対する推奨インフルエンザ
ワクチンの一覧を表 15 に示す。
米国においては、臨床試験に基づく免疫原性、安全性の評価を踏まえ、2010/11 シーズンより、65 歳
以上の高齢者に対する HD-IIV3 の推奨および導入が決定された。ただし、当時は SD-IIV との間での推
奨の優劣はなかった 95。その後、2022/23 シーズンからは、システマティックレビューと GRADE(Grading
of Recommendations Assessment, Development and Evaluation)手法、さらに ACIP(Advisory Committee
on Immunization Practices)のフレームワークに基づく評価により、65 歳以上の高齢者に対し、HD-IIV・
RIV・aIIV(いずれも 4 価)の接種が推奨された 96。
英国では、2017 年に aIIV、2018 年に HD-IIV について有効性、費用対効果の評価が行われ、これらの
結果を踏まえて両ワクチンの接種推奨が決定された 97。
カナダにおいては、2016/17 シーズンに HD-IIV の有効性と安全性が評価され、導入が決定された 98。
さらに、2024 年 7 月には文献レビューが実施され、
有効性や安全性に加え、
EEFA(ethics, equity, feasibility,
and acceptability)フレームワークに基づいて評価が行われ、HD-IIV・RIV・aIIV のいずれかの接種を推
33