薬-1令和8年度薬価改定について➄ (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_66037.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第241回 11/19)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
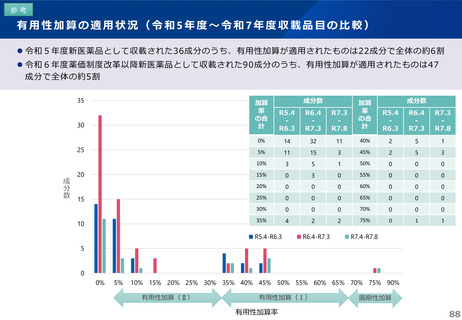
新規作用機序医薬品の⾰新性・有用性の基準に該当する新薬については、薬価収載時には有用性系加算の対象となり得る。
新規作用機序医薬品の革新性・有用性の基準
類似する有用性系加算項目
新規作用機序に
より既存治療で
効果不十分な疾
患に有効性を示
したものである
こと
当該疾患に対する標準療法で効果不十分又は不耐容の患者を
含む臨床試験(当初の承認を目的として実施されたもので、
効果不十分又は不耐容の患者の目標症例数が事前に設定され
た企業治験に限る。)において有効性が示されることなどに
より、添付文書の効能・効果、使用上の注意、臨床試験成績
の項において、これらの患者に対して投与可能であることが
明示的になっているものであること。
③ 対象疾病の治療方法の改善
a. 既存の治療方法では効果が不十分な患者群、あるいは安全性等
の理由で既存の治療方法が使用できない患者群において効果が認
められる
新規作用機序に
より既存治療に
対して比較試験
により優越性を
示したものであ
ること
対象疾患に対する既存治療(本邦における治療方法として妥
当性があるものに限る。)を対照群(プラセボ除く)に設定
した臨床試験(当初の承認を目的として実施されたもので、
優越性を検証することを目的とした仮説に基づき実施された
企業治験に限る。)を実施し、主要評価項目において既存治
療に対する本剤の優越性が示されていること。
また、製造販売後において、当初の承認時の疾患を対象とし
た製造販売後臨床試験も同様に取り扱うものとする。
② 類似薬に比した高い有効性又は安全性
②-1 高い有効性又は安全性の内容
a. 臨床上重要な有効性指標において類似薬に比した高い有効性が
示される
新規作用機序に
より認められた
効能を有する他
の医薬品が存在
しないこと
① 臨床上有用な新規の作用機序
a. 薬理作用発現のための薬剤の作用点(部位)が既収載品目と大
きく異なる
b. 薬理作用発現のための薬剤の標的分子(酵素、受容体など)が
既収載品目と異なる
薬事承認時点において、本剤と効能・効果が一致するものが
なく、対象疾患に対して初めての治療選択肢を提供するもの、 ③ 対象疾病の治療方法の改善
又は類似の効能・効果を有する既存薬と比べて、治療対象と
a. 既存の治療方法では効果が不十分な患者群、あるいは安全性等
なる患者の範囲が拡大することが明らかであるもの。
の理由で既存の治療方法が使用できない患者群において効果が認
められる
c.既存の治療方法に比べて効果の発現が著しく速い若しくは効果
の持続が著しく長い、又は使用に際しての利便性が著しく高い
(製剤工夫によるものを除く)
21