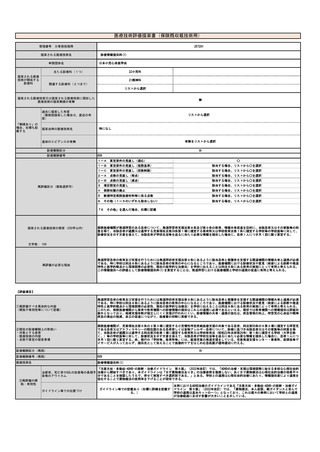
提案書04(0599頁~0801頁)医療技術評価・再評価提案書 (38 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000190899_00011.html |
| 出典情報 | 中央社会保険医療協議会 診療報酬調査専門組織・医療技術評価分科会(令和5年度第1回 11/20)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
拠・有効性
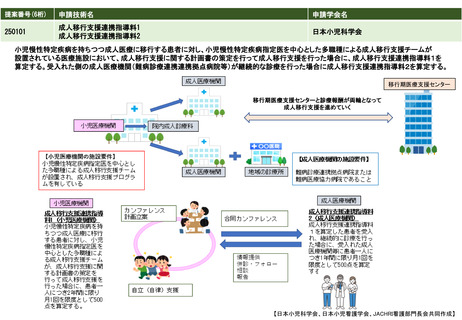
潰瘍性大腸炎及びクローン病は、慢性あるいは寛解・再燃性の腸管の炎症性疾患で、原因不明で複雑な病態を有し、主として腸管を傷害し種々の
臨床症状を呈する。ベドリズマブは、接着因子をターゲットとした新たな作用機序を持つ生物学的製剤で、点滴静注製剤は2018年7月に潰瘍性大
腸炎、2019年5月にクローン病に対し薬事承認された。このベドリズマブは、初回投与後、2週、6週に投与し、以降8週間隔で点滴静注する。
潰瘍性大腸炎患者の治療導入期における国内第Ⅲ相試験(CCT-101試験)では、14週間でコホート1群のベドリズマブ治療群において164例中5例
(3.0%)、海外第Ⅲ相試験(C13006試験)では、6週間でコホート1群のベドリズマブ治療群において225例中6例(2.7%)、コホート2群のベド
治癒率、死亡率やQOLの改善等の長期予 リズマブ治療群において521例中11例(2.1%)にinfusion reactionが認められている(ベドリズマブ審査報告書のp40記載)。治療維持期におけ
後等のアウトカム
る国内第Ⅲ相試験(CCT-101試験)では、60週間でコホートA群のベドリズマブ治療群において41例中0例(0.0%)、海外第Ⅲ相試験(C13006試
験)では、52週間(導入期から維持期までの集計)でコホートA群のベドリズマブ8週間間隔維持治療群において122例中5例(4.1%)にinfusion
reactionが認められている(ベドリズマブ審査報告書のp41記載)。
以上のことから投与患者の注意深い観察と異常が生じた際の迅速な対応が必要である。入院での投与が望まれるが、投与の度、入院するのは患者
にとっても負担であり、より多くの医療費につながる。
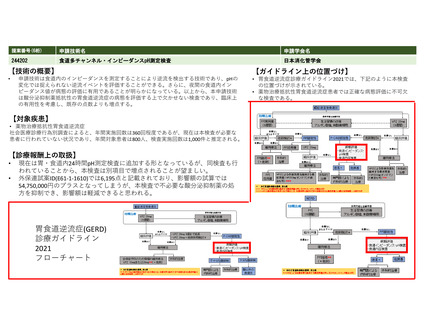
ガイドライン等での位置づけ
④普及性の変化
※下記のように推定した根拠
年間対象者数の
変化
年間実施回数の
変化等
IBD診療ガイドライン(2020年 日本消化器病学会発刊)によれば、ベドリズマブは中等軽
ガイドライン等での記載あり(右欄に詳細を記載す 症~重症の潰瘍性大腸炎のステロイド抵抗性/依存性に対し、他の生物学的製剤と同様に第
る。)
一選択薬、活動期クローン病のステロイド抵抗性/依存性に対し、他の生物学的製剤と同様
に第一選択薬に推奨されている。
再評価によって対象患者数や実施回数は変化しない。
見直し前の症例数(人)
―
見直し後の症例数(人)
―
見直し前の回数(回)
―
見直し後の回数(回)
―
⑤医療技術の成熟度
・学会等における位置づけ
・難易度(専門性等)
炎症性腸疾患の治療に対し、専門性を持つ医師を始め、看護師、薬剤師が必要である。
施設の要件
適応患者は主に消化器内科を受診していると考えられ、これらの科があり、かつ腫瘍関連の科(腫瘍内科など)・血液内科・膠原病内科があるた
(標榜科、手術件数、検査や手術の体 めに既に外来化学療法室を有している施設。
制等)
・施設基準
(技術の専門性
等を踏まえ、必
要と考えられる
要件を、項目毎
に記載するこ
と)
・化学療法の経験を有する専任の常勤看護師が薬剤投与を実施している時間帯において常時当該治療室に勤務していること
人的配置の要件
・化学療法につき専任の常勤薬剤師が勤務していること
(医師、看護師等の職種や人数、専門 ・急変時等の緊急時に当該患者が入院できる体制が確保されていること又は他の保険医療機関との連携により緊急時に当該患者が入院できる体制
性や経験年数等)
が整備されていること
その他
(遵守すべきガイドライン等その他の 特になし
要件)
⑥安全性
・副作用等のリスクの内容と頻度
潰瘍性大腸炎患者の治療導入期における国内第Ⅲ相試験(CCT-101試験)では、14週間でコホート1群のベドリズマブ治療群において164例中5例
(3.0%)、海外第Ⅲ相試験(C13006試験)では、6週間でコホート1群のベドリズマブ治療群において225例中6例(2.7%)、コホート2群のベド
リズマブ治療群において521例中11例(2.1%)にinfusion reactionが認められている(ベドリズマブ審査報告書のp40記載)。治療維持期におけ
る国内第Ⅲ相試験(CCT-101試験)では、60週間でコホートA群のベドリズマブ治療群において41例中0例(0.0%)、海外第Ⅲ相試験(C13006試
験)では、52週間(導入期から維持期までの集計)でコホートA群のベドリズマブ8週間間隔維持治療群において122例中5例(4.1%)にinfusion
reactionが認められている(ベドリズマブ審査報告書のp41記載)。その他副作用については添付文書を参照。
⑦倫理性・社会的妥当性
(問題点があれば必ず記載)
化学療法加算を算定できるようにすることで専門チームで副作用等の管理を十分に実施することができ患者に対してベネフィットとなる。炎症性
腸疾患においては、既に点滴静注であるインフリキシマブについても外来化学療法加算が認められており、妥当であると判断した。
⑧点数等見直し
の場合
見直し前
見直し後
その根拠
加算なし
外来化学療法加算1: ① 15歳未満670点、② 15歳以上450点、又は外来化学療法加算2:① 15歳未満640点、② 15歳以上370点
同効薬で既に加算対象となっているインフリキシマブを参照した。
区分
⑨関連して減点
や削除が可能と
考えられる医療
技術(当該医療
技術を含む)
区分をリストから選択
番号
技術名
―
―
具体的な内容
―
減(-)
プラスマイナス
⑩予想影響額
予想影響額(円)
12,617万円
その根拠
①2022年9月時点のベドリズマブの治療を受けている患者数は約8,500名(潰瘍性大腸炎7,500名、クローン病1,000名)で、このうち、外来化学療
法加算の要件を満たす施設での投与例は約6,000名と推計される。実際に外来化学療法加算を算定する患者数は約80%(インフリキシマブにおけ
る実際の算定割合)の5,000名以下と考えられる。よって、最大で予想される当該技術に係る年間医療費は11,100万円=患者数5,000名×加算370点
×6回/年(8週間隔投与)と考えられる。
②ベドリズマブを潰瘍性大腸炎に対して入院で投与した場合、1日目は10,158点(薬剤費抜き)、2日目は1,745点、クローン病対して入院で投与し
た場合、1日目は7,390点(薬剤費抜き)、2日目は1,740点のDPC点数が算定される。現在、入院で投与されている患者の割合は全体の約4.0%である
ため、これらの患者が1泊2日の入院で投与される場合、最大で年間医療費は27,617万円=潰瘍性大腸炎患者数7,500名×約4.0%×入院費用11,903
点×6回/年(8週間隔投与)+クローン病患者1,000名×約4.0%×入院費用9,130点×6回/年(8週間隔投与)と考えられる。
①ー②=12,617万円
備考
外来化学療法加算の算定できる要件が整っている施設で投与した場合、加算分の医療費増額が予想される。
⑪算定要件の見直し等によって、新たに使用される医薬
品、医療機器又は体外診断薬
特になし
636