よむ、つかう、まなぶ。
07_令和8年度診療報酬改定の概要 7.外来医療の機能分化・強化等 (28 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71068.html |
| 出典情報 | 令和8年度診療報酬改定説明資料等について(3/5)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
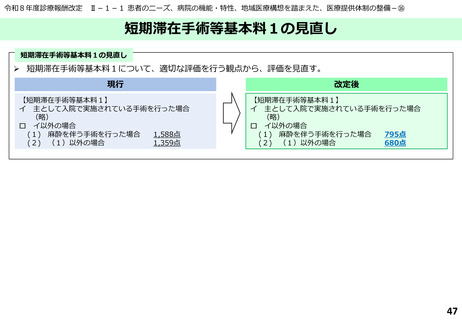
令和8年度診療報酬改定
Ⅳ-1
後発医薬品・バイオ後続品の使用促進-②
バイオ後続品使用体制加算の見直し
バイオ後続品使用体制加算の見直し
➢
➢
➢
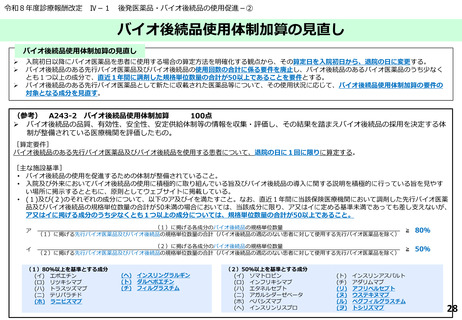
入院初日以降にバイオ医薬品を患者に使用する場合の算定方法を明確化する観点から、その算定日を入院初日から、退院の日に変更する。
バイオ後続品のある先行バイオ医薬品及びバイオ後続品の使用回数の合計に係る要件を廃止し、バイオ後続品のあるバイオ医薬品のうち少なく
とも1つ以上の成分で、直近1年間に調剤した規格単位数量の合計が50以上であることを要件とする。
バイオ後続品のある先行バイオ医薬品として新たに収載された医薬品等について、その使用状況に応じて、バイオ後続品使用体制加算の要件の
対象となる成分を見直す。
(参考) A243-2 バイオ後続品使用体制加算
100点
➢ バイオ後続品の品質、有効性、安全性、安定供給体制等の情報を収集・評価し、その結果を踏まえバイオ後続品の採用を決定する体
制が整備されている医療機関を評価したもの。
[算定要件]
バイオ後続品のある先行バイオ医薬品及びバイオ後続品を使用する患者について、退院の日に1回に限りに算定する。
[主な施設基準]
• バイオ後続品の使用を促進するための体制が整備されていること。
• 入院及び外来においてバイオ後続品の使用に積極的に取り組んでいる旨及びバイオ後続品の導入に関する説明を積極的に行っている旨を見やす
い場所に掲示するとともに、原則としてウェブサイトに掲載している。
• (1)及び(2)のそれぞれの成分について、以下のア及びイを満たすこと。なお、直近1年間に当該保険医療機関において調剤した先行バイオ医薬
品及びバイオ後続品の規格単位数量の合計が50未満の場合においては、当該成分に限り、ア又はイに定める基準未満であっても差し支えないが、
ア又はイに掲げる成分のうち少なくとも1つ以上の成分については、規格単位数量の合計が50以上であること。
ア
(1)に掲げる各成分のバイオ後続品の規格単位数量
(1)に掲げる先行バイオ医薬品及びバイオ後続品の規格単位数量の合計(バイオ後続品の適応のない患者に対して使用する先行バイオ医薬品を除く)
≧
80%
イ
(2)に掲げる各成分のバイオ後続品の規格単位数量
(2)に掲げる先行バイオ医薬品及びバイオ後続品の規格単位数量の合計(バイオ後続品の適応のない患者に対して使用する先行バイオ医薬品を除く)
≧
50%
(1)80%以上を基準とする成分
(イ) エポエチン
(ロ) リツキシマブ
(ハ) トラスツズマブ
(二) テリパラチド
(ホ) ラニビズマブ
(ヘ) インスリングラルギン
(ト) ダルベポエチン
(チ) フィルグラスチム
(2)50%以上を基準とする成分
(イ) ソマトロピン
(ロ) インフリキシマブ
(ハ) エタネルセプト
(二) アガルシダーゼベータ
(ホ) ベバシズマブ
(へ) インスリンリスプロ
(ト)
(チ)
(リ)
(ヌ)
(ル)
(ヲ)
インスリンアスパルト
アダリムマブ
アフリベルセプト
ウステキヌマブ
ペグフィルグラスチム
トシリズマブ
28
Ⅳ-1
後発医薬品・バイオ後続品の使用促進-②
バイオ後続品使用体制加算の見直し
バイオ後続品使用体制加算の見直し
➢
➢
➢
入院初日以降にバイオ医薬品を患者に使用する場合の算定方法を明確化する観点から、その算定日を入院初日から、退院の日に変更する。
バイオ後続品のある先行バイオ医薬品及びバイオ後続品の使用回数の合計に係る要件を廃止し、バイオ後続品のあるバイオ医薬品のうち少なく
とも1つ以上の成分で、直近1年間に調剤した規格単位数量の合計が50以上であることを要件とする。
バイオ後続品のある先行バイオ医薬品として新たに収載された医薬品等について、その使用状況に応じて、バイオ後続品使用体制加算の要件の
対象となる成分を見直す。
(参考) A243-2 バイオ後続品使用体制加算
100点
➢ バイオ後続品の品質、有効性、安全性、安定供給体制等の情報を収集・評価し、その結果を踏まえバイオ後続品の採用を決定する体
制が整備されている医療機関を評価したもの。
[算定要件]
バイオ後続品のある先行バイオ医薬品及びバイオ後続品を使用する患者について、退院の日に1回に限りに算定する。
[主な施設基準]
• バイオ後続品の使用を促進するための体制が整備されていること。
• 入院及び外来においてバイオ後続品の使用に積極的に取り組んでいる旨及びバイオ後続品の導入に関する説明を積極的に行っている旨を見やす
い場所に掲示するとともに、原則としてウェブサイトに掲載している。
• (1)及び(2)のそれぞれの成分について、以下のア及びイを満たすこと。なお、直近1年間に当該保険医療機関において調剤した先行バイオ医薬
品及びバイオ後続品の規格単位数量の合計が50未満の場合においては、当該成分に限り、ア又はイに定める基準未満であっても差し支えないが、
ア又はイに掲げる成分のうち少なくとも1つ以上の成分については、規格単位数量の合計が50以上であること。
ア
(1)に掲げる各成分のバイオ後続品の規格単位数量
(1)に掲げる先行バイオ医薬品及びバイオ後続品の規格単位数量の合計(バイオ後続品の適応のない患者に対して使用する先行バイオ医薬品を除く)
≧
80%
イ
(2)に掲げる各成分のバイオ後続品の規格単位数量
(2)に掲げる先行バイオ医薬品及びバイオ後続品の規格単位数量の合計(バイオ後続品の適応のない患者に対して使用する先行バイオ医薬品を除く)
≧
50%
(1)80%以上を基準とする成分
(イ) エポエチン
(ロ) リツキシマブ
(ハ) トラスツズマブ
(二) テリパラチド
(ホ) ラニビズマブ
(ヘ) インスリングラルギン
(ト) ダルベポエチン
(チ) フィルグラスチム
(2)50%以上を基準とする成分
(イ) ソマトロピン
(ロ) インフリキシマブ
(ハ) エタネルセプト
(二) アガルシダーゼベータ
(ホ) ベバシズマブ
(へ) インスリンリスプロ
(ト)
(チ)
(リ)
(ヌ)
(ル)
(ヲ)
インスリンアスパルト
アダリムマブ
アフリベルセプト
ウステキヌマブ
ペグフィルグラスチム
トシリズマブ
28