よむ、つかう、まなぶ。
(別紙2)[2.5MB] (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00174.html |
| 出典情報 | 先進医療会議(第153回 4/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
先進医療審査の事前照会事項に対する回答1
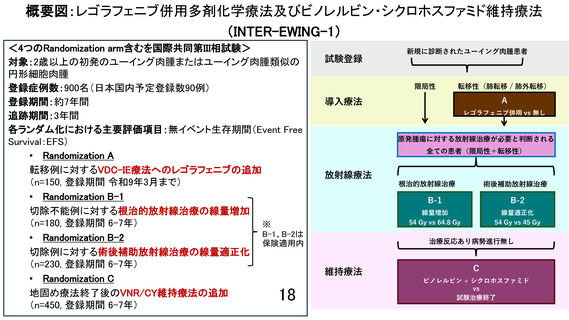
先進医療技術名:レゴラフェニブ併用多剤化学療法及びビノレルビン・シクロホスファミド維持療法
2026 年 1 月 23 日
所属・氏名:国立がん研究センター中央病院 岩田 慎太郎
1.基本的な確認で申し訳ございませんが、先進医療実施届出書様式3号2-1にはスチバーガ錠 40
mgについて、「医薬品医療機器法承認又は認証番号」は「なし」と記載されています。しかし、翻訳
剤は PMDA 承認済みであり、承認番号 22500AMX00886000 となっています。
今回用いられる薬剤は承認済みのスチバーガとは異なる薬剤ということでしょうか。
【回答】
本試験で用いるスチバーガ錠は Bayer AG(本社)から無償で提供される治験薬で本邦では薬事承認さ
れおりませんので、認証番号はございませんが、有効成分は本邦で承認されているスチバーガ錠 40mg
と同一です。
2.先進医療実施届出書には「特に、本試験に含まれるレゴラフェニブやビノレルビン(維持療法)は、
既存治療に対する上乗せ効果が期待されており、有効性が示されれば、希少がんである小児肉腫
に対する公知申請、条件付き承認制度、もしくは適応追加を通じた保険収載が強く望まれる。」と記
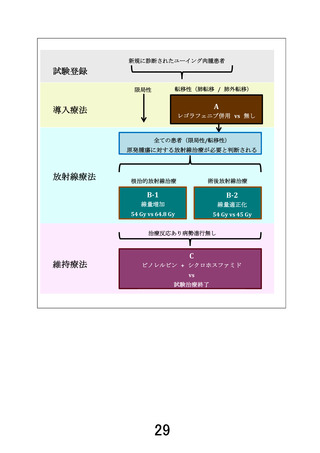
載があり、ロードマップでもこの記載と矛盾しない内容が記載されていますが、本先進医療で使用さ
れる医薬品の適応拡大について、ドラッグロスやラグを回避する観点から、現時点での製造販売企
業側の考えについても分かる範囲でご教示いただけますでしょうか。
【回答】
本試験の結果が得られるのは5年以上先となる見込みであることから、現時点で日本の支社と薬事承
認に向けた具体的な方策について合意に至っておりません。しかし、本試験の結果、本併用療法が期待
通りの有効性を示した場合は、未承認薬・適応外薬等検討会議へ要望書を提出した上での公知申請な
ど、適切な方法で薬事承認を目指す方針であることは日本支社に相談し、了承を得られています。
以上
1
5
先進医療技術名:レゴラフェニブ併用多剤化学療法及びビノレルビン・シクロホスファミド維持療法
2026 年 1 月 23 日
所属・氏名:国立がん研究センター中央病院 岩田 慎太郎
1.基本的な確認で申し訳ございませんが、先進医療実施届出書様式3号2-1にはスチバーガ錠 40
mgについて、「医薬品医療機器法承認又は認証番号」は「なし」と記載されています。しかし、翻訳
剤は PMDA 承認済みであり、承認番号 22500AMX00886000 となっています。
今回用いられる薬剤は承認済みのスチバーガとは異なる薬剤ということでしょうか。
【回答】
本試験で用いるスチバーガ錠は Bayer AG(本社)から無償で提供される治験薬で本邦では薬事承認さ
れおりませんので、認証番号はございませんが、有効成分は本邦で承認されているスチバーガ錠 40mg
と同一です。
2.先進医療実施届出書には「特に、本試験に含まれるレゴラフェニブやビノレルビン(維持療法)は、
既存治療に対する上乗せ効果が期待されており、有効性が示されれば、希少がんである小児肉腫
に対する公知申請、条件付き承認制度、もしくは適応追加を通じた保険収載が強く望まれる。」と記
載があり、ロードマップでもこの記載と矛盾しない内容が記載されていますが、本先進医療で使用さ
れる医薬品の適応拡大について、ドラッグロスやラグを回避する観点から、現時点での製造販売企
業側の考えについても分かる範囲でご教示いただけますでしょうか。
【回答】
本試験の結果が得られるのは5年以上先となる見込みであることから、現時点で日本の支社と薬事承
認に向けた具体的な方策について合意に至っておりません。しかし、本試験の結果、本併用療法が期待
通りの有効性を示した場合は、未承認薬・適応外薬等検討会議へ要望書を提出した上での公知申請な
ど、適切な方法で薬事承認を目指す方針であることは日本支社に相談し、了承を得られています。
以上
1
5