よむ、つかう、まなぶ。
(別紙2)[2.5MB] (19 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00174.html |
| 出典情報 | 先進医療会議(第153回 4/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
薬事承認申請までのロードマップ
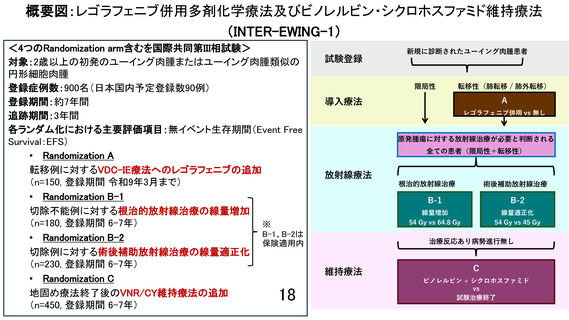
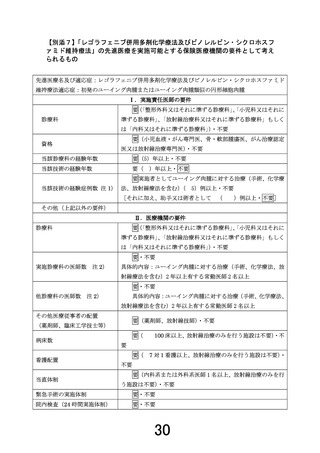
先進医療技術名:レゴラフェニブ併用多剤化学療法及びビノレルビン・シクロホスファミド維持療法
適応症:初発ユーイング肉腫またはユーイング肉腫類似の円形細胞肉腫
先進医療
臨床研究(海外で実施)
試験名:REGO-INTER-EWING-1
試験デザイン:VDC-IE療法との併用におけるレゴラフェニブのRP2D
を決定する第Ib相試験
期間:2023年1月~2025年1月
被験者数:24名
結果の概要:本試験では、レゴラフェニブを標準化学療法(VDC/IE)
に併用した新規発症多発転移型Ewing肉腫患者において、82 mg/m²/
日が最大耐用量として確認され、許容可能な安全性が示された。本
併用療法の有効性は、Inter-Ewing-1試験にて検証予定。また、海外
では、レゴラフェニブ単剤の肉腫に対する有効性を評価する第II相試
験が2試験実施され、ユーイング肉腫に対して一定の抗腫瘍効果が
示された。
国内ではレゴラフェニブ+VDC-IE療法の併用療法の臨床試験は実施
されていない。
試験名:RMS2005試験
試験デザイン:初発横紋筋肉腫に対するリスク層別化に基づく治療
最適化のための国際多施設共同臨床試験
期間:2005年10月~2016年12月
被験者数:1733名(うち維持療法ランダム化登録数は371名)
結果の概要:本試験において、VNR/CY併用維持療法の有効性を評
価する第III相ランダム化試験が行われ、小児を含む182名の転移の
ない横紋筋肉腫患者を対象にVNR/CY維持療法を実施有効性と安
全性が示され、横紋筋肉腫に対する標準治療として確立された。
国内ではVNR/CY療法の臨床試験は実施されていない。
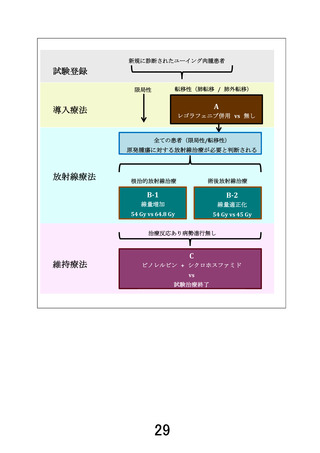
試験名:レゴラフェニブ併用多剤化学療法及びビノレルビ
ン・シクロホスファミド維持療法(INTER-EWING-1)
試験デザイン:国際共同 無作為化 第Ⅲ相試験(4つのラ
ンダム化を組み込み)
期間:2026年2月開始予定~ 2037年12月31日(欧州では、
2021年12月開始)
【Randomisation A】
対象:転移性ユーイング肉腫またはユーイング肉腫類似
の円形細胞肉腫
内容:VDC/IE + レゴラフェニブ vs VDC/IE※1
海外登録数:150例
国内:登録予定数:20例
主要評価項目:無イベント生存期間(EFS)
副次評価項目:全生存期間(OS)、毒性、QoL、組織学的
効果判定(手術を行った場合)
初発ユーイング肉腫に対する
国際的新規標準治療として確立
本先進医療のデータを利活用し
公知申請などを検討
薬事承認申請
【Randomisation C】
対象:強化療法後のユーイング肉腫またはユーイング肉
腫類似の円形細胞肉腫
内容:維持療法(VNR + CY)追加 vs 非追加 ※2
海外登録数:450例
国内登録予定数:40例
主要評価項目:EFS
副次評価項目:OS、毒性、QoL
主な適格規準
1. 試験参加のおよびランダム化ための適格規準を満たしている
2. (RandomisationAのみ)転移性病変がある(肺もしくは胸膜のみの転移を含む)
3. (RandomisationCのみ)VDC/IE/VC/VAI/BuMelベースのレジメンによる寛解導入/
地固め化学療法を受けている
4. 患者または親・法定後見人からの書面によるインフォームド・コンセントを得ている
主な除外規準
1. (RandomisationAのみ)限局性腫瘍である
2. (RandomisationCのみ)R2切除後(肉眼的腫瘍遺残)
予想される有害事象
好中球減少、貧血、血小板減少、下痢、発疹、発声障害、口内炎、悪心、粘膜炎 etc.
試験薬;レゴラフェニブおよびビノレルビン
本邦での現状
ガイドライン記載:(無) 進行中の臨床試験(無)
海外での現状
保険適用:米国(無)、英国(無)、フランス(無)、ドイツ(無)、カナダ(無)、オーストラリア
(無)、その他(無)
ガイドライン記載:(無)
進行中の臨床試験(有)
• INTER-EWING-1試験が既に欧州と豪で開始している
• 現在REGO-INTER-EWING-1試験が欧州で終了し、VDC-IE療法との併用における
レゴラフェニブのRP2Dが決定。
19
※1. VDC/IE:ビンクリスチン+ドキソルビシン+シクロホスファミド/イホマイド+エトポシド
※2. VNR + CY:ビノレルビン+エンドキサン
先進医療技術名:レゴラフェニブ併用多剤化学療法及びビノレルビン・シクロホスファミド維持療法
適応症:初発ユーイング肉腫またはユーイング肉腫類似の円形細胞肉腫
先進医療
臨床研究(海外で実施)
試験名:REGO-INTER-EWING-1
試験デザイン:VDC-IE療法との併用におけるレゴラフェニブのRP2D
を決定する第Ib相試験
期間:2023年1月~2025年1月
被験者数:24名
結果の概要:本試験では、レゴラフェニブを標準化学療法(VDC/IE)
に併用した新規発症多発転移型Ewing肉腫患者において、82 mg/m²/
日が最大耐用量として確認され、許容可能な安全性が示された。本
併用療法の有効性は、Inter-Ewing-1試験にて検証予定。また、海外
では、レゴラフェニブ単剤の肉腫に対する有効性を評価する第II相試
験が2試験実施され、ユーイング肉腫に対して一定の抗腫瘍効果が
示された。
国内ではレゴラフェニブ+VDC-IE療法の併用療法の臨床試験は実施
されていない。
試験名:RMS2005試験
試験デザイン:初発横紋筋肉腫に対するリスク層別化に基づく治療
最適化のための国際多施設共同臨床試験
期間:2005年10月~2016年12月
被験者数:1733名(うち維持療法ランダム化登録数は371名)
結果の概要:本試験において、VNR/CY併用維持療法の有効性を評
価する第III相ランダム化試験が行われ、小児を含む182名の転移の
ない横紋筋肉腫患者を対象にVNR/CY維持療法を実施有効性と安
全性が示され、横紋筋肉腫に対する標準治療として確立された。
国内ではVNR/CY療法の臨床試験は実施されていない。
試験名:レゴラフェニブ併用多剤化学療法及びビノレルビ
ン・シクロホスファミド維持療法(INTER-EWING-1)
試験デザイン:国際共同 無作為化 第Ⅲ相試験(4つのラ
ンダム化を組み込み)
期間:2026年2月開始予定~ 2037年12月31日(欧州では、
2021年12月開始)
【Randomisation A】
対象:転移性ユーイング肉腫またはユーイング肉腫類似
の円形細胞肉腫
内容:VDC/IE + レゴラフェニブ vs VDC/IE※1
海外登録数:150例
国内:登録予定数:20例
主要評価項目:無イベント生存期間(EFS)
副次評価項目:全生存期間(OS)、毒性、QoL、組織学的
効果判定(手術を行った場合)
初発ユーイング肉腫に対する
国際的新規標準治療として確立
本先進医療のデータを利活用し
公知申請などを検討
薬事承認申請
【Randomisation C】
対象:強化療法後のユーイング肉腫またはユーイング肉
腫類似の円形細胞肉腫
内容:維持療法(VNR + CY)追加 vs 非追加 ※2
海外登録数:450例
国内登録予定数:40例
主要評価項目:EFS
副次評価項目:OS、毒性、QoL
主な適格規準
1. 試験参加のおよびランダム化ための適格規準を満たしている
2. (RandomisationAのみ)転移性病変がある(肺もしくは胸膜のみの転移を含む)
3. (RandomisationCのみ)VDC/IE/VC/VAI/BuMelベースのレジメンによる寛解導入/
地固め化学療法を受けている
4. 患者または親・法定後見人からの書面によるインフォームド・コンセントを得ている
主な除外規準
1. (RandomisationAのみ)限局性腫瘍である
2. (RandomisationCのみ)R2切除後(肉眼的腫瘍遺残)
予想される有害事象
好中球減少、貧血、血小板減少、下痢、発疹、発声障害、口内炎、悪心、粘膜炎 etc.
試験薬;レゴラフェニブおよびビノレルビン
本邦での現状
ガイドライン記載:(無) 進行中の臨床試験(無)
海外での現状
保険適用:米国(無)、英国(無)、フランス(無)、ドイツ(無)、カナダ(無)、オーストラリア
(無)、その他(無)
ガイドライン記載:(無)
進行中の臨床試験(有)
• INTER-EWING-1試験が既に欧州と豪で開始している
• 現在REGO-INTER-EWING-1試験が欧州で終了し、VDC-IE療法との併用における
レゴラフェニブのRP2Dが決定。
19
※1. VDC/IE:ビンクリスチン+ドキソルビシン+シクロホスファミド/イホマイド+エトポシド
※2. VNR + CY:ビノレルビン+エンドキサン