よむ、つかう、まなぶ。
(別紙2)[2.5MB] (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00174.html |
| 出典情報 | 先進医療会議(第153回 4/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
8.
妊娠する可能性のある女性、または妊娠させる可能性のある男性の場合には、治療中お
よび最後の試験治療後12ヵ月間(女性)、または最後の試験治療後6ヵ月間(男性)の
避妊に同意する
9.
患患者または親・法定後見人からの書面によるインフォームド・コンセントを得ている
除外基準
1.
R2切除後(肉眼的腫瘍遺残)
2.
四肢原発で、広範切除(R0かつ化学療法前の腫瘍範囲が完全に切除されている)が達成
されており、かつ組織学的効果判定が良好(viable cellが10%未満)で腫瘍体積が小
さい(診断時200mL未満)
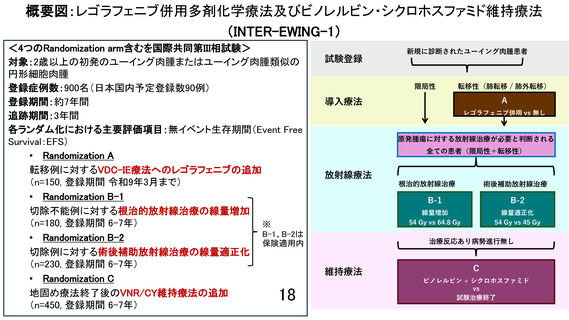
選定方法
対象患者が本試験の試験参加のための適格基準をすべて満たし、除外基準に該当しないことを
各試験実施施設において確認したうえで、患者本人または親・法定代理人に対して試験の目的、
方法、予想される効果およびリスク等を十分に説明し、文書による同意を取得する。同意取得
後、各施設は適格性チェックリストを作成し、国立がん研究センター(NCC)による確認を経て、
英国コーディネートセンター(CRCTU)が当該施設を試験参加施設として有効化した時点で、オ
ンラインデータ入力システム(eRDC)を用いて試験登録(Study Entry)を行う。試験登録時に
患者には固有の試験番号(TNO)が付与され、以降のすべての Randomisation において同一番号
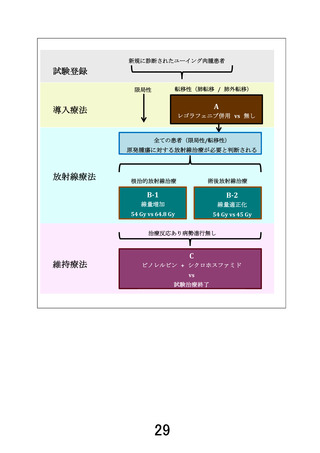
を用いる。各 Randomisation は、プロトコールに定められたタイミング(導入療法終了後、局所
療法終了後、維持療法開始時など)で参加する Randomisation の適格規準をすべて満たし、除
外基準に該当しないことを確認した上で実施され、1:1 の比率で治療群が自動割付される。すべ
ての登録および割付結果は eRDC 上で確認・印刷し、ISF(Investigator’s site file)および
カルテに保存する。なお、各 Randomisation は独立しており、前段階の Randomisation への参
加は後続 Randomisation への参加要件とはならない。
24
妊娠する可能性のある女性、または妊娠させる可能性のある男性の場合には、治療中お
よび最後の試験治療後12ヵ月間(女性)、または最後の試験治療後6ヵ月間(男性)の
避妊に同意する
9.
患患者または親・法定後見人からの書面によるインフォームド・コンセントを得ている
除外基準
1.
R2切除後(肉眼的腫瘍遺残)
2.
四肢原発で、広範切除(R0かつ化学療法前の腫瘍範囲が完全に切除されている)が達成
されており、かつ組織学的効果判定が良好(viable cellが10%未満)で腫瘍体積が小
さい(診断時200mL未満)
選定方法
対象患者が本試験の試験参加のための適格基準をすべて満たし、除外基準に該当しないことを
各試験実施施設において確認したうえで、患者本人または親・法定代理人に対して試験の目的、
方法、予想される効果およびリスク等を十分に説明し、文書による同意を取得する。同意取得
後、各施設は適格性チェックリストを作成し、国立がん研究センター(NCC)による確認を経て、
英国コーディネートセンター(CRCTU)が当該施設を試験参加施設として有効化した時点で、オ
ンラインデータ入力システム(eRDC)を用いて試験登録(Study Entry)を行う。試験登録時に
患者には固有の試験番号(TNO)が付与され、以降のすべての Randomisation において同一番号
を用いる。各 Randomisation は、プロトコールに定められたタイミング(導入療法終了後、局所
療法終了後、維持療法開始時など)で参加する Randomisation の適格規準をすべて満たし、除
外基準に該当しないことを確認した上で実施され、1:1 の比率で治療群が自動割付される。すべ
ての登録および割付結果は eRDC 上で確認・印刷し、ISF(Investigator’s site file)および
カルテに保存する。なお、各 Randomisation は独立しており、前段階の Randomisation への参
加は後続 Randomisation への参加要件とはならない。
24