よむ、つかう、まなぶ。
20_令和8年度保険医療材料制度改革の概要 (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71068.html |
| 出典情報 | 令和8年度診療報酬改定説明資料等について(3/5)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
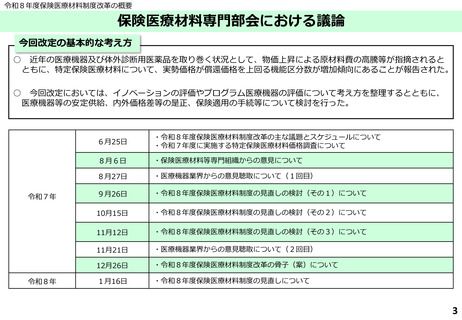
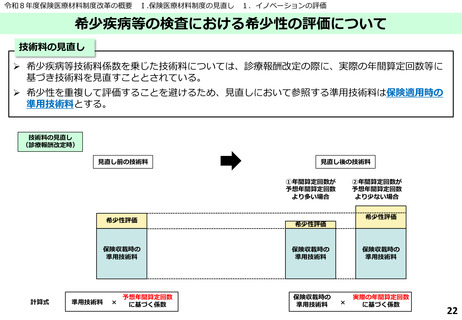
令和8年度保険医療材料制度改革の概要
Ⅰ.保険医療材料制度の見直し 1.イノベーションの評価
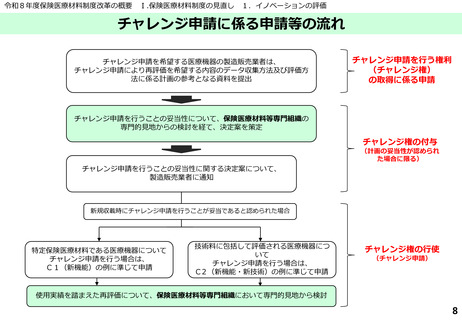
使用実績を踏まえた再評価に係る申請(チャレンジ申請)
使用実績を踏まえた評価が必要な製品に対する対応
➢ チャレンジ申請による再評価の対象は、チャレンジ申請を行うことが妥当であると判断された(以
下チャレンジ申請を行う権利を「チャレンジ権」という。)後に製造販売業者が関与の上で収集し
たデータ(チャレンジ権の取得時点ですでに収集を開始しているものも含む。)に基づき、査読付
き論文として公表されたものに限られ、独自の解析等は対象とならないことを明確化する。
➢ 評価方法に係る計画については、原則として比較試験を求める。比較試験の実施が困難な場合には、
バイアスのリスクを軽減する方法等を十分に検討した研究計画を示すこと。
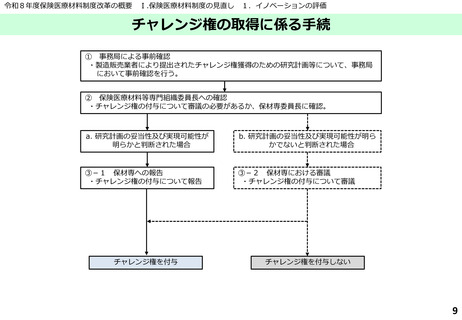
➢ 既存治療との比較等により新たな知見を得られることが十分に期待でき、実現可能性も高いと考え
られる計画については、事務局による事前確認を経て保険医療材料等専門組織委員長が認めた場合
に限り、保険医療材料等専門組織への報告をもってチャレンジ権を付与できる。
➢ 保険医療材料等専門組織での審議において、既存治療との比較が困難と判断されるものや実現可能
性が認められないもの等については、チャレンジ権を付与しないこととし、製造販売業者にその理
由を伝達することとする。
7
Ⅰ.保険医療材料制度の見直し 1.イノベーションの評価
使用実績を踏まえた再評価に係る申請(チャレンジ申請)
使用実績を踏まえた評価が必要な製品に対する対応
➢ チャレンジ申請による再評価の対象は、チャレンジ申請を行うことが妥当であると判断された(以
下チャレンジ申請を行う権利を「チャレンジ権」という。)後に製造販売業者が関与の上で収集し
たデータ(チャレンジ権の取得時点ですでに収集を開始しているものも含む。)に基づき、査読付
き論文として公表されたものに限られ、独自の解析等は対象とならないことを明確化する。
➢ 評価方法に係る計画については、原則として比較試験を求める。比較試験の実施が困難な場合には、
バイアスのリスクを軽減する方法等を十分に検討した研究計画を示すこと。
➢ 既存治療との比較等により新たな知見を得られることが十分に期待でき、実現可能性も高いと考え
られる計画については、事務局による事前確認を経て保険医療材料等専門組織委員長が認めた場合
に限り、保険医療材料等専門組織への報告をもってチャレンジ権を付与できる。
➢ 保険医療材料等専門組織での審議において、既存治療との比較が困難と判断されるものや実現可能
性が認められないもの等については、チャレンジ権を付与しないこととし、製造販売業者にその理
由を伝達することとする。
7