よむ、つかう、まなぶ。
20_令和8年度保険医療材料制度改革の概要 (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71068.html |
| 出典情報 | 令和8年度診療報酬改定説明資料等について(3/5)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
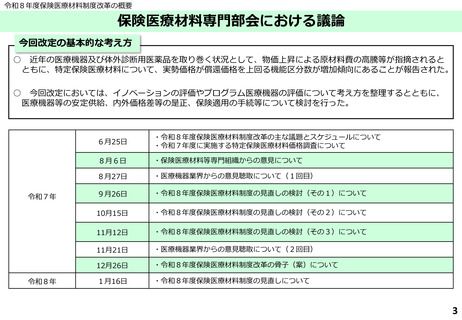
令和8年度保険医療材料制度改革の概要
Ⅰ.保険医療材料制度の見直し 1.イノベーションの評価
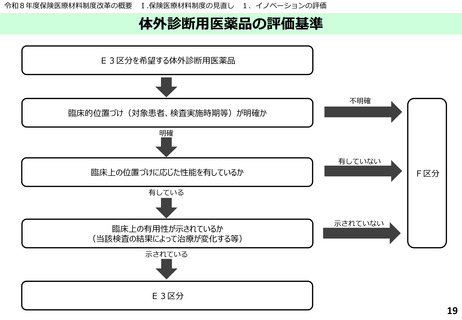
体外診断用医薬品の評価基準
体外診断用医薬品の保険適用における評価基準の明確化
➢ 新たに保険適用希望のある体外診断用医薬品について、療養担当規則の趣旨を踏まえ、臨床上の
必要性を踏まえた評価を行う。
➢ 区分E3(新項目、改良項目)として保険適用を希望する体外診断用医薬品について、以下の①か
ら③に該当する場合は、区分F(保険診療上の有用性に関し、明確な立証があったと認められない
もの)として、保険適用しない。
① 臨床上の位置づけ(対象患者、実施時期)が不明確である場合
② 臨床上の位置づけに応じた性能を有していない場合
③ 当該検査の結果により治療が変化する等の臨床上の有用性が示されていない場合
(参考)体外診断用医薬品の保険適用上の区分
E1(既存項目)
測定項目、測定方法とも既存の品目
E2(既存項目・変更あり)
測定項目は新しくないが測定方法等が新しい品目で、E3(新項目、改良項目)
に該当しないもの
E3(新項目、改良項目)
測定項目が新しい品目又は技術改良等により臨床的意義、利便性の向上等を伴う
既存測定項目
F
保険診療上の有用性に関し、明確な立証があったと認められないもの
18
Ⅰ.保険医療材料制度の見直し 1.イノベーションの評価
体外診断用医薬品の評価基準
体外診断用医薬品の保険適用における評価基準の明確化
➢ 新たに保険適用希望のある体外診断用医薬品について、療養担当規則の趣旨を踏まえ、臨床上の
必要性を踏まえた評価を行う。
➢ 区分E3(新項目、改良項目)として保険適用を希望する体外診断用医薬品について、以下の①か
ら③に該当する場合は、区分F(保険診療上の有用性に関し、明確な立証があったと認められない
もの)として、保険適用しない。
① 臨床上の位置づけ(対象患者、実施時期)が不明確である場合
② 臨床上の位置づけに応じた性能を有していない場合
③ 当該検査の結果により治療が変化する等の臨床上の有用性が示されていない場合
(参考)体外診断用医薬品の保険適用上の区分
E1(既存項目)
測定項目、測定方法とも既存の品目
E2(既存項目・変更あり)
測定項目は新しくないが測定方法等が新しい品目で、E3(新項目、改良項目)
に該当しないもの
E3(新項目、改良項目)
測定項目が新しい品目又は技術改良等により臨床的意義、利便性の向上等を伴う
既存測定項目
F
保険診療上の有用性に関し、明確な立証があったと認められないもの
18