よむ、つかう、まなぶ。
材-2医療機器・医療技術 (34 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62378.html |
| 出典情報 | 中央社会保険医療協議会 保険医療材料専門部会(第130回 8/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(参考資料2)
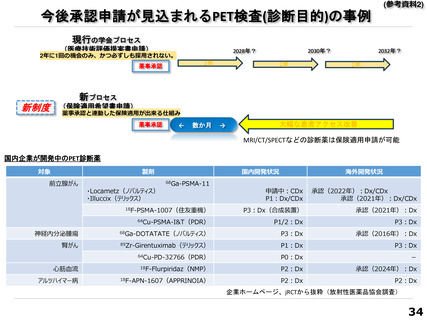
今後承認申請が見込まれるPET検査(診断目的)の事例
現行の学会プロセス
(医療技術評価提案書申請)
2年
薬事承認
新制度
2030年?
2028年?
2年に1回の機会のみ、かつ必ずしも採用されない。
2年
2032年?
2年
新プロセス
(保険適用希望書申請)
薬事承認と連動した保険適用が出来る仕組み
薬事承認
←
数か月
大幅な患者アクセス改善
→
MRI/CT/SPECTなどの診断薬は保険適用申請が可能
国内企業が開発中のPET診断薬
対象
製剤
前立腺がん
国内開発状況
海外開発状況
68Ga-PSMA-11
・Locametz(ノバルティス)
・Illuccix(テリックス)
申請中:CDx
P1:Dx/CDx
承認(2022年):Dx/CDx
承認(2021年):Dx/CDx
18F-PSMA-1007(住友重機)
P3:Dx(合成装置)
承認(2021年):Dx
64Cu-PSMA-I&T(PDR)
P1/2:Dx
P3:Dx
神経内分泌腫瘍
68Ga-DOTATATE(ノバルティス)
P3:Dx
承認(2016年):Dx
腎がん
89Zr-Girentuximab(テリックス)
P1:Dx
P3:Dx
64Cu-PD-32766(PDR)
P0:Dx
-
心筋血流
18F-Flurpiridaz(NMP)
P2:Dx
承認(2024年):Dx
アルツハイマー病
18F-APN-1607(APPRINOIA)
P2:Dx
P2:Dx
企業ホームページ、jRCTから抜粋(放射性医薬品協会調査)
34
今後承認申請が見込まれるPET検査(診断目的)の事例
現行の学会プロセス
(医療技術評価提案書申請)
2年
薬事承認
新制度
2030年?
2028年?
2年に1回の機会のみ、かつ必ずしも採用されない。
2年
2032年?
2年
新プロセス
(保険適用希望書申請)
薬事承認と連動した保険適用が出来る仕組み
薬事承認
←
数か月
大幅な患者アクセス改善
→
MRI/CT/SPECTなどの診断薬は保険適用申請が可能
国内企業が開発中のPET診断薬
対象
製剤
前立腺がん
国内開発状況
海外開発状況
68Ga-PSMA-11
・Locametz(ノバルティス)
・Illuccix(テリックス)
申請中:CDx
P1:Dx/CDx
承認(2022年):Dx/CDx
承認(2021年):Dx/CDx
18F-PSMA-1007(住友重機)
P3:Dx(合成装置)
承認(2021年):Dx
64Cu-PSMA-I&T(PDR)
P1/2:Dx
P3:Dx
神経内分泌腫瘍
68Ga-DOTATATE(ノバルティス)
P3:Dx
承認(2016年):Dx
腎がん
89Zr-Girentuximab(テリックス)
P1:Dx
P3:Dx
64Cu-PD-32766(PDR)
P0:Dx
-
心筋血流
18F-Flurpiridaz(NMP)
P2:Dx
承認(2024年):Dx
アルツハイマー病
18F-APN-1607(APPRINOIA)
P2:Dx
P2:Dx
企業ホームページ、jRCTから抜粋(放射性医薬品協会調査)
34