よむ、つかう、まなぶ。
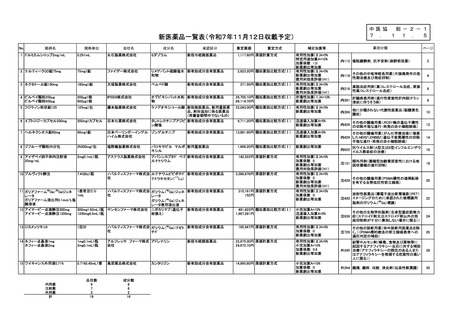
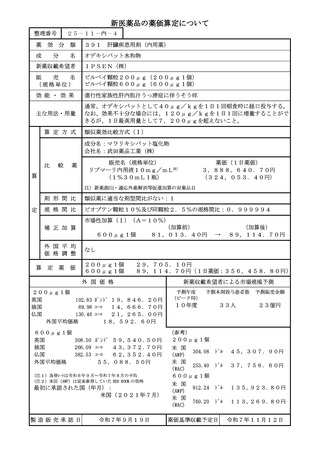
総-2-1医薬品の新規薬価収載等について (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_65606.html |
| 出典情報 | 中央社会保険医療協議会 総会(第624回 11/5)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
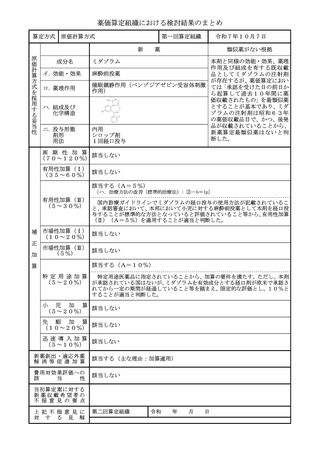
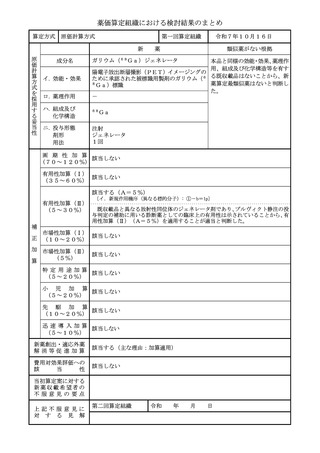
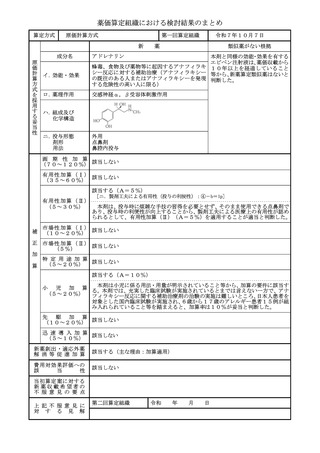
薬価算定組織における検討結果のまとめ
算定方式
類似薬効比較方式(Ⅰ)
第一回算定組織
新
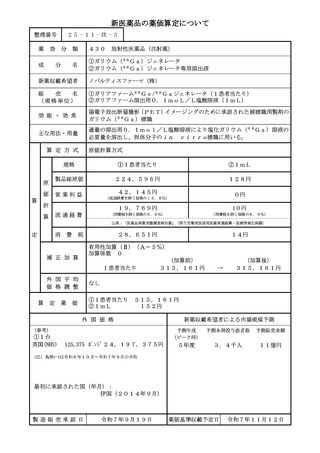
成分名
イ.効能・効果
最
類
似
薬 ロ.薬理作用
選
定
の
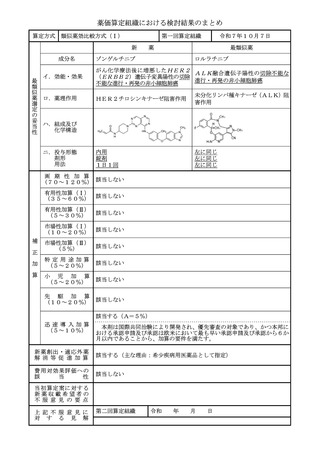
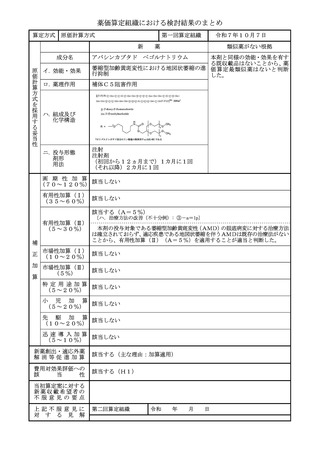
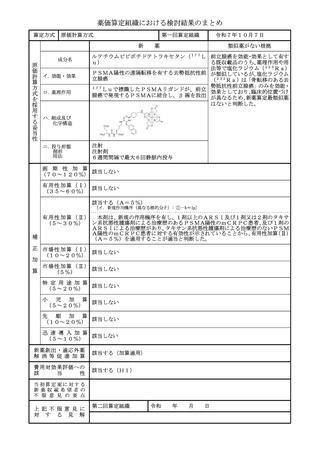
妥 ハ.組成及び
当
化学構造
性
令和7年10月7日
薬
最類似薬
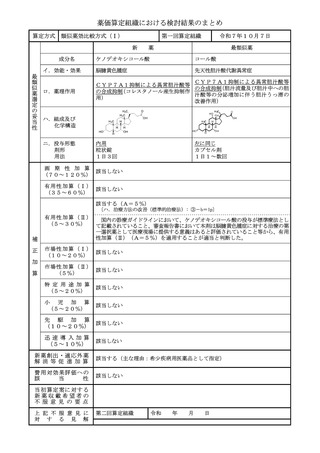
ケノデオキシコール酸
コール酸
脳腱黄色腫症
先天性胆汁酸代謝異常症
CYP7A1抑制による異常胆汁酸等
CYP7A1抑制による異常胆汁酸等
の合成抑制(胆汁流量及び胆汁中への胆
の合成抑制(コレスタノール産生抑制作
汁酸等の分泌増加に伴う胆汁うっ滞の
用)
改善作用)
ニ.投与形態
剤形
用法
内用
粒状錠
1日3回
画 期 性 加 算
(70~120%)
該当しない
左に同じ
カプセル剤
1日1~数回
有用性 加算(Ⅰ)
該当しない
(35~60%)
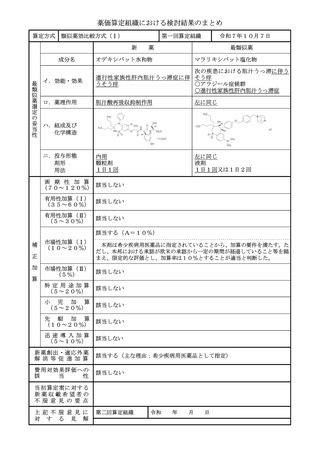
該当する(A=5%)
〔ハ.治療方法の改善(標準的治療法): ③-b=1p〕
補
正
加
算
有用性 加算(Ⅱ)
国内の診療ガイドラインにおいて、ケノデオキシコール酸の投与が標準療法とし
(5~30%)
て記載されていること、審査報告書において本剤は脳腱黄色腫症に対する治療の第
一選択薬として医療現場に提供する意義はあると評価されていること等から、有用
性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
市場性 加算(Ⅰ)
該当しない
(10~20%)
市場性 加算(Ⅱ)
該当しない
(5%)
特 定 用 途 加 算
(5~20%)
小
該当しない
児 加 算
(5~20%)
該当しない
先 駆 加 算
(10~20%)
該当しない
迅速 導 入加算
(5~10%)
該当しない
新薬創出・適応外薬
解 消 等 促 進 加 算
該当する(主な理由:希少疾病用医薬品として指定)
費用対効果評価への
該
当
性
該当しない
当初算定案に対する
新薬収載希望者の
不 服 意 見 の 要 点
上 記 不 服 意 見 に
対 す る 見 解
第二回算定組織
令和
11
年
月
日
算定方式
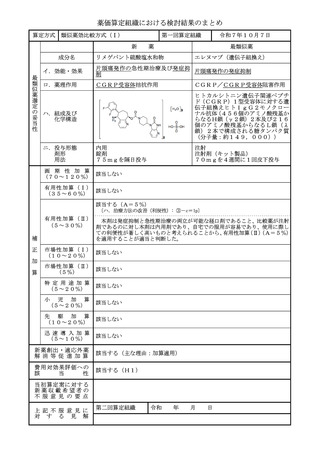
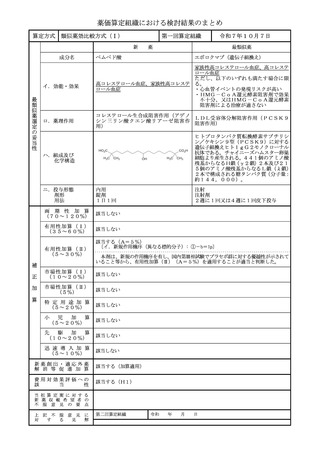
類似薬効比較方式(Ⅰ)
第一回算定組織
新
成分名
イ.効能・効果
最
類
似
薬 ロ.薬理作用
選
定
の
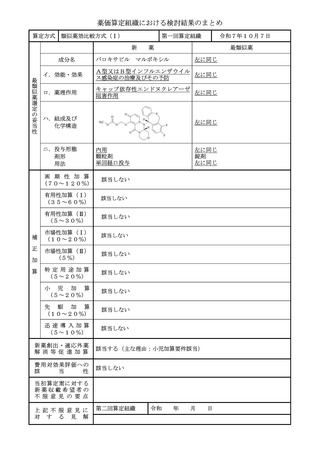
妥 ハ.組成及び
当
化学構造
性
令和7年10月7日
薬
最類似薬
ケノデオキシコール酸
コール酸
脳腱黄色腫症
先天性胆汁酸代謝異常症
CYP7A1抑制による異常胆汁酸等
CYP7A1抑制による異常胆汁酸等
の合成抑制(胆汁流量及び胆汁中への胆
の合成抑制(コレスタノール産生抑制作
汁酸等の分泌増加に伴う胆汁うっ滞の
用)
改善作用)
ニ.投与形態
剤形
用法
内用
粒状錠
1日3回
画 期 性 加 算
(70~120%)
該当しない
左に同じ
カプセル剤
1日1~数回
有用性 加算(Ⅰ)
該当しない
(35~60%)
該当する(A=5%)
〔ハ.治療方法の改善(標準的治療法): ③-b=1p〕
補
正
加
算
有用性 加算(Ⅱ)
国内の診療ガイドラインにおいて、ケノデオキシコール酸の投与が標準療法とし
(5~30%)
て記載されていること、審査報告書において本剤は脳腱黄色腫症に対する治療の第
一選択薬として医療現場に提供する意義はあると評価されていること等から、有用
性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
市場性 加算(Ⅰ)
該当しない
(10~20%)
市場性 加算(Ⅱ)
該当しない
(5%)
特 定 用 途 加 算
(5~20%)
小
該当しない
児 加 算
(5~20%)
該当しない
先 駆 加 算
(10~20%)
該当しない
迅速 導 入加算
(5~10%)
該当しない
新薬創出・適応外薬
解 消 等 促 進 加 算
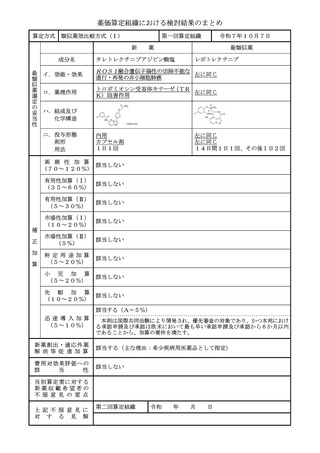
該当する(主な理由:希少疾病用医薬品として指定)
費用対効果評価への
該
当
性
該当しない
当初算定案に対する
新薬収載希望者の
不 服 意 見 の 要 点
上 記 不 服 意 見 に
対 す る 見 解
第二回算定組織
令和
11
年
月
日