よむ、つかう、まなぶ。
資料5 新たに定期接種に位置づけられるワクチンに係る副反応疑い報告基準について (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_00170.html |
| 出典情報 | 厚生科学審議会・薬事審議会(合同開催) 予防接種・ワクチン分科会副反応検討部会(第110回 2/4)医薬品等安全対策部会安全対策調査会(令和7年度第11回 2/4)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
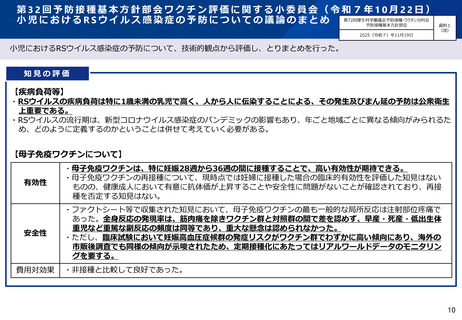
RSウイルス母子免疫ワクチンについて
○我が国におけるRSウイルス母子免疫ワクチンの薬事承認の内容等については、以下のとおり。
販売名
アブリスボ筋注用
一般名
組換えRSウイルスワクチン
製造販売業者
ファイザー株式会社
製造販売承認日
令和6年1月18日
販売開始日
令和6年5月31日
効能又は効果
○妊婦への能動免疫による新生児及び乳児におけるRSウイルスを原因とする下気道疾患の予防
○60歳以上の者におけるRSウイルスによる感染症の予防
効能又は効果に関連する注意
用法及び用量
〈妊婦への能動免疫による新生児及び乳児におけるRSウイルスを原因とする下気道疾患の予防〉
○本剤の臨床試験において生後6ヵ月までの有効性が検証されている。生後6ヵ月以降の有効性は確立していない。
○本剤の接種後14日以内に出生した乳児における有効性は確立していない。本剤の有効性は妊婦への能動免疫
により産生された抗体が胎児に移行することにより得られることから、本剤の接種後14日以内に出生した乳児において
は、胎児への抗体の移行が十分でない可能性がある。
〈妊婦への能動免疫による新生児及び乳児におけるRSウイルスを原因とする下気道疾患の予防〉
抗原製剤を専用溶解用液全量で溶解後、妊娠24~36週の妊婦に、1回0.5mLを筋肉内に接種する。
用法及び用量に関連する注意
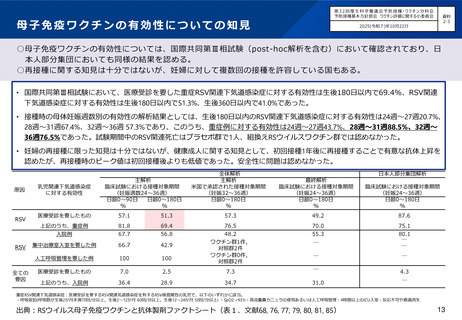
本剤は妊娠28~36週の間に接種することが望ましい。本剤の臨床試験において、妊娠28~36週に本剤を接種した
場合に有効性がより高い傾向が認められている。
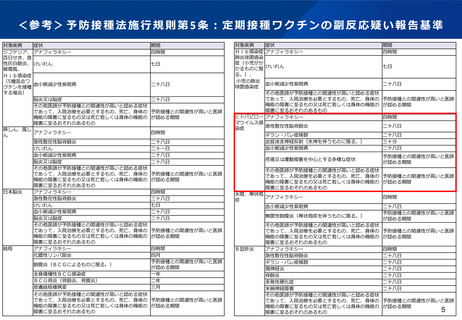
添付文書の「重大な副反応」の項
の記載
ショック、アナフィラキシー
9
○我が国におけるRSウイルス母子免疫ワクチンの薬事承認の内容等については、以下のとおり。
販売名
アブリスボ筋注用
一般名
組換えRSウイルスワクチン
製造販売業者
ファイザー株式会社
製造販売承認日
令和6年1月18日
販売開始日
令和6年5月31日
効能又は効果
○妊婦への能動免疫による新生児及び乳児におけるRSウイルスを原因とする下気道疾患の予防
○60歳以上の者におけるRSウイルスによる感染症の予防
効能又は効果に関連する注意
用法及び用量
〈妊婦への能動免疫による新生児及び乳児におけるRSウイルスを原因とする下気道疾患の予防〉
○本剤の臨床試験において生後6ヵ月までの有効性が検証されている。生後6ヵ月以降の有効性は確立していない。
○本剤の接種後14日以内に出生した乳児における有効性は確立していない。本剤の有効性は妊婦への能動免疫
により産生された抗体が胎児に移行することにより得られることから、本剤の接種後14日以内に出生した乳児において
は、胎児への抗体の移行が十分でない可能性がある。
〈妊婦への能動免疫による新生児及び乳児におけるRSウイルスを原因とする下気道疾患の予防〉
抗原製剤を専用溶解用液全量で溶解後、妊娠24~36週の妊婦に、1回0.5mLを筋肉内に接種する。
用法及び用量に関連する注意
本剤は妊娠28~36週の間に接種することが望ましい。本剤の臨床試験において、妊娠28~36週に本剤を接種した
場合に有効性がより高い傾向が認められている。
添付文書の「重大な副反応」の項
の記載
ショック、アナフィラキシー
9