よむ、つかう、まなぶ。
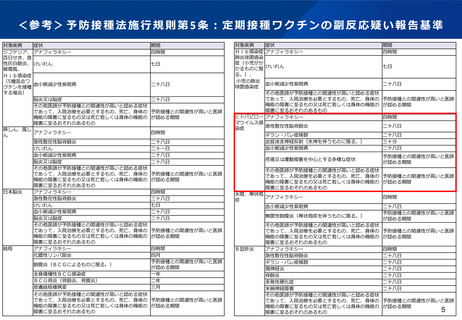
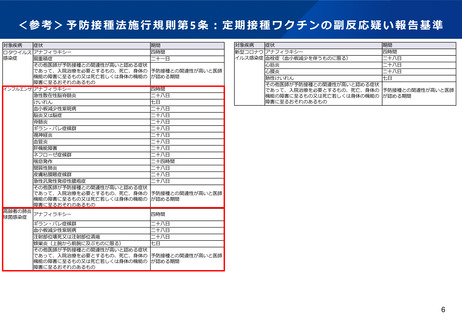
資料5 新たに定期接種に位置づけられるワクチンに係る副反応疑い報告基準について (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_00170.html |
| 出典情報 | 厚生科学審議会・薬事審議会(合同開催) 予防接種・ワクチン分科会副反応検討部会(第110回 2/4)医薬品等安全対策部会安全対策調査会(令和7年度第11回 2/4)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
RSウイルス母子免疫ワクチンの予診票について
第72回厚生科学審議会予防接種・ワクチン分科会
予防接種基本方針部会
資料1
(改)
2025(令和7)年11月19日
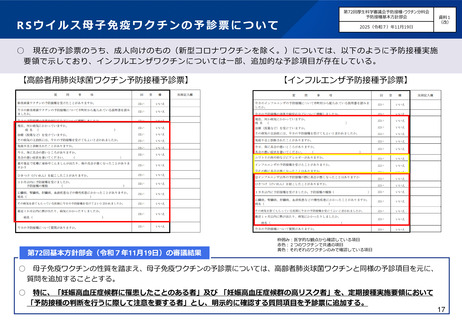
○ 現在の予診票のうち、成人向けのもの(新型コロナワクチンを除く。)については、以下のように予防接種実施
要領で示しており、インフルエンザワクチンについては一部、追加的な予診項目が存在している。
【高齢者用肺炎球菌ワクチン予防接種予診票】
第72回基本方針部会(令和7年11月19日)の審議結果
【インフルエンザ予防接種予診票】
枠囲み:医学的な観点から確認している項目
赤色:2つのワクチンで共通の項目
黄色:それぞれのワクチンのみで確認している項目
○
母子免疫ワクチンの性質を踏まえ、母子免疫ワクチンの予診票については、高齢者肺炎球菌ワクチンと同様の予診項目を元に、
質問を追加することとする。
○
特に、「妊娠高血圧症候群に罹患したことのある者」及び 「妊娠高血圧症候群の高リスク者」を、定期接種実施要領において
「予防接種の判断を行うに際して注意を要する者」とし、明示的に確認する質問項目を予診票に追加する。
17
第72回厚生科学審議会予防接種・ワクチン分科会
予防接種基本方針部会
資料1
(改)
2025(令和7)年11月19日
○ 現在の予診票のうち、成人向けのもの(新型コロナワクチンを除く。)については、以下のように予防接種実施
要領で示しており、インフルエンザワクチンについては一部、追加的な予診項目が存在している。
【高齢者用肺炎球菌ワクチン予防接種予診票】
第72回基本方針部会(令和7年11月19日)の審議結果
【インフルエンザ予防接種予診票】
枠囲み:医学的な観点から確認している項目
赤色:2つのワクチンで共通の項目
黄色:それぞれのワクチンのみで確認している項目
○
母子免疫ワクチンの性質を踏まえ、母子免疫ワクチンの予診票については、高齢者肺炎球菌ワクチンと同様の予診項目を元に、
質問を追加することとする。
○
特に、「妊娠高血圧症候群に罹患したことのある者」及び 「妊娠高血圧症候群の高リスク者」を、定期接種実施要領において
「予防接種の判断を行うに際して注意を要する者」とし、明示的に確認する質問項目を予診票に追加する。
17