よむ、つかう、まなぶ。
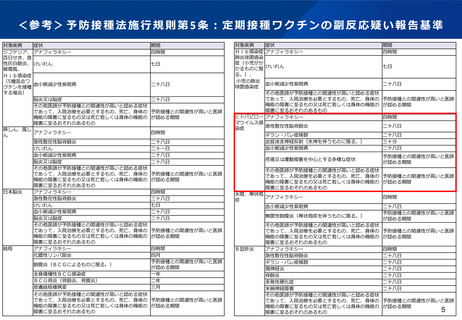
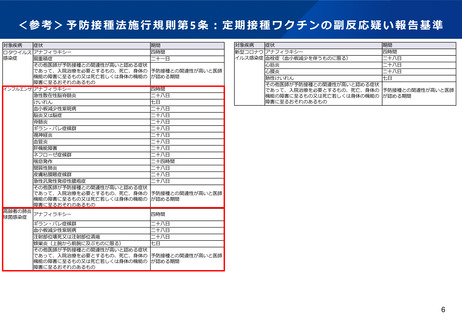
資料5 新たに定期接種に位置づけられるワクチンに係る副反応疑い報告基準について (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_00170.html |
| 出典情報 | 厚生科学審議会・薬事審議会(合同開催) 予防接種・ワクチン分科会副反応検討部会(第110回 2/4)医薬品等安全対策部会安全対策調査会(令和7年度第11回 2/4)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
母子免疫ワクチンの安全性についての知見:
国際共同第Ⅲ相試験日本人部分集団に関する評価
第32回厚生科学審議会予防接種・ワクチン分科会
予防接種基本方針部会 ワクチン評価に関する小委員会
2025(令和7)年10月22日
資料
2-3
○母子免疫ワクチンの安全性について、国際共同第Ⅲ相試験の日本人部分集団に関する解析において確認されている。
• 妊娠24週~36週の49歳以下の妊婦を対象として実施された国際共同第Ⅲ相試験の日本人部分集団を対象に解析。
• 母体の安全性の傾向は国際共同試験全体の結果と一致していた。最も一般的な局所反応は注射部位疼痛であった。全身反応の発現率
は、筋肉痛を除きワクチン群と対照群の間で差を認めなかった。
• 児の安全性に関する報告の傾向は、副反応及び重篤な副反応の発症について国際共同試験全体の結果と一致していたが、ともに高い
傾向を示した。低出生体重児(2,500g以下)はワクチン群: 6.9%・対照群: 9.7%と、全体集団と同様に両群間で差は認めなかった。
母体における接種後副反応の発症率
局所反応
出生した新生児における有害事象の発症率
全身反応
出典:RSウイルス母子免疫ワクチンと抗体製剤ファクトシート(文献79)
14
国際共同第Ⅲ相試験日本人部分集団に関する評価
第32回厚生科学審議会予防接種・ワクチン分科会
予防接種基本方針部会 ワクチン評価に関する小委員会
2025(令和7)年10月22日
資料
2-3
○母子免疫ワクチンの安全性について、国際共同第Ⅲ相試験の日本人部分集団に関する解析において確認されている。
• 妊娠24週~36週の49歳以下の妊婦を対象として実施された国際共同第Ⅲ相試験の日本人部分集団を対象に解析。
• 母体の安全性の傾向は国際共同試験全体の結果と一致していた。最も一般的な局所反応は注射部位疼痛であった。全身反応の発現率
は、筋肉痛を除きワクチン群と対照群の間で差を認めなかった。
• 児の安全性に関する報告の傾向は、副反応及び重篤な副反応の発症について国際共同試験全体の結果と一致していたが、ともに高い
傾向を示した。低出生体重児(2,500g以下)はワクチン群: 6.9%・対照群: 9.7%と、全体集団と同様に両群間で差は認めなかった。
母体における接種後副反応の発症率
局所反応
出生した新生児における有害事象の発症率
全身反応
出典:RSウイルス母子免疫ワクチンと抗体製剤ファクトシート(文献79)
14