よむ、つかう、まなぶ。
特定細胞加工物の微生物学的安全性指針(案)[1.1MB] (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_63117.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第110回 9/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
未定稿
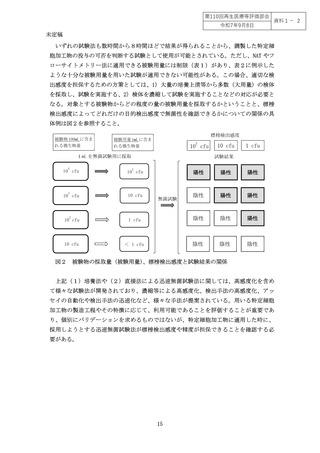
局方無菌試験に沿った試験実施を求めることは現実的ではない場合がある。そのため、
投与方法や投与量によるリスクを考慮し、局方無菌試験の実施が困難である場合は、リ
スクベースの迅速無菌試験を実施することが有用である(別添1表1、図2)。
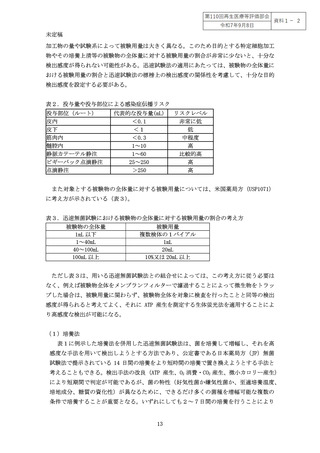
例えば、採取した細胞を培養し製造した特定細胞加工物を血中に投与する場合には高
いリスクが想定され、無菌試験の実施が必須である。一方、数 10mL の自己血液から医療
機器として承認されたキットを用いて PRP を調製し、抜歯等の後の止血や組織再生を目
的に使用(皮下投与)する場合には汚染による感染症発症のリスクは低く、無菌試験の
実施を不要とする判断が可能な場合もありうるかもしれない(別添1表2)。但し投与
部位を含めたリスクの評価が必要である。その一方で培養工程を伴わない特定細胞加工
物であっても定期的に無菌試験を実施し、無菌製造工程の完全性を担保することが重要
である(3(3)参照)
。
(2) 検出感度の考え方
無菌製剤に適用される医薬品の局方無菌試験の検出感度は、1cfu/検体とされ、実質
的に検体に対してほぼ 100%の無菌性を担保しているが、このような感度を特定細胞加
工物に適用することは試験に供しうる検体量や時間的制約等から現実的でない場合があ
る。一方で、非培養条件又は数日程度の培養下での濁度の目視やグラム染色のみを、無
菌試験として採用することは検出感度の点から無菌試験法として不適切である(ただし、
培養法と併用した迅速無菌試験を工程の確認のための試験や検体を濃縮して、その濃縮
物に対してグラム染色試験を用いることはあり得る)。
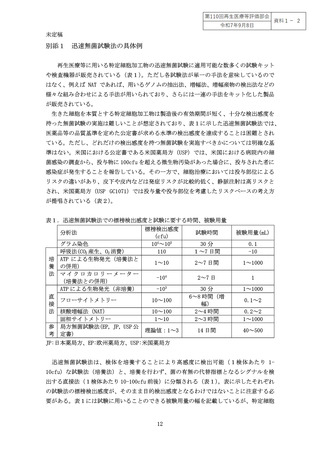
迅速 無菌試験 法として利用 される各 種試験法の標 榜上の検 出限界値(Limit-ofdetection:LOD)(以下、「標榜検出感度」という。)を別添1表1に例示している。こ
こに示している検出感度は、各試験法での検査対象とした検体に含まれる細菌に対する
「標榜上の検出感度」であり、無菌試験の対象(特定細胞加工物、その培養液又は適切
な洗浄液。以下「被験物」という。)の全体量に占める試験に供するために採取する検
体量(以下「被験用量」という。)の割合やメンブランフィルター法などの濃縮法の適
用の有無によって最終的に求めるべき被験物の全体量に対する検出限界値(以下「目的
検出感度」という。)は異なってくる。すなわち、標榜検出感度は、目的とする個別の
特定細胞加工物に対して必要とされる目的検出感度を表しているわけではないことに注
意する必要がある。検出感度の考え方の詳細については、5.(2)①を参照すること。
(3) 無菌試験実施のタイミングや検体の選択に関する考え方
どの無菌試験をどのタイミングでどの検体を用いて実施するかは、提供される再生医
療等のリスク分類(第一種、第二種、第三種)や製法の違いで異なる。例えば、第一種
では同種細胞から製造された特定細胞加工物がロットを形成している場合もあり、その
場合、構成するロット中から適切な数量の検体をサンプリングし、無菌試験に供するこ
とによって、構成するロット全体の無菌性を評価することも可能となる。
6
局方無菌試験に沿った試験実施を求めることは現実的ではない場合がある。そのため、
投与方法や投与量によるリスクを考慮し、局方無菌試験の実施が困難である場合は、リ
スクベースの迅速無菌試験を実施することが有用である(別添1表1、図2)。
例えば、採取した細胞を培養し製造した特定細胞加工物を血中に投与する場合には高
いリスクが想定され、無菌試験の実施が必須である。一方、数 10mL の自己血液から医療
機器として承認されたキットを用いて PRP を調製し、抜歯等の後の止血や組織再生を目
的に使用(皮下投与)する場合には汚染による感染症発症のリスクは低く、無菌試験の
実施を不要とする判断が可能な場合もありうるかもしれない(別添1表2)。但し投与
部位を含めたリスクの評価が必要である。その一方で培養工程を伴わない特定細胞加工
物であっても定期的に無菌試験を実施し、無菌製造工程の完全性を担保することが重要
である(3(3)参照)
。
(2) 検出感度の考え方
無菌製剤に適用される医薬品の局方無菌試験の検出感度は、1cfu/検体とされ、実質
的に検体に対してほぼ 100%の無菌性を担保しているが、このような感度を特定細胞加
工物に適用することは試験に供しうる検体量や時間的制約等から現実的でない場合があ
る。一方で、非培養条件又は数日程度の培養下での濁度の目視やグラム染色のみを、無
菌試験として採用することは検出感度の点から無菌試験法として不適切である(ただし、
培養法と併用した迅速無菌試験を工程の確認のための試験や検体を濃縮して、その濃縮
物に対してグラム染色試験を用いることはあり得る)。
迅速 無菌試験 法として利用 される各 種試験法の標 榜上の検 出限界値(Limit-ofdetection:LOD)(以下、「標榜検出感度」という。)を別添1表1に例示している。こ
こに示している検出感度は、各試験法での検査対象とした検体に含まれる細菌に対する
「標榜上の検出感度」であり、無菌試験の対象(特定細胞加工物、その培養液又は適切
な洗浄液。以下「被験物」という。)の全体量に占める試験に供するために採取する検
体量(以下「被験用量」という。)の割合やメンブランフィルター法などの濃縮法の適
用の有無によって最終的に求めるべき被験物の全体量に対する検出限界値(以下「目的
検出感度」という。)は異なってくる。すなわち、標榜検出感度は、目的とする個別の
特定細胞加工物に対して必要とされる目的検出感度を表しているわけではないことに注
意する必要がある。検出感度の考え方の詳細については、5.(2)①を参照すること。
(3) 無菌試験実施のタイミングや検体の選択に関する考え方
どの無菌試験をどのタイミングでどの検体を用いて実施するかは、提供される再生医
療等のリスク分類(第一種、第二種、第三種)や製法の違いで異なる。例えば、第一種
では同種細胞から製造された特定細胞加工物がロットを形成している場合もあり、その
場合、構成するロット中から適切な数量の検体をサンプリングし、無菌試験に供するこ
とによって、構成するロット全体の無菌性を評価することも可能となる。
6