よむ、つかう、まなぶ。
特定細胞加工物の微生物学的安全性指針(案)[1.1MB] (15 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_63117.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第110回 9/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
未定稿
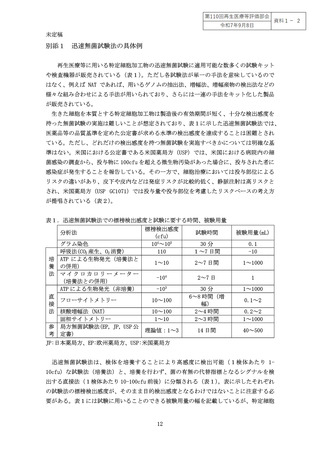
いずれの試験法も数時間から8時間ほどで結果が得られることから、調製した特定細
胞加工物の投与の可否を判断する試験として使用が可能とされている。ただし、NAT やフ
ローサイトメトリー法に適用できる被験用量には制限(表1)があり、表2に例示した
ような十分な被験用量を用いた試験が適用できない可能性がある。この場合、適切な検
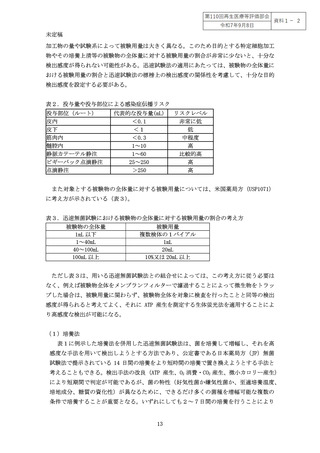
出感度を担保するための方策としては、1)大量の培養上清等から多数(大用量)の検体
を採取し、試験を実施する、2)検体を濃縮して試験を実施することなどの対応が必要と
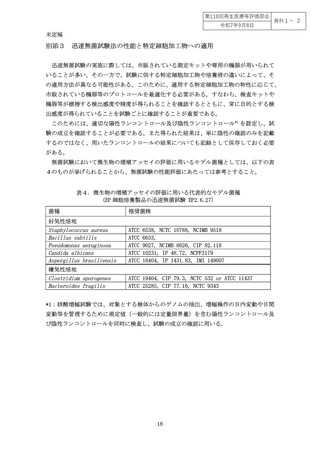
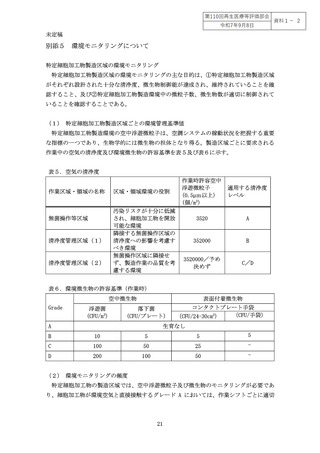
なる。対象とする被験物からどの程度の量の被験用量を採取するかということと、標榜
検出感度によってどれだけの目的検出感度で無菌性を確認できるかについての関係の具
体例は図2を参照すること。
被験物 100mL に含ま
れる微生物量
標榜検出感度
被験用量 1mL に含ま
れる微生物量
2
10 cfu
1mL を無菌試験用に採取
4
10 cfu
3
10 cfu
10 cfu
1 cfu
試験結果
2
10 cfu
10 cfu
無菌試験
陽性
陽性
陽性
陰性
陽性
陽性
10 cfu
1 cfu
陰性
陰性
陽性
10 cfu
< 1a cfu
陰性
陰性
陰性
2
図2 被験物の採取量(被験用量)
、標榜検出感度と試験結果の関係
上記(1)培養法や(2)直接法による迅速無菌試験法に関しては、高感度化を含め
て様々な試験法が開発されており、濃縮等による高感度化、検出手法の高感度化、アッ
セイの自動化や検出手法の迅速化など、様々な手法が提案されている。用いる特定細胞
加工物の製造工程やその特徴に応じて、利用可能であることを評価することが重要であ
り、個別にバリデーションを求めるものではないが、特定細胞加工物に適用した時に、
採用しようとする迅速無菌試験法が標榜検出感度や精度が担保できることを確認する必
要がある。
15
いずれの試験法も数時間から8時間ほどで結果が得られることから、調製した特定細
胞加工物の投与の可否を判断する試験として使用が可能とされている。ただし、NAT やフ
ローサイトメトリー法に適用できる被験用量には制限(表1)があり、表2に例示した
ような十分な被験用量を用いた試験が適用できない可能性がある。この場合、適切な検
出感度を担保するための方策としては、1)大量の培養上清等から多数(大用量)の検体
を採取し、試験を実施する、2)検体を濃縮して試験を実施することなどの対応が必要と
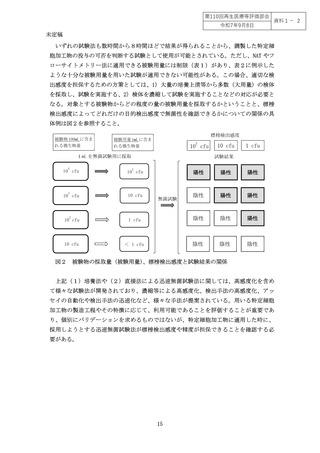
なる。対象とする被験物からどの程度の量の被験用量を採取するかということと、標榜
検出感度によってどれだけの目的検出感度で無菌性を確認できるかについての関係の具
体例は図2を参照すること。
被験物 100mL に含ま
れる微生物量
標榜検出感度
被験用量 1mL に含ま
れる微生物量
2
10 cfu
1mL を無菌試験用に採取
4
10 cfu
3
10 cfu
10 cfu
1 cfu
試験結果
2
10 cfu
10 cfu
無菌試験
陽性
陽性
陽性
陰性
陽性
陽性
10 cfu
1 cfu
陰性
陰性
陽性
10 cfu
< 1a cfu
陰性
陰性
陰性
2
図2 被験物の採取量(被験用量)
、標榜検出感度と試験結果の関係
上記(1)培養法や(2)直接法による迅速無菌試験法に関しては、高感度化を含め
て様々な試験法が開発されており、濃縮等による高感度化、検出手法の高感度化、アッ
セイの自動化や検出手法の迅速化など、様々な手法が提案されている。用いる特定細胞
加工物の製造工程やその特徴に応じて、利用可能であることを評価することが重要であ
り、個別にバリデーションを求めるものではないが、特定細胞加工物に適用した時に、
採用しようとする迅速無菌試験法が標榜検出感度や精度が担保できることを確認する必
要がある。
15