よむ、つかう、まなぶ。
特定細胞加工物の微生物学的安全性指針(案)[1.1MB] (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_63117.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第110回 9/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
未定稿
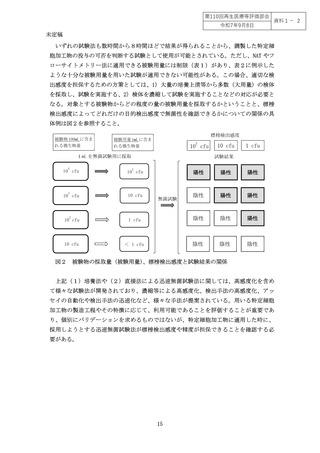
加工物の量や試験系によって被験用量は大きく異なる。このため目的とする特定細胞加工
物やその培養上清等の被験物の全体量に対する被験用量の割合が非常に少ないと、十分な
検出感度が得られない可能性がある。迅速試験法の適用にあたっては、被験物の全体量に
おける被験用量の割合と迅速試験法の標榜上の検出感度の関係性を考慮して、十分な目的
検出感度を設定する必要がある。
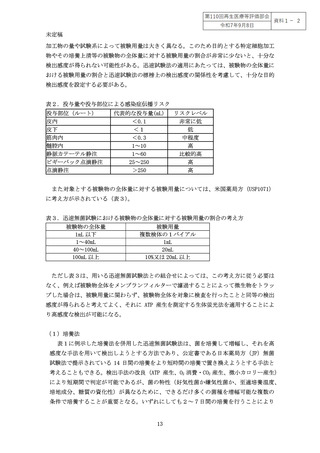
表2.投与量や投与部位による感染症伝播リスク
投与部位(ルート)
皮内
皮下
筋肉内
髄腔内
静脈カテーテル静注
ピギーバック点滴静注
点滴静注
代表的な投与量(mL)
<0.1
<1
<0.3
1~10
1~60
25~250
>250
リスクレベル
非常に低
低
中程度
高
比較的高
高
高
また対象とする被験物の全体量に対する被験用量については、米国薬局方(USP1071)
に考え方が示されている(表3)。
表3.迅速無菌試験における被験物の全体量に対する被験用量の割合の考え方
被験物の全体量
1mL 以下
1~40mL
40~100mL
100mL 以上
被験用量
複数検体の1バイアル
1mL
20mL
10%又は 20mL 以上
ただし表3は、用いる迅速無菌試験法との組合せによっては、この考え方に従う必要は
なく、例えば被験物全体をメンブランフィルターで濾過することによって微生物をトラッ
プした場合は、被験用量に関わらず、被験物全体を対象に検査を行ったことと同等の検出
感度が得られると考えてよく、それに ATP 産生を測定する生体蛍光法を適用することによ
り高感度な検出が可能になる。
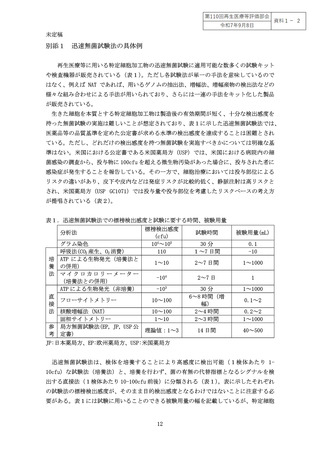
(1)培養法
表1に例示した培養法を併用した迅速無菌試験法は、菌を培養して増幅し、それを高
感度な手法を用いて検出しようとする方法であり、公定書である日本薬局方(JP)無菌
試験法で提示されている 14 日間の培養をより短時間の培養で置き換えようとする手法と
考えることもできる。検出手法の改良(ATP 産生、O2 消費・CO2 産生、微小カロリー産生)
により短期間で判定が可能であるが、菌の特性(好気性菌か嫌気性菌か、至適培養温度、
培地成分、糖質の資化性)が異なるために、できるだけ多くの菌種を増幅可能な複数の
条件で培養することが重要となる。いずれにしても2~7日間の培養を行うことにより
13
加工物の量や試験系によって被験用量は大きく異なる。このため目的とする特定細胞加工
物やその培養上清等の被験物の全体量に対する被験用量の割合が非常に少ないと、十分な
検出感度が得られない可能性がある。迅速試験法の適用にあたっては、被験物の全体量に
おける被験用量の割合と迅速試験法の標榜上の検出感度の関係性を考慮して、十分な目的
検出感度を設定する必要がある。
表2.投与量や投与部位による感染症伝播リスク
投与部位(ルート)
皮内
皮下
筋肉内
髄腔内
静脈カテーテル静注
ピギーバック点滴静注
点滴静注
代表的な投与量(mL)
<0.1
<1
<0.3
1~10
1~60
25~250
>250
リスクレベル
非常に低
低
中程度
高
比較的高
高
高
また対象とする被験物の全体量に対する被験用量については、米国薬局方(USP1071)
に考え方が示されている(表3)。
表3.迅速無菌試験における被験物の全体量に対する被験用量の割合の考え方
被験物の全体量
1mL 以下
1~40mL
40~100mL
100mL 以上
被験用量
複数検体の1バイアル
1mL
20mL
10%又は 20mL 以上
ただし表3は、用いる迅速無菌試験法との組合せによっては、この考え方に従う必要は
なく、例えば被験物全体をメンブランフィルターで濾過することによって微生物をトラッ
プした場合は、被験用量に関わらず、被験物全体を対象に検査を行ったことと同等の検出
感度が得られると考えてよく、それに ATP 産生を測定する生体蛍光法を適用することによ
り高感度な検出が可能になる。
(1)培養法
表1に例示した培養法を併用した迅速無菌試験法は、菌を培養して増幅し、それを高
感度な手法を用いて検出しようとする方法であり、公定書である日本薬局方(JP)無菌
試験法で提示されている 14 日間の培養をより短時間の培養で置き換えようとする手法と
考えることもできる。検出手法の改良(ATP 産生、O2 消費・CO2 産生、微小カロリー産生)
により短期間で判定が可能であるが、菌の特性(好気性菌か嫌気性菌か、至適培養温度、
培地成分、糖質の資化性)が異なるために、できるだけ多くの菌種を増幅可能な複数の
条件で培養することが重要となる。いずれにしても2~7日間の培養を行うことにより
13