よむ、つかう、まなぶ。
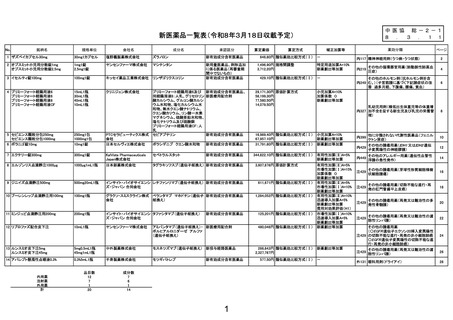
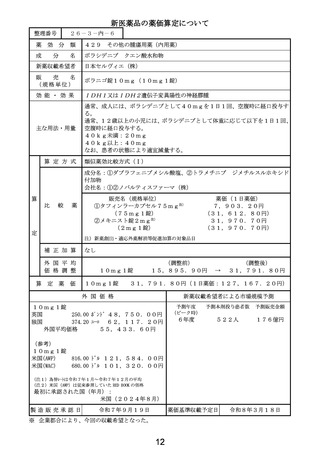
総-2-1医薬品の新規薬価収載等について (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71462.html |
| 出典情報 | 中央社会保険医療協議会 総会(第648回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
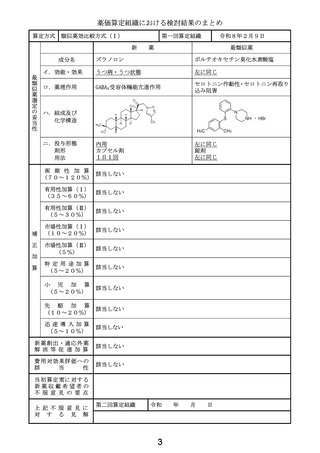
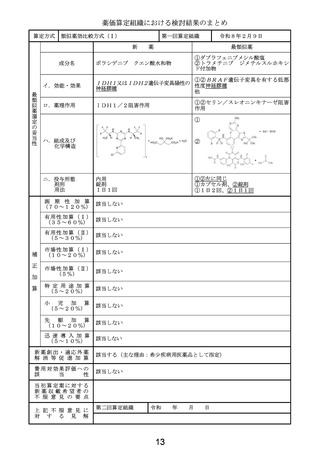
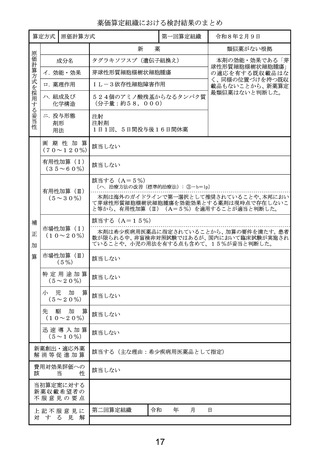
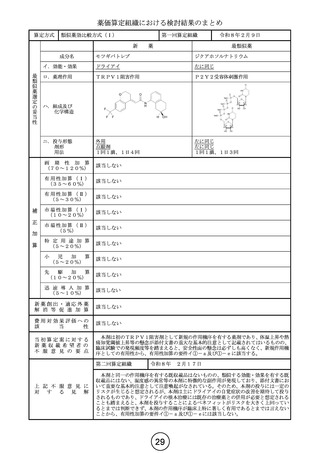
薬価算定組織における検討結果のまとめ
算定方式
原
価
計
算
方
式
を
採
用
す
る
妥
当
性
原価計算方式
第一回算定組織
新
成分名
令和8年2月9日
薬
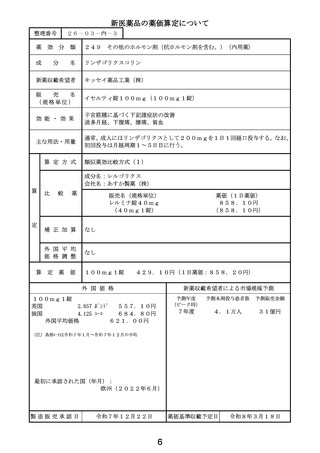
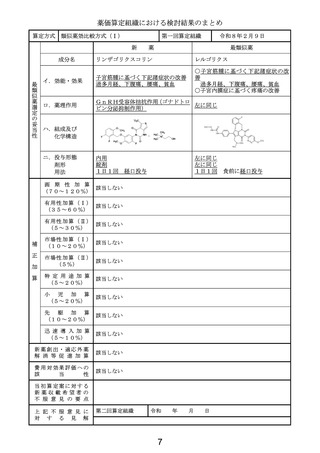
類似薬がない根拠
タグラキソフスプ(遺伝子組換え)
イ.効能・効果
芽球性形質細胞様樹状細胞腫瘍
ロ.薬理作用
IL-3依存性細胞障害作用
ハ.組成及び
化学構造
524個のアミノ酸残基からなるタンパク質
(分子量:約58,000)
ニ.投与形態
剤形
用法
注射
注射剤
1日1回、5日間投与後16日間休薬
本剤の効能・効果である「芽
球性形質細胞様樹状細胞腫瘍」
の適応を有する既収載品はな
く、同様の位置づけを持つ既収
載品もないことから、新薬算定
最類似薬はないと判断した。
画 期 性 加 算
該当しない
(70~120%)
有用性加算(Ⅰ)
該当しない
(35~60%)
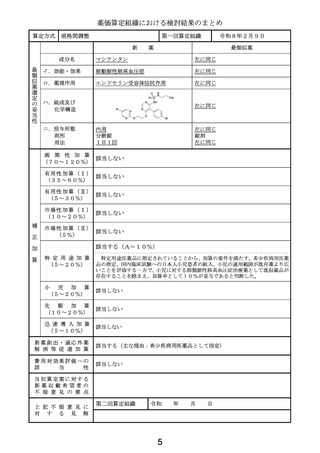
該当する(A=5%)
有用性加算(Ⅱ)
(5~30%)
〔ハ.治療方法の改善(標準的治療法): ③-b=1p〕
本剤は海外のガイドラインで第一選択として推奨されていることや、本邦におい
て芽球性形質細胞様樹状細胞腫瘍を効能効果とする薬剤は現時点で存在しないこ
と等から、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
該当する(A=15%)
補
市場性加算(Ⅰ)
本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。患者
(10~20%) 数が限られる中、非盲検非対照試験ではあるが、国内において臨床試験が実施され
ていることや、小児の用法を有する点も含めて、15%が妥当と判断した。
加
正
算 市場性加算(Ⅱ) 該当しない
(5%)
特定 用 途加算
該当しない
(5~20%)
小 児 加 算
該当しない
(5~20%)
先 駆 加 算
該当しない
(10~20%)
迅速 導 入加算
該当しない
(5~10%)
新薬創出・適応外薬
解消等促進加算
該当する(主な理由:希少疾病用医薬品として指定)
費用対効果評価への
該
当
性
該当しない
当初算定案に対する
新薬収載希望者の
不服意見の要点
上記不服意見に
対 す る 見 解
第二回算定組織
令和
17
年
月
日
算定方式
原
価
計
算
方
式
を
採
用
す
る
妥
当
性
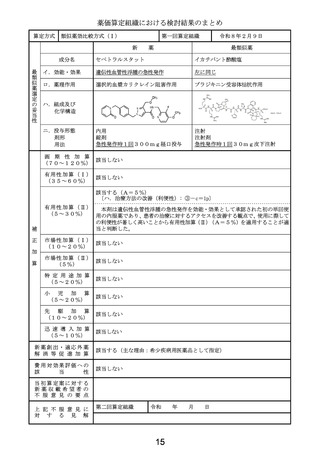
原価計算方式
第一回算定組織
新
成分名
令和8年2月9日
薬
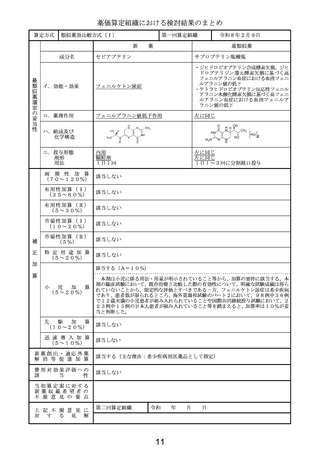
類似薬がない根拠
タグラキソフスプ(遺伝子組換え)
イ.効能・効果
芽球性形質細胞様樹状細胞腫瘍
ロ.薬理作用
IL-3依存性細胞障害作用
ハ.組成及び
化学構造
524個のアミノ酸残基からなるタンパク質
(分子量:約58,000)
ニ.投与形態
剤形
用法
注射
注射剤
1日1回、5日間投与後16日間休薬
本剤の効能・効果である「芽
球性形質細胞様樹状細胞腫瘍」
の適応を有する既収載品はな
く、同様の位置づけを持つ既収
載品もないことから、新薬算定
最類似薬はないと判断した。
画 期 性 加 算
該当しない
(70~120%)
有用性加算(Ⅰ)
該当しない
(35~60%)
該当する(A=5%)
有用性加算(Ⅱ)
(5~30%)
〔ハ.治療方法の改善(標準的治療法): ③-b=1p〕
本剤は海外のガイドラインで第一選択として推奨されていることや、本邦におい
て芽球性形質細胞様樹状細胞腫瘍を効能効果とする薬剤は現時点で存在しないこ
と等から、有用性加算(Ⅱ)(A=5%)を適用することが適当と判断した。
該当する(A=15%)
補
市場性加算(Ⅰ)
本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。患者
(10~20%) 数が限られる中、非盲検非対照試験ではあるが、国内において臨床試験が実施され
ていることや、小児の用法を有する点も含めて、15%が妥当と判断した。
加
正
算 市場性加算(Ⅱ) 該当しない
(5%)
特定 用 途加算
該当しない
(5~20%)
小 児 加 算
該当しない
(5~20%)
先 駆 加 算
該当しない
(10~20%)
迅速 導 入加算
該当しない
(5~10%)
新薬創出・適応外薬
解消等促進加算
該当する(主な理由:希少疾病用医薬品として指定)
費用対効果評価への
該
当
性
該当しない
当初算定案に対する
新薬収載希望者の
不服意見の要点
上記不服意見に
対 す る 見 解
第二回算定組織
令和
17
年
月
日