よむ、つかう、まなぶ。
資料4 Ⅳ-112,140_メトトレキサート[1.5MB] (62 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00045.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第67回 2/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
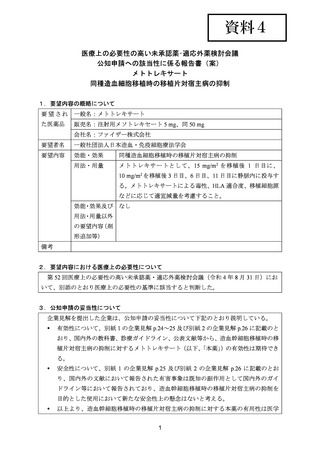
(公知申請への該当性に係る企業見解の様式)
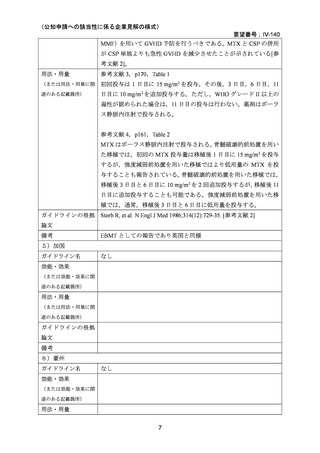
要望番号;IV-140
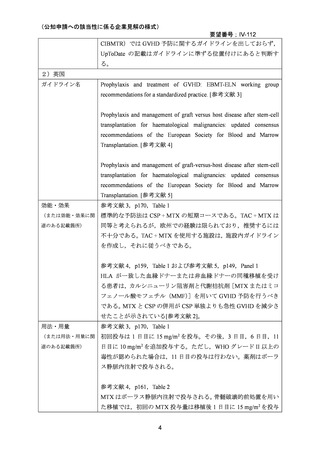
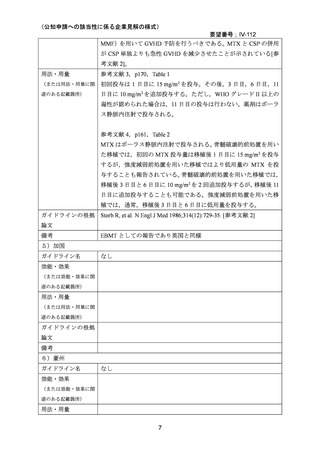
日本においては,無作為化試験の報告はなかったものの,骨髄移植または臍帯血移植を受
けた患者を対象として,移植登録一元管理プログラム登録データベースを用いた研究
37,38,44
,後ろ向き研究 19,39,40 が報告されている。小児または青少年を対象とした研究39,40,41,42,43
および使用実態調査 45 の報告もあり,小児または青少年においても MTX とカルシニュー
リン阻害剤の併用療法が標準的に行われていると考えられる。副作用として口内炎,肝障
害,骨髄抑制等があるが 36,既に添付文書において注意喚起されており新たな安全性の懸
念はないと考える。
以上のことから,要望されている効能・効果は妥当であると判断した。
【効能・効果】
造血幹細胞移植時の移植片対宿主病の抑制
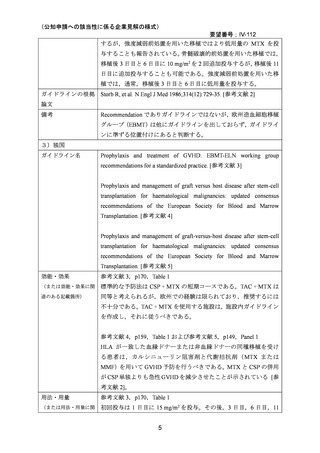
(2)用法・用量について
本剤とカルシニューリン阻害剤との併用においては,国内外のガイドラインで移植後 1 日
目に 15 mg/m2,3,6,11 日目に 10 mg/m2(日本造血・免疫細胞療法学会. 造血細胞移植ガ
イドライン GVHD(第 6 版)2025 [参考文献 36]における原法)の投与が MTX の用法・用
量として推奨されている。骨髄移植患者を対象とした無作為化試験においても,CSP また
は TAC との併用時は多くがこの用法・用量で検討されていた。ただし,米国および欧州の
ガイドラインでは,WHO グレード II 以上の毒性が認められた場合は,11 日目の投与は行
わないとされている。日本のガイドラインにおいては,11 日目の投与の省略,1 日目に 10
mg/m2,3,6 日目に 7 mg/m2 を投与する方法,1,3,6 日目に 5 mg/m2 を投与する方法も用
いられている旨の記載がある 36。また,移植登録一元管理プログラム登録データベースを
用いた研究 41,後ろ向き研究 39,40 で,11 日目の投与の省略,減量の検討が報告されている。
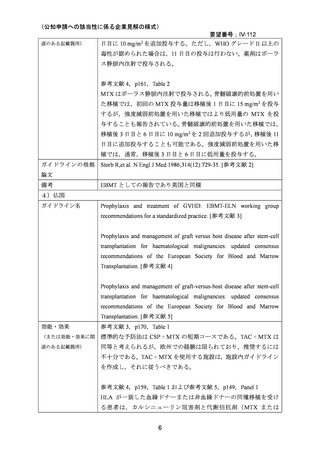
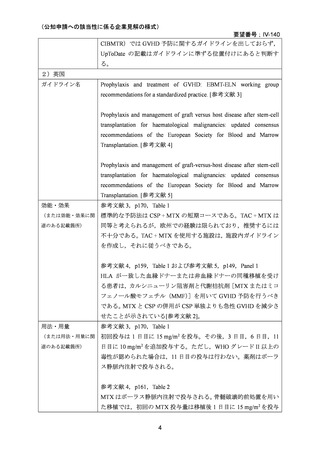
本邦で実施された同種造血細胞移植時の GVHD の抑制を目的とした本剤の用法・用量を評
価する使用実態調査 45 において,本剤の原法の使用割合が最も高かった一方で,投与量の
減量や移植後 11 日目の投与を省略するレジメン[10 mg/m2(day 1)および 7 mg/m2(day 3,
6)
(227 例,21.9%)
]が本邦で多く使用されている実態が明らかとなった。しかしながら,
本レジメンは,原法を基に一部を変更(減量)したレジメンであり,本調査に加えて国内
のガイドラインの記載および臨床試験成績の報告等も踏まえ,用法・用量および用法及び
用量に関連する注意を以下のとおり設定することが妥当と考える。
【用法・用量】
メトトレキサートとして,15 mg/m2 を移植後 1 日目に,10 mg/m2 を移植後 3 日目,6 日目,
11 日目に静脈内に投与する。患者の状態に応じて適宜減量する。
用法及び用量に関連する注意
27
要望番号;IV-140
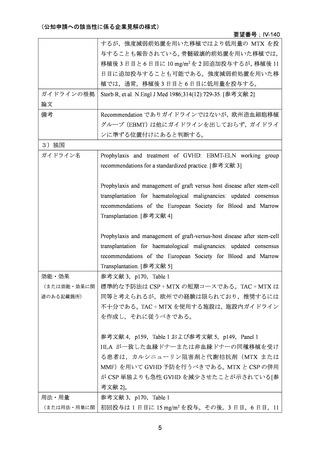
日本においては,無作為化試験の報告はなかったものの,骨髄移植または臍帯血移植を受
けた患者を対象として,移植登録一元管理プログラム登録データベースを用いた研究
37,38,44
,後ろ向き研究 19,39,40 が報告されている。小児または青少年を対象とした研究39,40,41,42,43
および使用実態調査 45 の報告もあり,小児または青少年においても MTX とカルシニュー
リン阻害剤の併用療法が標準的に行われていると考えられる。副作用として口内炎,肝障
害,骨髄抑制等があるが 36,既に添付文書において注意喚起されており新たな安全性の懸
念はないと考える。
以上のことから,要望されている効能・効果は妥当であると判断した。
【効能・効果】
造血幹細胞移植時の移植片対宿主病の抑制
(2)用法・用量について
本剤とカルシニューリン阻害剤との併用においては,国内外のガイドラインで移植後 1 日
目に 15 mg/m2,3,6,11 日目に 10 mg/m2(日本造血・免疫細胞療法学会. 造血細胞移植ガ
イドライン GVHD(第 6 版)2025 [参考文献 36]における原法)の投与が MTX の用法・用
量として推奨されている。骨髄移植患者を対象とした無作為化試験においても,CSP また
は TAC との併用時は多くがこの用法・用量で検討されていた。ただし,米国および欧州の
ガイドラインでは,WHO グレード II 以上の毒性が認められた場合は,11 日目の投与は行
わないとされている。日本のガイドラインにおいては,11 日目の投与の省略,1 日目に 10
mg/m2,3,6 日目に 7 mg/m2 を投与する方法,1,3,6 日目に 5 mg/m2 を投与する方法も用
いられている旨の記載がある 36。また,移植登録一元管理プログラム登録データベースを
用いた研究 41,後ろ向き研究 39,40 で,11 日目の投与の省略,減量の検討が報告されている。
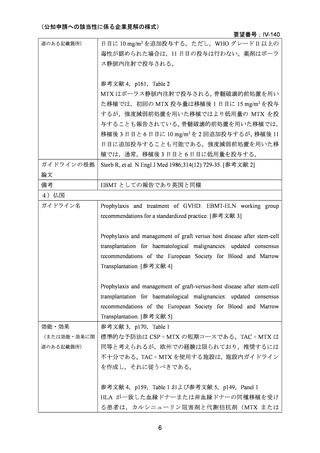
本邦で実施された同種造血細胞移植時の GVHD の抑制を目的とした本剤の用法・用量を評
価する使用実態調査 45 において,本剤の原法の使用割合が最も高かった一方で,投与量の
減量や移植後 11 日目の投与を省略するレジメン[10 mg/m2(day 1)および 7 mg/m2(day 3,
6)
(227 例,21.9%)
]が本邦で多く使用されている実態が明らかとなった。しかしながら,
本レジメンは,原法を基に一部を変更(減量)したレジメンであり,本調査に加えて国内
のガイドラインの記載および臨床試験成績の報告等も踏まえ,用法・用量および用法及び
用量に関連する注意を以下のとおり設定することが妥当と考える。
【用法・用量】
メトトレキサートとして,15 mg/m2 を移植後 1 日目に,10 mg/m2 を移植後 3 日目,6 日目,
11 日目に静脈内に投与する。患者の状態に応じて適宜減量する。
用法及び用量に関連する注意
27