よむ、つかう、まなぶ。
資料2-2-1 MID-NET・NDB の行政利活用の調査実施状況について[2.4MB] (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70725.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第4回 3/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
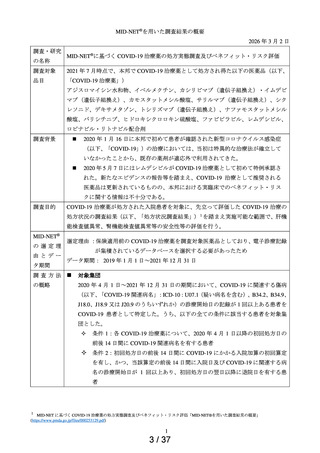
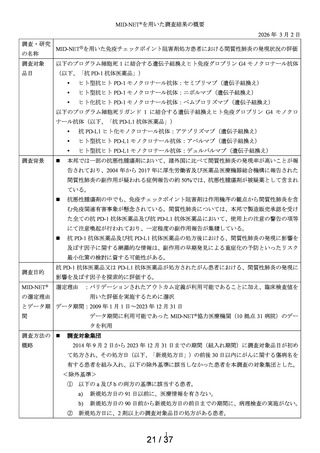
MID-NET®を用いた調査結果の概要
2026 年 3 月 2 日
調査・研究
の名称
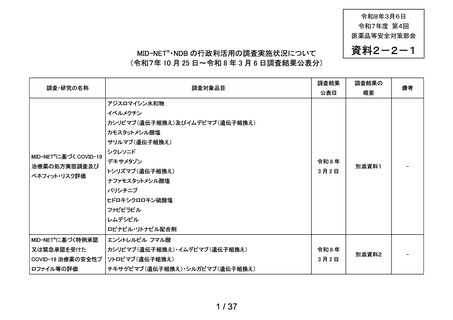
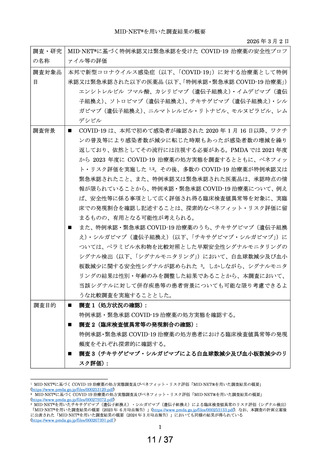
MID-NET®に基づく COVID-19 治療薬の処方実態調査及びベネフィット・リスク評価
調査対象
2021 年 7 月時点で、本邦で COVID-19 治療薬として処方され得た以下の医薬品(以下、
品目
「COVID-19 治療薬」)
アジスロマイシン水和物、イベルメクチン、カシリビマブ(遺伝子組換え)・イムデビ
マブ(遺伝子組換え)、カモスタットメシル酸塩、サリルマブ(遺伝子組換え)、シク
レソニド、デキサメタゾン、トシリズマブ(遺伝子組換え)、ナファモスタットメシル
酸塩、バリシチニブ、ヒドロキシクロロキン硫酸塩、ファビピラビル、レムデシビル、
ロピナビル・リトナビル配合剤
調査背景
2020 年 1 月 16 日に本邦で初めて患者が確認された新型コロナウイルス感染症
(以下、「COVID-19」)の治療においては、当初は特異的な治療法が確立して
いなかったことから、既存の薬剤が適応外で利用されてきた。
2020 年 5 月 7 日にはレムデシビルが COVID-19 治療薬として初めて特例承認さ
れた。新たなエビデンスの報告等を踏まえ、COVID-19 治療として推奨される
医薬品は更新されているものの、本邦における実臨床でのベネフィット・リス
クに関する情報は不十分である。
調査目的
COVID-19 治療薬が処方された入院患者を対象に、先立って評価した COVID-19 治療の
処方状況の調査結果(以下、「処方状況調査結果」)1を踏まえ実施可能な範囲で、肝機
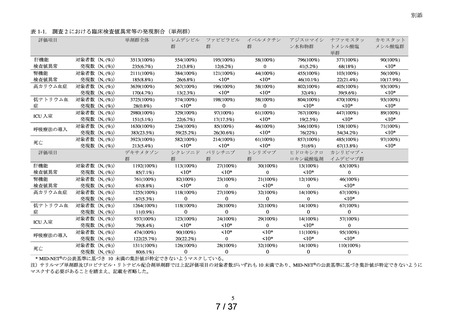
能検査値異常、腎機能検査値異常等の安全性等の評価を行う。
MID-NET
®
の選定理
由とデー
タ期間
選定理由 :保険適用前の COVID-19 治療薬を調査対象医薬品としており、電子診療記録
が集積されているデータベースを選択する必要があったため
データ期間: 2019 年 1 月 1 日~2021 年 12 月 31 日
調査方法
対象集団
の概略
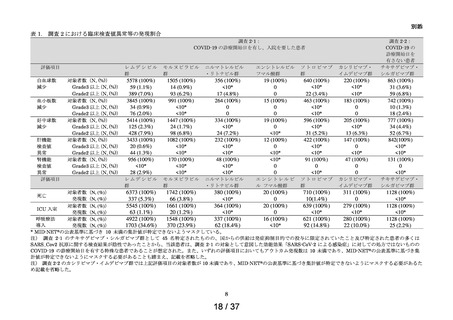
2020 年 4 月 1 日~2021 年 12 月 31 日の期間において、COVID-19 に関連する傷病
(以下、「COVID-19 関連病名」:ICD-10:U07.1(疑い病名を含む)、B34.2、B34.9、
J18.0、J18.9 又は J20.9 のうちいずれか)の診療開始日の記録が 1 回以上ある患者を
COVID-19 患者として特定した。うち、以下の全ての条件に該当する患者を対象集
団とした。
条件 1:各 COVID-19 治療薬について、2020 年 4 月 1 日以降の初回処方日の
前後 14 日間に COVID-19 関連病名を有する患者
条件 2:初回処方日の前後 14 日間に COVID-19 にかかる入院加算の初回算定
を有し、かつ、当該算定の前後 14 日間に入院日及び COVID-19 に関連する病
名の診療開始日が 1 回以上あり、初回処方日の翌日以降に退院日を有する患
者
1
MID-NET に基づく COVID-19 治療薬の処方実態調査及びベネフィット・リスク評価「MID-NET®を用いた調査結果の概要」
(https://www.pmda.go.jp/files/000253129.pdf)
1
3 / 37
2026 年 3 月 2 日
調査・研究
の名称
MID-NET®に基づく COVID-19 治療薬の処方実態調査及びベネフィット・リスク評価
調査対象
2021 年 7 月時点で、本邦で COVID-19 治療薬として処方され得た以下の医薬品(以下、
品目
「COVID-19 治療薬」)
アジスロマイシン水和物、イベルメクチン、カシリビマブ(遺伝子組換え)・イムデビ
マブ(遺伝子組換え)、カモスタットメシル酸塩、サリルマブ(遺伝子組換え)、シク
レソニド、デキサメタゾン、トシリズマブ(遺伝子組換え)、ナファモスタットメシル
酸塩、バリシチニブ、ヒドロキシクロロキン硫酸塩、ファビピラビル、レムデシビル、
ロピナビル・リトナビル配合剤
調査背景
2020 年 1 月 16 日に本邦で初めて患者が確認された新型コロナウイルス感染症
(以下、「COVID-19」)の治療においては、当初は特異的な治療法が確立して
いなかったことから、既存の薬剤が適応外で利用されてきた。
2020 年 5 月 7 日にはレムデシビルが COVID-19 治療薬として初めて特例承認さ
れた。新たなエビデンスの報告等を踏まえ、COVID-19 治療として推奨される
医薬品は更新されているものの、本邦における実臨床でのベネフィット・リス
クに関する情報は不十分である。
調査目的
COVID-19 治療薬が処方された入院患者を対象に、先立って評価した COVID-19 治療の
処方状況の調査結果(以下、「処方状況調査結果」)1を踏まえ実施可能な範囲で、肝機
能検査値異常、腎機能検査値異常等の安全性等の評価を行う。
MID-NET
®
の選定理
由とデー
タ期間
選定理由 :保険適用前の COVID-19 治療薬を調査対象医薬品としており、電子診療記録
が集積されているデータベースを選択する必要があったため
データ期間: 2019 年 1 月 1 日~2021 年 12 月 31 日
調査方法
対象集団
の概略
2020 年 4 月 1 日~2021 年 12 月 31 日の期間において、COVID-19 に関連する傷病
(以下、「COVID-19 関連病名」:ICD-10:U07.1(疑い病名を含む)、B34.2、B34.9、
J18.0、J18.9 又は J20.9 のうちいずれか)の診療開始日の記録が 1 回以上ある患者を
COVID-19 患者として特定した。うち、以下の全ての条件に該当する患者を対象集
団とした。
条件 1:各 COVID-19 治療薬について、2020 年 4 月 1 日以降の初回処方日の
前後 14 日間に COVID-19 関連病名を有する患者
条件 2:初回処方日の前後 14 日間に COVID-19 にかかる入院加算の初回算定
を有し、かつ、当該算定の前後 14 日間に入院日及び COVID-19 に関連する病
名の診療開始日が 1 回以上あり、初回処方日の翌日以降に退院日を有する患
者
1
MID-NET に基づく COVID-19 治療薬の処方実態調査及びベネフィット・リスク評価「MID-NET®を用いた調査結果の概要」
(https://www.pmda.go.jp/files/000253129.pdf)
1
3 / 37