よむ、つかう、まなぶ。
資料2-2-1 MID-NET・NDB の行政利活用の調査実施状況について[2.4MB] (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70725.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第4回 3/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
チキサゲビマブ・シルガビマブ及びペラミビル水和物の新規処方患者を対象に血球
減少及び血小板数減少の発現状況等を比較する。
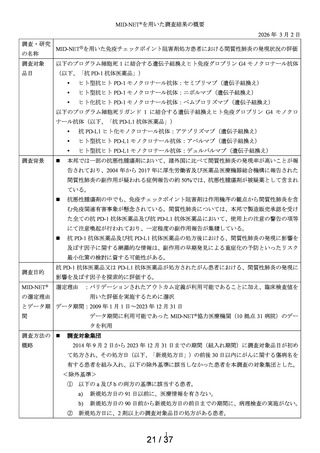
MID-NET® 選定理由:保険適用前の COVID-19 治療薬を調査対象医薬品としており、電子診療記録
の選定理
が集積されているデータベースを選択する必要があったため
由 と デ ー データ期間:2013 年 1 月 1 日~2023 年 12 月 31 日
データ期間に利用可能であった MID-NET®協力医療機関(10 拠点 32 病院)
タ期間
のデータを利用
調査方法の
調査の対象集団
概略
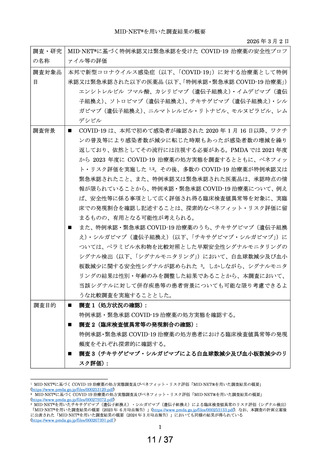
調査 1(処方状況の確認)
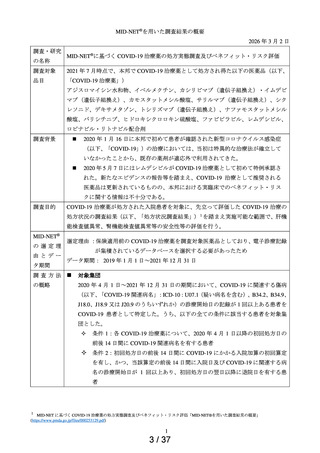
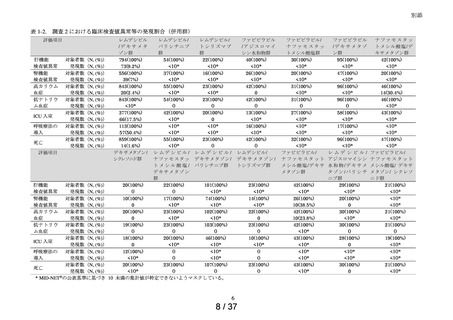
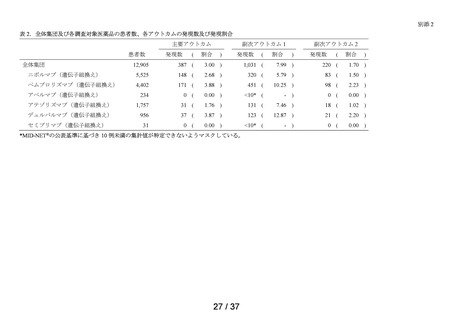
2020 年 1 月 1 日から 2023 年 12 月 31 日までの期間に特例承認・緊急承認 COVID19 治療薬の処方がある患者を調査の対象集団とした。
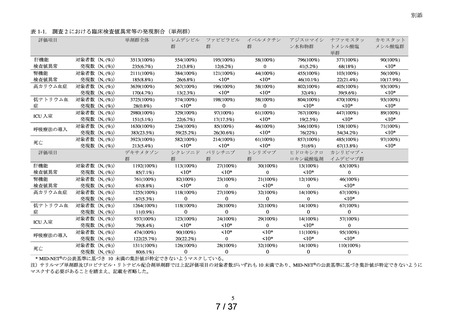
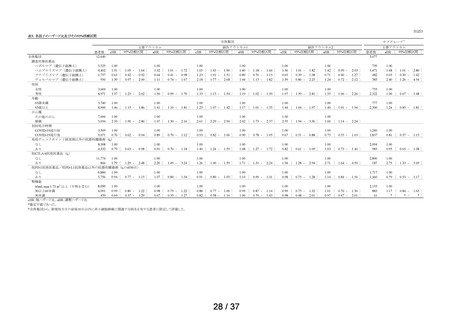
調査 2(臨床検査値異常等の発現割合の確認)
:
特例承認・緊急承認 COVID-19 治療薬のうち、チキサゲビマブ・シルガビマブ及
びカシリビマブ・イムデビマブは、効能効果が「SARS-CoV-2 による感染症及び
SARS-CoV-2 による感染症の発症抑制」であることから、調査の対象集団を以下の
通り 2 パターン設定した 4。
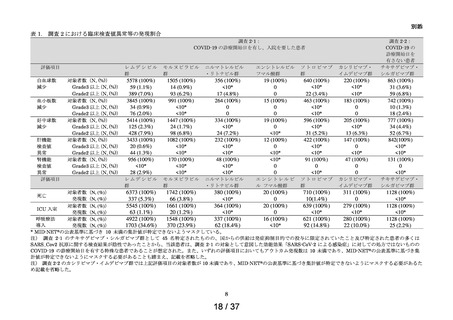
<調査 2-1: COVID-19 の診療開始日を有し、入院を要した患者>
2021 年 7 月 1 日から 2023 年 12 月 31 日までの期間において、特例承認・緊急承
認 COVID-19 治療薬の処方日があり、その処方日の前 14 日から処方日の翌日の範
囲に ICD-10 コードの U07.1(疑い病名含む)の診療開始日が 1 回以上ある患者を
特定し、この条件を満たす処方日のうち最も早い日を t0 とした。このうち、t0 の
前 14 日から t0 の翌日の範囲に入院日があり、対応する退院日が t0 の翌日以降に
あり、除外基準(「t0 の前 180 日から t0 までの期間の着目する臨床検査値が CTCAE
Grade 1 以上の事象又は欠測」等)に該当しない患者を調査の対象集団とし、t0 時
点で処方された特例承認・緊急承認 COVID-19 治療薬ごとに群分けを行った。
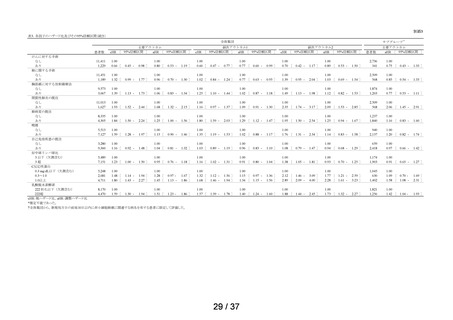
<調査 2-2: COVID-19 の診療開始日を有さない患者>
2021 年 7 月 1 日から 2023 年 12 月 31 日までの期間において、チキサゲビマブ・
シルガビマブ又はカシリビマブ・イムデビマブの処方がある患者を特定し、この期
間における処方日のうち最も早い日を t0 とした。このうち、データ期間中の最初の
医療記録日が t0 の 180 日以上前にあり、除外基準(「t0 の前 14 日から t0 までの期
間に ICD-10 コードの U07.1(疑い病名を含む)の診療開始日が 1 回以上ある」、
「t0 の前 180 日から t0 までの期間の着目する臨床検査値が CTCAE Grade 1 以上
の事象又は欠測」等)に該当しない患者を調査の対象集団とし、t0 時点で処方され
た特例承認・緊急承認 COVID-19 治療薬ごとに群分けを行った。
4
調査の計画立案時点ではチキサゲビマブ・シルガビマブは発症抑制目的での投与に限定されていたものの、使用予定のデータ期間には計画立
案時以降の期間も含めていたため、当該期間では上記限定が解除され治療目的でも投与可となっている可能性も考慮し、調査 2 では 2 パターン
を設定する計画とした。ただし、調査開始後もチキサゲビマブ・シルガビマブは発症抑制目的での投与に限定されたままであった
2
12 / 37
減少及び血小板数減少の発現状況等を比較する。
MID-NET® 選定理由:保険適用前の COVID-19 治療薬を調査対象医薬品としており、電子診療記録
の選定理
が集積されているデータベースを選択する必要があったため
由 と デ ー データ期間:2013 年 1 月 1 日~2023 年 12 月 31 日
データ期間に利用可能であった MID-NET®協力医療機関(10 拠点 32 病院)
タ期間
のデータを利用
調査方法の
調査の対象集団
概略
調査 1(処方状況の確認)
2020 年 1 月 1 日から 2023 年 12 月 31 日までの期間に特例承認・緊急承認 COVID19 治療薬の処方がある患者を調査の対象集団とした。
調査 2(臨床検査値異常等の発現割合の確認)
:
特例承認・緊急承認 COVID-19 治療薬のうち、チキサゲビマブ・シルガビマブ及
びカシリビマブ・イムデビマブは、効能効果が「SARS-CoV-2 による感染症及び
SARS-CoV-2 による感染症の発症抑制」であることから、調査の対象集団を以下の
通り 2 パターン設定した 4。
<調査 2-1: COVID-19 の診療開始日を有し、入院を要した患者>
2021 年 7 月 1 日から 2023 年 12 月 31 日までの期間において、特例承認・緊急承
認 COVID-19 治療薬の処方日があり、その処方日の前 14 日から処方日の翌日の範
囲に ICD-10 コードの U07.1(疑い病名含む)の診療開始日が 1 回以上ある患者を
特定し、この条件を満たす処方日のうち最も早い日を t0 とした。このうち、t0 の
前 14 日から t0 の翌日の範囲に入院日があり、対応する退院日が t0 の翌日以降に
あり、除外基準(「t0 の前 180 日から t0 までの期間の着目する臨床検査値が CTCAE
Grade 1 以上の事象又は欠測」等)に該当しない患者を調査の対象集団とし、t0 時
点で処方された特例承認・緊急承認 COVID-19 治療薬ごとに群分けを行った。
<調査 2-2: COVID-19 の診療開始日を有さない患者>
2021 年 7 月 1 日から 2023 年 12 月 31 日までの期間において、チキサゲビマブ・
シルガビマブ又はカシリビマブ・イムデビマブの処方がある患者を特定し、この期
間における処方日のうち最も早い日を t0 とした。このうち、データ期間中の最初の
医療記録日が t0 の 180 日以上前にあり、除外基準(「t0 の前 14 日から t0 までの期
間に ICD-10 コードの U07.1(疑い病名を含む)の診療開始日が 1 回以上ある」、
「t0 の前 180 日から t0 までの期間の着目する臨床検査値が CTCAE Grade 1 以上
の事象又は欠測」等)に該当しない患者を調査の対象集団とし、t0 時点で処方され
た特例承認・緊急承認 COVID-19 治療薬ごとに群分けを行った。
4
調査の計画立案時点ではチキサゲビマブ・シルガビマブは発症抑制目的での投与に限定されていたものの、使用予定のデータ期間には計画立
案時以降の期間も含めていたため、当該期間では上記限定が解除され治療目的でも投与可となっている可能性も考慮し、調査 2 では 2 パターン
を設定する計画とした。ただし、調査開始後もチキサゲビマブ・シルガビマブは発症抑制目的での投与に限定されたままであった
2
12 / 37